Valvulopathies et échocardiographie Doppler de stress

L
e domaine d’application de l’échocardiographie de
stress s’est étendu récemment à l’évaluation de la sévé-
rité des valvulopathies. Sa méthode de réalisation et
son interprétation sont spécifiques aux valvulopathies et diffè-
rent de celles utilisées pour l’étude de l’ischémie myocardique.
Nous proposons dans cet article de faire le point sur cette tech-
nique, et de développer plus particulièrement son application en
cas de rétrécissement aortique en bas débit et de rétrécissement
mitral asymptomatique.
RÉTRÉCISSEMENT AORTIQUE ET STRESS
Un rétrécissement aortique serré est défini comme une surface
aortique inférieure à 0,75 cm
2
ou 0,5 cm
2
/m
2
en échodoppler, ou
à 1 cm
2
par cathétérisme (1-3). Cette distinction est importante,
car il peut exister une différence significative entre ces deux types
de calcul. En effet, le phénomène de recouvrement de pression
post-sténotique est différent selon les situations rencontrées. En
cas d’aorte de petit diamètre (inférieure à 3 cm), le recouvrement
en pression se fait très tôt après la sténose, car la dissipation de
l’énergie en turbulence est minime et l’énergie cinétique se trans-
forme quasi intégralement en énergie hydrostatique, c’est-à-dire
en pression. Dans ce cas, le calcul par cathétérisme avec équation
de Gorlin aura tendance à retrouver une surface aortique signifi-
cativement plus grande que celle calculée par doppler avec l’équa-
tion de continuité, qui utilise le gradient transaortique au niveau
de la vena contracta, là où le gradient de pression est maximal.
Rétrécissement aortique serré asymptomatique
Le recours à la chirurgie en cas de RAC serré asymptomatique
est encore sujet à discussion. Les données sont en faveur d’une
abstention thérapeutique, car la mortalité opératoire est plus
importante que la mortalité spontanée (par mort subite le plus
souvent) : 2 % versus 1 % (4). Cependant, un sous-groupe de
patients présentant un plus mauvais pronostic a pu être identifié,
chez lequel la chirurgie peut être envisagée. On peut résumer
ainsi ses caractéristiques (5) :
–épreuve d’effort positive (sous-décalage de ST, douleur thora-
cique, lipothymie, arythmie ventriculaire complexe, chute ten-
sionnelle > 20 mmHg) ;
Valvulopathies
et échocardiographie Doppler de stress
Stress echocardiography and valvular diseases
●
E. Messas*
*Service de cardiologie, hôpital Necker, Paris.
■L’intérêt de l’échocardiographie Doppler de stress dans
l’évaluation et le traitement des valvulopathies est gran-
dissant.
■Les applications cliniques les plus fréquentes actuelle-
ment sont le rétrécissement aortique (RAC) serré en bas
débit et le rétrécissement mitral (RM) asymptomatique :
–écho-dobutamine pour le RAC serré en bas débit, à la
recherche d’une viabilité qui permet d’identifier un sous-
groupe à meilleur pronostic postopératoire ;
–échocardiographie d’effort pour le RM asymptomatique,
à la recherche d’une augmentation de la pression artérielle
pulmonaire systolique (PAPS) à l’effort et du gradient
moyen transmitral en faveur d’une intervention par com-
missurotomie percutanée.
■L’évaluation de l’insuffisance mitrale (IM) ischémique
a bénéficié récemment de cette technique, avec des études
cliniques démontrant l’intérêt de l’échocardiographie d’ef-
fort, qui permet d’identifier un sous-groupe de patients à
pronostic plus sévère et susceptible de faire des œdèmes
aigus pulmonaires (OAP).
■D’autres études sont encore nécessaires afin de préciser
l’indication de cette technique dans les autres valvulopa-
thies et de définir plus précisément sa place dans l’algo-
rithme décisionnel de la prise en charge des valvulopathies.
Mots-clés : Dobutamine - Exercice - Rétrécissement aor-
tique - Rétrécissement mitral.
Keywords: Dobutamine - Exercise - Aortic stenosis -
Mitral stenosis.
Points forts
MISE AU POINT
La Lettre du Cardiologue - n° 382 - février 2005
20

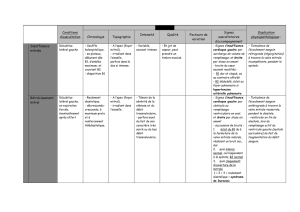
–pic de vélocité transaortique au doppler continu supérieur à
4m/s (figure 1) ;
–RAC rapidement progressif, avec augmentation supérieure à
0,3 cm
2
tous les six mois.
L’épreuve d’effort fait donc office de révélateur : elle peut démas-
quer des patients faussement asymptomatiques qui sont en fait
limités dans leur vie quotidienne et auront une épreuve d’effort
précocement positive. Dans d’autres cas, elle permet d’identifier
un groupe de patients avec valve peu compliante qui ne s’adapte
pas à l’effort.
Rétrécissement aortique serré symptomatique
En cas de RAC symptomatique, l’indication opératoire est for-
melle : l’épreuve d’effort n’est pas nécessaire, car le pronostic
spontané est mauvais. En effet, à ce stade, on retrouve 50 % de
survie à 5 ans en cas d’angor, 50 % à 3 ans en cas de syncope et
50 % à 2 ans en cas d’insuffisance cardiaque gauche (6).
Rétrécissement aortique avec dysfonction ventriculaire
gauche
La présence d’un RAC serré associé à une dysfonction ventricu-
laire gauche (VG) et à un faible gradient transaortique incite à la
réalisation d’une échocardiographie de stress à la recherche d’une
réserve contractile. Plusieurs études ont été réalisées sur le sujet
(7-10) ; elles convergent toutes vers un meilleur pronostic opé-
ratoire en cas de réserve contractile significative. Celle-ci est défi-
nie, selon les études, par une augmentation du volume d’éjection
systolique (VES) de 20 %, une augmentation de la fraction d’éjec-
tion (FE) de 10 % ou une augmentation de la surface aortique de
0,3 cm
2
(encadré).
Deux cas de figure sont possibles :
•En cas de RAC serré (< 1 cm
2
) avec dysfonction VG et gradient
moyen supérieur à 30 mmHg, on peut raisonnablement attribuer
la dysfonction VG à l’augmentation de la postcharge secondaire
au RAC (afterload mismatch). Dans ce cas, la chirurgie est de
meilleur pronostic, avec une amélioration de la dysfonction VG
en postopératoire après diminution de la postcharge (11).
•En cas de RAC serré avec dysfonction VG et gradient moyen
inférieur à 30 mmHg, la dysfonction VG peut être due à une perte
de la contractilité intrinsèque ou à l’augmentation de la post-
charge.
Dans ce cas, le but de l’étude hémodynamique doppler sous dobu-
tamine est double : rechercher une réserve contractile et préciser
la réelle sévérité du RAC (pseudo stenosis).
Selon Monin, la fréquence des “pseudosténoses aortiques” est
plutôt basse en pratique clinique (10) ; cependant, dans la série
de Carabello, celle-ci atteint plus de 25 % des cas (8). L’hypo-
thèse est que, après dobutamine, la surface calculée par équation
de continuité augmente de plus de 0,3 cm
2
et dépasse la valeur
seuil de 1 cm
2
,alors que le gradient transaortique reste stable. Ce
phénomène peut s’expliquer par plusieurs mécanismes (9) :
–variation du coefficient de contraction en cas de bas débit abou-
tissant à une diminution du calcul de la surface aortique fonc-
tionnelle, alors même que la surface anatomique reste inchangée ;
–variation réelle de la surface anatomique ;
–variation du profil des vélocités du flux à travers l’orifice aor-
tique : passant d’un flux plat à un flux parabolique avec diminu-
tion des vélocités sur les bords de la vena contracta, là où les
forces de viscosité sont les plus importantes. Ainsi, le calcul de
la surface aortique utilisant la vélocité maximale du profil en dop-
pler continu surestimera les vélocités à travers l’orifice aortique
et sous-estimera donc la surface aortique en cas de bas débit car-
diaque.
Monin (10) a pu distinguer deux groupes à pronostic différent en
cas de dysfonction VG et de RAC serré : le premier avec réserve
contractile (augmentation du VES > 20 %) et bon pronostic per-
mettant une chirurgie, et le deuxième avec absence de réserve
contractile contre-indiquant la chirurgie.
Ainsi, dans le groupe avec réserve contractile, la mortalité opé-
ratoire est de 5 %, contre 32 % en cas d’absence de réserve
contractile. Les facteurs prédictifs de mortalité à long terme sont
l’absence de réserve contractile et un gradient moyen de base
inférieur à 20 mmHg.
La Lettre du Cardiologue - n° 382 - février 2005
21
MISE AU POINT
Vmax < 3,0 m/s
3,0-4,0 m/s
> 4,0 m/s
1,0
0,8
0,6
0,4
0,2
0,0 012 24 36 48 60
Durée depuis l'inclusion (mois)
Survie libre d'événement
(Otto, Circulation 1997)
.
Figure 1. Graphe montrant l’intérêt de la valeur pronostique de la vélo-
cité maximale du profil doppler continu transaortique.
•Diamètre sous-aortique calculé à l’état de base et considéré comme
constant
•À l’état de base et pour chaque palier, calculs :
–intégrale temps-vitesse sous-aortique (ITV) [voie apicale]
–gradients transvalvulaires et surface aortique par équation
de continuité
–calcul fraction d’éjection par Simpson biplan si recueil des
images de qualité suffisante
•Dobutamine débutée à 5 γ/kg/mn ; palier de 2,5 γ/kg/mn toutes les 5 mn
•Critères d’arrêt : fréquence cardiaque augmentant de plus de 10 bat-
tements par cycle, ce qui correspond au seuil d’inotropisme positif
sans risque d’ischémie myocardique associée
Encadré. Méthode de réalisation de l’écho-dobutamine de stress en
cas de rétrécissement aortique serré et de dysfonction VG.

En conclusion, la réalisation d’un écho-doppler de stress à la
recherche d’une réserve contractile est recommandée systémati-
quement en préopératoire d’un RAC serré associé à une dys-
fonction VG ; si l’on retrouve une réserve contractile significa-
tive, la chirurgie est de meilleur pronostic.
RÉTRÉCISSEMENT MITRAL (RM) ET STRESS
Il existe plusieurs techniques pour calculer la surface mitrale en
écho-doppler cardiaque (figure 2).
Ce calcul peut se faire :
–par le temps de demi-décroissance du gradient de pression
(PHT) avec l’équation de Hatle : surface mitrale = 220/PHT
(figure 2a) ;
–par planimétrie en petit axe, en réalisant le contourage au niveau
où la distance séparant les deux feuillets mitraux est égale à celle
retrouvée en grand axe (figure 2b) ;
–par la proximal isovelocity area (PISA), en calculant la surface
au niveau de la vena contracta (figure 2c) ;
–par l’équation de continuité (figure 2d) ;
–par analyse du flux couleur de remplissage sur deux plans per-
pendiculaires (4 cavités et 2 cavités) et calcul de la surface par
la formule de l’ellipsoïde (figure 2e).
Fort de ces différentes méthodes de calcul, on peut déterminer le
caractère serré du rétrécissement mitral et analyser le degré de
remaniement de l’appareil mitral par le score de Wilkins ou de
Abascal.
L’hémodynamique à l’effort en cas de sténose mitrale a été étu-
diée par Dahan et al. (12). Sur un groupe de 27 patients, l’aug-
mentation de la surface mitrale à l’effort est corrélée à la surface
mitrale de repos et à son degré de calcification. À un stade pré-
coce, la valve garde un certain degré d’élasticité et augmente sa
surface à l’effort, permettant une bonne adaptation du patient.
Après un certain temps d’évolution de la valvulopathie, avec cal-
cification des feuillets plus étendue, la surface n’augmente plus
à l’effort et le patient devient symptomatique.
L’étude hémodynamique de stress dans le rétrécissement mitral
se fait préférentiellement par écho-doppler d’effort, et avec cal-
cul de la surface mitrale par équation de continuité (13).
En cas de RM modéré (> 1,5 cm
2
) avec patients très symptomatiques,
une échocardiographie d’effort doit être réalisée : si celle-ci retrouve
un gradient multiplié par 2, un gradient supérieur à 15 mmHg ou une
PAPS supérieure à 60 mmHg, la commissurotomie est indiquée, car
elle permet une nette amélioration de la dyspnée et des symptômes.
Un autre cas de figure est à connaître : patients symptomatiques
avec RM non serré au calcul de la surface mitrale par la formule
de Hatle et hypertension artérielle pulmonaire (HTAP) de repos
s’aggravant à l’effort. En fait, le calcul par la formule de Hatle
est faussé par la diminution du temps de décélération de l’onde E
secondaire à la baisse de la compliance mitrale.
Les patients à faible compliance AV présentent une forte aug-
mentation de la PAPS à l’effort et une sévérité de l’obstruction
mitrale sous-estimée par une PHT courte (figure 3). Le calcul de
la surface mitrale par équation de continuité rectifie cette sous-
estimation en retrouvant une surface mitrale le plus souvent ser-
rée. Ces patients sont donc susceptibles de bénéficier d’une com-
missurotomie mitrale quand celle-ci est réalisable (14).
En conclusion, l’indication de l’écho-doppler d’effort en cas de
RM peut être résumée ainsi :
•Chez les patients asymptomatiques avec surface mitrale infé-
rieure à 1,5 cm
2
et PAPS de repos inférieure à 50 mmHg et qui
ont une valve possiblement réparable par commissurotomie per-
cutanée : une mauvaise tolérance à l’effort lors de l’échocardio-
graphie de stress et une PAPS > 60 mmHg nécessitent la réali-
sation d’une commissurotomie.
•Chez les patients symptomatiques, l’échocardiographie d’ef-
fort est réalisée en cas de sténose modérée > 1,5 cm
2
.L’appari-
tion à l’effort d’une PAPS > 60 mmHg et d’un gradient auriculo-
ventriculaire > 15 mmHg doit, si la valve s’y prête, pousser à la
réalisation d’une commissurotomie mitrale percutanée. .../...
La Lettre du Cardiologue - n° 382 - février 2005
22
MISE AU POINT
Compliance auriculo-ventriculaire (ml/mmHg) =
1270 x SVM/pente de décélération de l’onde E mitrale,
où SVM = surface de la valve mitrale calculée par équation
de continuité
Figure 2. Méthodes de calcul de la surface mitrale.
Figure 3. Exemple d’un patient avec surface mitrale par PHT à 1,7 cm
2
,
mais avec gradient moyen à 12 mmHg et PAPS de repos à 64 mmHg attei-
gnant 96 mmHg à l’effort. En fait, ce patient présente un RM serré à
0,7 cm
2
,calculé par l’équation de continuité au repos. La diminution de la
PHT s’explique par la diminution de la compliance mitrale (2 ml/mmHg).
a
de
b
c

.../...
•Enfin, en cas de discordance entre clinique et échographie,
on réalise l’échographie d’effort afin de dépister une PAPS
>60mmHg, un gradient > 15 mmHg et une désaturation à l’ef-
fort, qui seraient en faveur d’une correction percutanée du RM.
INSUFFISANCE AORTIQUE (IA) ET STRESS
L’histoire naturelle de l’IA sévère est connue. En cas d’IA asymp-
tomatique avec FEVG > 45 %, la mortalité est de 0,5 % par an ;
chaque année, 4 à 6 % des patients développeront une insuffi-
sance cardiaque gauche ou auront un remplacement valvulaire
aortique, avec un risque opératoire de 2 à 5 % (2).
En cas d’IA sévère asymptomatique, la chirurgie est indiquée si le
diamètre télésystolique (DTSVG) est supérieur à 55 mm et la FEVG
inférieure à 55 %. Dans l’étude de Borer (15), sur 104 patients
asymptomatiques ou paucisymptomatiques explorés en échocar-
diographie d’effort, c’est le delta FEVG (repos-effort) indexé au
stress pariétal qui est le mieux corrélé au développement des symp-
tômes et des décès. Dans ce type d’évaluation, la scintigraphie au
technétium permet une évaluation aussi performante de la FE.
Selon d’autres auteurs, la présence d’une réserve contractile en
préopératoire (définie par une augmentation d’au moins une
déviation standard de la FE calculée en Simpson) chez des
patients pauci- ou asymptomatiques permet de prédire l’amélio-
ration de la FE en postopératoire (16).
Enfin, rappelons ici les recommandations ACC/AHA de la pra-
tique du stress en cas d’IA chronique sévère :
•En cas d’IA dont l’association aux symptômes est équivoque,
l’ECG d’effort est indiqué afin de démasquer une fatigue pré-
coce ou une dyspnée en faveur d’une IA symptomatique.
•En cas d’IA asymptomatique et de fonction VG conservée avec
DTS entre 50 et 55 mm et DTDVG entre 65 et 70 mm, l’écho-
dobutamine est indiquée, à la recherche d’une dysfonction VG au
pic du stress, qui serait en faveur d’une indication chirurgicale (2).
Mais, comme on le remarque, la place de l’échocardiographie de
stress dans l’évaluation de l’IA n’est pas véritablement codifiée
et nécessite encore la réalisation d’études avec suivi à long terme.
INSUFFISANCE MITRALE (IM) ET STRESS
Peu d’études ont été effectuées sur ce sujet, qui reste encore confi-
dentiel.
Stoddard et al. ont réalisé des échocardiographies d’effort sur un
groupe de 94 patients porteurs d’un prolapsus valvulaire mitral
sans fuite. Dans un tiers des cas, une IM significative apparais-
sait à l’effort. Après un suivi moyen de 38 mois, la présence de
l’IM à l’effort était corrélée à la survenue de syncopes, d’une
insuffisance cardiaque et d’une progression vers une IM chirur-
gicale (17). Cette étude incite, en cas de prolapsus valvulaire
symptomatique, à réaliser une échocardiographie d’effort afin de
dépister la survenue d’une IM significative.
En préopératoire d’une plastie mitrale, Leung et al. démontrent
que le meilleur facteur prédictif de dysfonction VG postopéra-
toire est l’absence d’élévation de la FEVG en préopératoire, lors
de l’échocardiographie d’effort (18).
Dans le cas des cardiopathies ischémiques, on peut distinguer
deux situations :
•L’apparition d’une IM, lors d’une écho-dobutamine réalisée en
routine pour évaluation d’une ischémie myocardique, n’aggrave
pas le pronostic du patient (19).
•Par contre, en cas d’IM ischémique avérée détectée au repos,
une augmentation de la fuite en échocardiographie de stress est
un facteur de mauvais pronostic à long terme.
En effet, l’étude réalisée par Lancellotti et al. analyse les résul-
tats de l’échographie d’effort de 98 patients avec cardiopathies
ischémiques, dysfonction VG et fuite mitrale au minimum modé-
rée. L’IM est évaluée par la méthode de la PISA à l’état basal et
au pic du stress (figure 4). Après un suivi moyen de 19±8mois,
l’analyse par régression multivariée de Cox retrouve comme fac-
teurs indépendants de mortalité cardiovasculaire : une augmen-
tation ≥13 mm
2
à l’échocardiographie d’effort de l’orifice régur-
gitant effectif (ORE), un ORE de base > 20 mm
2
,et un temps de
décélération mitrale diminué. Aucun des 14 patients présentant
une diminution de l’ORE à l’effort n’est décédé de causes car-
diovasculaires durant la période de suivi (20). La présence d’une
augmentation significative de l’IM ischémique lors de l’écho
d’effort permet de déterminer un sous-groupe de patients à haut
risque cardiovasculaire qui pourraient être plus susceptibles de
bénéficier d’une plastie mitrale.
Enfin, une étude sur des patients porteurs d’une cardiomyopa-
thie dilatée démontre une bonne corrélation entre, d’une part,
l’augmentation à l’effort du volume régurgité mitral et, d’autre
part, la diminution du volume d’éjection systolique et l’élévation
des pressions pulmonaires. Les auteurs concluent que la majo-
ration de l’IM observée lors de l’échocardiographie de stress
pourrait expliquer l’inadaptation à l’effort de ces patients et serait
en faveur d’une correction chirurgicale de cette fuite (16).
D’autres études à effectifs plus élevés sont nécessaires afin de
préciser la place exacte de l’échographie de stress dans la prise
en charge de la fuite mitrale.
CONCLUSION
L’étude hémodynamique doppler de stress permet d’évaluer de
manière objective le retentissement hémodynamique et la tolé-
rance fonctionnelle des patients porteurs de valvulopathies
La Lettre du Cardiologue - n° 382 - février 2005
23
MISE AU POINT
Figure 4. Exemple de calcul de l’IM par la PISA au repos et à l’effort,
avec augmentation du rayon de la PISA à l’effort.

MISE AU POINT
sévères asymptomatiques. En cas de valvulopathie sévère et de
dysfonction VG, la réserve contractile évaluée par dobutamine
permet d’apprécier le pronostic opératoire et la survie à moyen
terme. Les évaluations les mieux validées sont l’écho-dobuta-
mine du rétrécissement aortique serré avec dysfonction VG et
l’échographie d’effort du rétrécissement mitral asymptomatique.
L’évaluation de l’intérêt de ces examens dans les autres valvu-
lopathies est en cours d’étude. ■
Bibliographie
1. Gorlin R, Gorlin SG. Hydraulic formula for calculation of the area of the ste-
notic mitral valve, other cardiac valves and central circulatory shunts. Am Heart J
1951;41:1-29.
2. Bonow RO, Carabello BA, de Leon AC Jr et al. ACC/AHA guidelines for the
management of patients with valvular heart disease: a report of the American
College of Cardiology/American Heart Association Task Force on Practice
Guidelines. J Am Coll Cardiol 1998;32:1486-588.
3. Garcia D, Dumesnil JG, Durand LG, Kadem L, Pibarot P. Discrepancies bet-
ween catheter and Doppler estimates of valve effective orifice area can be pre-
dicted from the pressure recovery phenomenon: practical implications with
regards to quantification of aortic stenosis severity. J Am Coll Cardiol 2003;
41:435-42.
4. Bermejo J, Oderman R, Feijjo J et al. Clinical efficacy of Doppler-echocardio-
graphic indices of aortic valve stenosis: a comparative test-based analysis of out-
come. Am J Cardiol 2003;41:142-51.
5. Otto CM, Burwash IG, Legget ME et al. Prospective study of asymptomatic
valvular aortic stenosis. Clinical, echocardiographic, and exercise predictors of
outcome. Am J Cardiol 2003;41:142-51.
6. Carabello BA. Evaluation and management of patients with aortic stenosis.
Circulation 2002;105(15):1746-50.
7. Connolly HM, Oh JK, Schaff HV et al. Severe aortic stenosis with low trans-
valvular gradient and severe left ventricular dysfunction. Circulation 2000;101:
1940-6.
8. Carabello BA. Evaluation and management of patients with aortic stenosis.
Circulation 2002;105(15):1746-50.
9. Schwammenthal E, Vered Z, Moshkowitz Y et al. Dobutamine echocardiogra-
phy in patients with aortic stenosis and left ventricular dysfunction: predicting
outcome as a function of management strategy. Chest 2001;119:1766-77.
10. Monin JL, Quere JP, Monchi M et al. Low-gradient aortic stenosis: opera-
tive risk stratification and predictors for long-term outcome: a multicenter study
using dobutamine stress hemodynamics. Circulation 2003;108(3):319-24.
11. Defilippi CR, Willet DL, Brickner ME et al. Usefulness of dobutamine echo-
cardiography in distinguishing severe from non severe valvular aortic stenosis in
patients with depressed left ventricular function and low transvalvular gradients.
Am J Cardiol 1995;75:191-4.
12. Dahan M, Paillole C, Martin D et al. Determinants of stroke volume res-
ponse to exercise in patients with mitral stenosis: a Doppler echocardiographic
study. Am J Cardiol 1993;21:384-9.
13. Braveman AC, Thomas JD, Lee RT et al. Doppler echocardiographic esti-
mation of mitral valve area during changing hemodynamic condition. Am J
Cardiol 1991;68:1485-90.
14. Schwammenthal E,Vered Z,Agranat O et al. Impact of atrioventricular com-
pliance on pulmonary artery pressure in mitral stenosis: an exercise echocardio-
graphic study. Circulation 2000;102:2378-84.
15. Borer JS, Hochreiter C, Herrold EM et al. Prediction of indication of valve
replacement among asymptomatic or minimally symptomatic patients with chro-
nic aortic regurgitation and normal left ventricular performance. Circulation
1998;97:525-34.
16. Wahi S, Haluska B, Pasquet A et al. Exercise echocardiography predicts
developpement of left ventricular dysfunction in medically and surgically treated
patients with asymptomatic severe aortic regurgitation. Heart 2000;84:606-14.
17. Stoddard MF, Prince CR, Dillon S et al. Exercise-induced mitral regurgita-
tion is a predictor of morbid events in subjects with mitral valve prolapse. J Am
Col Cardiol 1995;25:693-9.
18. Leung DY, Griffin BP, Stewart WJ et al. Left ventricular function after valve
repair for chronic mitral regurgitation: predictive value of preoperative assess-
ment of contractile reserve by exercise echocardiography. J Am Coll Cardiol
1996;28:1198-205.
19. Heinle HK, Tice FD, Kisslo JD et al. Effect of dobutamine stress echocar-
diography on mitral regurgitation. J Am Coll Cardiol 1995;25:122-7.
20. Lancellotti P, Troisfontaines P, Toussaint AC et al. Prognostic importance of
exercise-induced changes in mitral regurgitation in patients with chronic ische-
mic left ventricular dysfunction. Circulation 2003;108(14):1713-7.
1
/
5
100%