T°SI 2015/ 2016 CONTEXTE: → En chimie organique, l`opérateur

T°SI
CHIMIE
TROISIEME PARTIE : « TRANSFORMATIONS CHIMIQUES DE LA MATIERE »
2015 / 2016
TP SUR LE CHAPITRE 9 « LE PARAMETRE TEMPS DANS LES TRANSFORMATIONS CHIMIQUES : CINETIQUE ET CATALYSE »
COMPETENCE EXIGIBLE OFFICIELLE
COMPETENCES DE LA DEMARCHE SCIENTIFIQUE MISES EN JEU AVEC LES PRINCIPALES CAPACITES ET ATTITUDES ASSOCIEES
Mettre en œuvre une démarche
expérimentale pour suivre dans le temps une
synthèse organique par CCM et en estimer la
durée.
APP
Mobiliser ses connaissances.
ANA
Exploiter ses connaissances et des informations extraites.
Proposer un protocole expérimental permettant de répondre à une problématique.
REA
Mettre en œuvre un protocole imaginé.
VAL
Interpréter des résultats expérimentaux.
COM
Rédiger à l’écrit un compte-rendu.
AUT
Travailler efficacement seul ou en équipe avec discernement et responsabilité.
Prendre des initiatives.
Mobiliser sa curiosité et /ou sa créativité.
SUIVI CINETIQUE QUALITATIF D’UNE REACTION LENTE PAR CHROMATOGRAPHIE SUR COUCHE MINCE (CCM)
CONTEXTE :
En chimie organique, l’opérateur est confronté à des réactions qui ne sont pas toujours très rapides. Il est alors amené à
s’interroger sur la durée nécessaire pour que la transformation soit considérée comme terminée. Pour cela, il peut étudier la
bibliographie scientifique ou alors utiliser une technique du suivi cinétique. Cette technique ne doit pas consommer beaucoup de
produit et être rapide à mettre en œuvre : la chromatographie sur couche mince (CCM) est particulièrement bien adaptée.
L’huile essentielle de jasmin, très couramment utilisée en parfumerie, est obtenue par extraction à
l’aide de solvants volatils des fleurs de jasmin. Cette huile essentielle contient un ester : l’éthanoate de
benzyle. L’extraction et la séparation étant des opérations coûteuses et complexes, leur synthèse est une
alternative utilisée en parfumerie et dans l’agroalimentaire. On se propose de synthétiser l’éthanoate de
benzyle et d’effectuer un suivi temporel de la réaction par chromatographie sur couche mince (CCM) pour
évaluer l’instant à partir duquel la transformation est terminée.
DOCUMENTS MIS A DISPOSITION :
DOCUMENT N°4 : SCHEMA ANNOTE D’UN MONTAGE CHAUFFAGE A
REFLUX
DOCUMENT N°1 : PROTOCOLE DE SYNTHESE DE L’ETHANOATE DE
BENZYLE
Introduire dans un ballon bicol bien sec 15 mL de
cyclohexane, 10 mL d’alcool benzylique et 25 mL
d’anhydride éthanoïque.
Ajouter quelques grains de pierre ponce.
Chauffer à reflux.
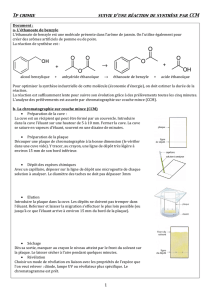
DOCUMENT N°2 : EQUATION DE LA REACTION DE LA SYNTHESE DE
L’ETHANOATE DE BENZYLE
C4H6O3 + C7H8O C9H10O2 + C2H4O2
DOCUMENT N°3 : DEUX GROUPES CARACTERISTIQUES UTILES
ECRITS EN FORMULES TOPOLOGIQUES
Groupe anhydride d’acide :
Groupe benzyle :

DOCUMENT N°5 : DONNEES CONCERNANT LES ESPECES CHIMIQUES MISES EN JEU
Anhydride éthanoïque
C4H6O3
M = 102 g.mol–1
d = 1,08
Teb = 139°C
Soluble dans l’eau et dans le
cyclohexane
Alcool benzylique
C7H8O
M = 108 g.mol–1
d = 1,04
Teb = 205°C
Soluble dans le cyclohexane
Ethanoate de benzyle
C9H10O2
M = 150 g.mol–1
d = 1,1
Teb = 212°C
Soluble dans le cyclohexane
Cyclohexane
C6H12
M = 84 g.mol–1
d = 0,78
Teb = 81°C
Insoluble dans l’eau
Acide éthanoïque
C2H4O2
M = 60 g.mol–1
d = 1,08
Teb = 117,9°C
Soluble dans l’eau
DOCUMENT N°6 : GENERALITES SUR LA CHROMATOGRAPHIE SUR COUCHE MINCE (CCM)
La chromatographie est une technique de SÉPARATION et
d’IDENTIFICATION d’espèces chimiques issues d’un mélange. Elle est basée
sur les différences d’affinités que possèdent les espèces chimiques du
mélange pour les deux phases : la phase stationnaire ou plaque à CCM ;
la phase mobile ou éluant.
La chromatographie sur couche mince est une chromatographie
d’ADSORPTION basée sur la formation de liaisons momentanées entre les
espèces chimiques des dépôts et la phase stationnaire. La façon dont
chaque espèce chimique migre dépend de son adsorption sur la phase
stationnaire et de sa solubilité dans la phase mobile, cette dernière montant
dans la phase stationnaire par capillarité. La séparation est alors basée sur la
différence de vitesse de déplacement des espèces chimiques sur la phase
stationnaire.
Chaque constituant d’un mélange mis en évidence par une tache est caractérisé, pour une phase stationnaire et un éluant
donné, par un rapport frontal noté Rf et défini par :
H
h
éluantl' par parcourue distance
tconstituan le par parcourue distance
Rf
Dans le cas d’espèces incolores présentes dans le mélange, la révélation consiste à faire apparaitre les tâches correspondant à
ces espèces. Deux types de méthode peuvent être utilisés :
la révélation aux UV ;
les méthodes chimiques : solution de permanganate de potassium ou vapeurs de diiode.

TRAVAIL A EFFECTUER :
Q1) S’APPROPRIER ET COMMUNIQUER.
Q1a) Ecrire avec les formules semi-développées l’équation de la synthèse de l’éthanoate de benzyle. Entourer et nommer
les groupes caractéristiques.
Q1b) La synthèse de l’éthanoate de benzyle est-elle une réaction de substitution ou d’addition ou d’élimination ? Justifier.
Q1c) Le cyclohexane utilisé dans le protocole expérimental de cette synthèse joue le rôle de solvant. Justifier ce rôle.
Q1d) Dans un montage chauffage à reflux, quel est le rôle du réfrigérant ? Du chauffage ? Des grains de pierre ponce ?
Q1e) Annoter le schéma du document n°6 en utilisant les mots suivants : éluant / plaque à CCM / dépôt / constituants du
mélange / ligne de front de l’éluant / cuve à élution / couvercle / ligne de dépôt / phase stationnaire / phase mobile.
APPEL N°1
APPELER VOTRE PROFESSEUR POUR LUI PRESENTER VOTRE APPROPRIATION OU EN CAS DE DIFFICULTE
Q2) ANALYSER, REALISER ET COMMUNIQUER.
Q2a) L’alcool benzylique est le réactif limitant. Indiquer les espèces chimiques présentes dans le ballon bicol :
Au cours de la transformation d’une part ;
Dans l’état final d’autre part.
Q2b) Comment peut-on savoir si la réaction est terminée ?
Q2c) Proposer alors un protocole expérimental pour suivre dans le temps la synthèse de l’éthanoate de benzyle et estimer
ainsi la durée de cette synthèse.
APPEL N°2
APPELER VOTRE PROFESSEUR POUR LUI PRESENTER VOTRE ANALYSE OU EN CAS DE DIFFICULTE
Q3) REALISER, VALIDER ET COMMUNIQUER.
Q3a) Réaliser la synthèse de l’éthanoate de benzyle.
Q3b) Estimer la durée en mettant en œuvre le protocole expérimental proposé en Q2c).
Q3c) On donne ci-dessous le mécanisme réactionnel de la synthèse de l’éthanoate de benzyle. Représenter en bleu les
flèches courbes qui traduisent la formation des liaisons covalentes et en rouge les flèches courbes qui traduisent la
rupture des liaisons covalentes dans chacune des étapes ci-dessus (R représente le groupe méthyle CH3 et
R’ représente le groupe benzyle C6H5–CH2).
APPEL N°3
APPELER VOTRE PROFESSEUR POUR LUI PRESENTER VOTRE REALISATION ET VOTRE VALIDATION
OU EN CAS DE DIFFICULTE
*****
1
/
3
100%