Lire l`article complet

Le Courrier des addictions (11) – n° 1 – janvier-février-mars 2009
31
F
i
c
h
e
F
i
c
h
e
F
i
c
h
e
F
i
c
h
e
F
i
c
h
e
F
i
c
h
e
Fiche
pratique
N° 30
Sous la responsabilité de leurs auteurs
Le syndrome de sevrage est défini par l’ensemble des manifestations cliniques survenant dans les suites immédiates (en
général 72 heures) ou différées, jusqu’à dix jours après l’arrêt brutal de la consommation d’alcool. Bien que nécessitant une
médicalisation, la prise en charge doit rester dans le cadre d’un travail d’équipe multidisciplinaire.
Celle-ci peut être somatique : liée à la décompensation aiguë de l’une des complications somatiques (cirrhose, pancréatite
aiguë…) ou lors d’une pathologie traumatique.
Elle peut être psychiatrique, en particulier l’idéation suicidaire gravissime, ou une situation mettant en jeu la vie du
patient ou de l’un de ses proches. L’hospitalisation peut alors se faire dans le cadre d’une hospitalisation à la demande d’un
tiers.
Sociale : dans de rares cas où le pronostic vital peut être mis en jeu par des conditions de précarité extrême. Il peut s’agir,
enfin, d’un sevrage carcéral.
Il s’intègre dans la trajectoire de vie du patient. Du récit factuel, avec sa composante de déni et de culpabilité, émergent
peu à peu des émotions et des affects. L’idée d’un travail de deuil de l’alcool commence à poindre. La motivation à l’absti-
nence s’exprime avec plus d’authenticité avec l’élaboration autour du concept d’une meilleure qualité de vie en cas d’absti-
nence, et d’autres arguments que ceux exclusivement d’un meilleur bien-être de l’entourage. Enfin, passer de la survie – où
seule l’immédiateté fait loi – à la vie – où les expériences du passé et les aspirations à un devenir sont prises en compte – est
une thématique fréquemment reprise par les patients lorsqu’ils se sentent prêts à programmer un sevrage.
Il permet d’effectuer la démarche de soins, tout en maintenant le patient dans son environnement. Cette prise en charge
nécessite l’implication active de l’entourage.
Les contre-indications : l’alcoolodépendance sévère ou les polyaddictions, l’existence d’une ou plusieurs poly-
pathologies somatiques lourdes ou des troubles psychiatriques aigus, un antécédent de complication médicale du
sevrage, un isolement extrême.
Il repose sur les éléments suivants :
L’information du patient. C’est le point crucial. Il faut rassurer et surtout sécuriser la période de sevrage. Celle-ci se
déroule sous la responsabilité d’un médecin appartenant à une structure spécialisée, en synergie avec le reste de l’équipe
du centre, si possible en parallèle avec le médecin référent. L’explication donnée au patient, et à une personne qu’il aura
désignée, doit être claire, pratique et personnalisée. Cette explication concerne : les coordonnées téléphoniques du centre
avec les heures d’ouverture, ainsi que le numéro du service d’urgence de l’hôpital le plus proche ; les effets secondaires des
benzodiazépines ; l’impossibilité de conduire ; la nécessité d’un suivi régulier : quotidien durant les 4 premiers jours et en
fin de sevrage. Le patient bénéficie d’un arrêt de travail de 10 jours.
Les principaux éléments en sont :
L’hydratation. Les apports hydriques doivent être suffisants sans hyperhydratation (1,5-2 l/j).
La prescription de benzodiazépines. Elle permet de réduire l’incidence et la sévérité des complications du syndrome
de sevrage. Il est logique d’utiliser une molécule à demi-vie intermédiaire (10 h-40 h) par voie orale (diazépam, lorazépam,
alprazolam, bromazépam, clobazam). La prescription concerne des doses fixes réparties sur le nycthémère à dose pleine
durant 3 jours, par exemple diazépam 10 mg toutes les 6 heures, puis à des doses dégressives pour un arrêt en 10 jours
maximum. La prescription doit toujours être adaptée à la clinique.
À éviter : les carbamates doués d’une faible activité anticomitiale et d’un risque létal en cas d’intoxication volontaire et
dont le bénéfice n’est pas validé dans le cadre du sevrage en alcool. En cas de prescription antérieure, ils seront remplacés
par une benzodiazépine selon un schéma de chevauchement sur trois jours sous surveillance médicale. Les barbituriques
ont également une efficacité démontrée, mais exposent plus aux risques de dépression respiratoire. Les neuroleptiques
potentiellement épileptogènes ne doivent pas être utilisés en première intention.
Les vitamines. Bien que non remboursées, elles ne doivent pas être oubliées, surtout la thiamine (B1) 500 mg/j, la pyri-
doxine (B6) 500 mg/j et son coenzyme le nicotinamide (vitamine PP). La prescription de vitamine B6 doit être limitée dans
le temps en raison du risque de neuropathie en cas de surdosage.
Une consultation quotidienne. Elle est hautement souhaitable au début.
Il permet d’effectuer la démarche de soins dans un environnement médicalisé.
Les indications. Elles sont addictologiques : alcoolodépendance sévère ou polyaddictions, antécédents de complication
de sevrage (convulsion, delirium tremens), échecs de plusieurs sevrages ambulatoires ; somatiques : affections somatiques
lourdes isolées, associées, ou décompensées ; psychiatriques : syndrome dépressif, ou pathologie psychiatrique décompen-
sée. L’association de ces deux pathologies peut être responsable d’un diagnostic erroné ou d’un retard à une prise en charge
spécialisée. Il est nécessaire de reprendre la diachronie des troubles et rechercher l’existence de symptômes psychiatriques
précédant les consommations abusives d’alcool (syndrome dépressif, TS à répétition, conduite d’évitement, anxiété mas-
sive et invalidante…) ; socio-environnementales : demande pressante de l’entourage familial ou professionnel, entourage
non coopératif, désocialisation avancée. Dans ce cas, dans le cadre d’un projet social établi avant l’admission.
Les bénéfices du temps de l’hospitalisation. Il permet de reprendre la biographie du patient avec ses cassures et ses
ruptures, son histoire avec ses souvenirs agréables ou aversifs avec le produit alcool. En explorant l’avant, le pendant et
l’après, le sevrage devient un élément de repère dans sa vie. En se référant ainsi à un avant et un après sevrage, on espère
que le patient évalue, avec plus de clairvoyance, combien l’alcool n’avait pas que des répercussions somatiques, mais aussi
Le sevrage alcool
B. Badin de Montjoye*, P. Podevin**
Rappel
Le sevrage accidentel
ou dans l’urgence
Le sevrage programmé
En ambulatoire
Résidentiel

Le Courrier des addictions (11) – n° 1 – janvier-février-mars 2009
32
Fiche
pratique
N° 30
Sous la responsabilité de leurs auteurs
dans tous les champs de sa vie. L’hospitalisation permet aussi un examen clinique complet, un bilan
systématique (tableau I) et le dépistage des autres cancers associés à l’alcool (côlon, sein, œsophage)
chez des patients peu souvent peu concernés par les campagnes de dépistage. Enfin, l’obtention de
l’abstinence permet de réévaluer l’existence ou non de troubles psychiatriques. Les principaux élé-
ments du traitement médical en sont :
L’hydratation. Mêmes modalités que lors du sevrage ambulatoire, sans hyperhydratation ni per-
fusion systématique.
Les apports en magnésium et potassium. Nécessaires seulement en cas d’hypokaliémie, révélant
souvent une tubulopathie induite par l’alcool
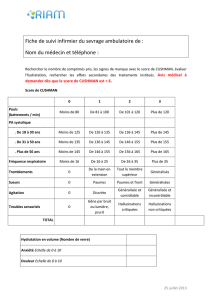
La prescription de benzodiazépines. Elle peut être systématique ou adaptée à un score validé
pour le syndrome de sevrage alcool. En France, le score de Cushman (tableau II) est le plus utilisé,
les Anglo-Saxons utilisant plutôt le CIWA. Le traitement est fondé sur l’administration d’une dose
initiale de benzodiazépines à demi-vie intermédiaire par voie orale de préférence en fonction du
score en adaptant cette dose sur un score refait toutes les 4 heures. Les équivalences sont estimées
comme suit : 10 mg diazépam = 30 mg oxazépam = 2 mg lorazépam = 1 mg alprazolam = 15 mg
chlorazépate. Les posologies sont donc adaptées à la clinique, maximale sur 3-4 jours puis à dose
dégressive sur 10 jours pour permettre un sevrage des benzodiazépines avant la sortie. En cas
d’insuffisance hépatocellulaire, les benzodiazépines à demi-vie courte seront préférées (lorazé-
pam, oxazépam). Les bêtabloquants et la clonidine diminuent les manifestations d’hyperactivité
adrénergique mais n’apportent pas de protection anticomitiale et faussent le score de Cushman.
Les vitamines. La prescription de vitamines B1 doit être systématique, surtout en cas
de perfusion glucosée. L’apport doit être entre 500 et 1 000 mg/j. Elle doit s’associer aux
vitamines B6 et PP.
La prise en charge des coaddictions
– Le tabac. Il concerne 80 à 90 % des patients. L’intérêt pour un sevrage combiné est de plus en
plus reconnu. La substitution nicotinique doit être proposée de façon systématique.
– Les opiacés. La surveillance clinique des benzodiazépines doit être plus importante chez les
patients sous traitement de substitution par buprénorphine haut dosage, en raison du risque de
dépression respiratoire. Par ailleurs, la posologie du traitement de substitution aux opiacés prescrit
antérieurement doit toujours être réévaluée sur les signes cliniques avant la sortie. Il est préférable
de faire le sevrage en opiacés dans un second temps.
– La cocaïne. La recherche d’une consommation de cocaïne doit être systématique en raison de
sa fréquence. L’alcool est souvent utilisé pour atténuer ou retarder la deuxième phase, celle de
l’effondrement psychique. L’alcool peut aussi être consommé lors des états d’hypervigilance. Il
n’existe pas de traitement spécifique du sevrage.
La prise en charge des complications du sevrage
– Le traitement du delirium tremens. Il fait appel aux neuroleptiques en association systématique avec les benzodiazépines par voie
veineuse, en dose de charge (5 à 10 mg diazépam toutes les 5 minutes jusqu’à la sédation puis 5 mg à la demande) ou 10 mg/h en
continu. L’administration de midazolam IV ( 2-30 mg/h) est également possible. Ces traitements doivent être administrés en USI,
parallèlement à une rééquilibration hydroélectrolytique. La clonidine peut être utile dans les poussées hypertensives.
– Le traitement des crises généralisées. Il est avant tout le traitement d’une cause associée (hypoglycémie, hyponatrémie, trau-
matisme crânien, infection cérébro-méningée, AVC, intoxication médicamenteuse). Dans 90 % des cas, les convulsions survien-
nent dans les 48 premières heures.
Les modalités de sortie de l’hôpital. Plus encore que pour les autres patients, l’ordonnance de sortie revêt une importance
cruciale, afin de limiter les risques de mésusage, en particulier l’abus de benzodiazépines. Le patient doit avoir un rendez-vous
auprès d’un centre spécialisé ou revoir son référent médical dans un délai rapide avec un compte rendu provisoire de sortie
précisant la durée de la prescription.
Le soutien socio-médico-psychologique. C’est le fondement même de la prise en charge de toute personne en difficulté avec
l’alcool en association avec les groupes d’anciens buveurs.
Le traitement pharmacologique. Il repose actuellement sur les molécules jouant sur l’appétence à l’alcool. L’acamprosate
(Aotal®) est un stimulant de la transmission gabaergique, dénué d’effet hypnotique, anxiolytique ou myorelaxant. L’acamprosate
augmente le nombre de patients abstinents et le nombre de jours d’abstinence. Les principaux effets secondaires sont les diarrhées,
céphalées, prurit. La posologie est de 4 cp/j si < 60 kg, 6cp/j au-delà. Dans l’AMM, la prescription est limitée à un an. La naltrexone
(Révia®) est un inhibiteur des récepteurs opioides µ. Il diminue l’effet euphorisant. Les effets secondaires sont les nausées,
vomissements, céphalées, anxiété. La posologie est de 50 mg/j par pallier sur une semaine. La naltrexone est contre-indiquée
en cas de dépendance aux opiacés ou d’hypersensibilité. Une hépatotoxicité dose-dépendante est possible. L’AMM limite la
prescription à trois mois. L’utilité des antidépresseurs doit être évaluée après 4 semaines d’abstinence.
Références bibliographiques
1. Cushman PJ, Forbes R, Lerner W, Stewart M. Alcohol withdrawl syndromes: clinical management with lofexidine. Alcohol Clin
Exp Res 1985;9;103-8.
2. Sullivan J, Sykora K, Schneiderman J, Naranjo CA, Sellers E. Assessment of alcohol withdrawl: the revised clinical institute
withdrawl for alcohol scale (CIWA-Ar)? Br J Addiction 1989;84:1353-7.
3. Objectifs, indications et modalités du sevrage du patient alcoolodépendant. Gastroenterol Clin Biol 1999;23:865-73.
4. Mc Keon A, Frye MA, Delanty. The alcohol withdrawl syndrome. J Neurol Neurosurg Psychiatry 2008;79:854-62.
5. Anton RF. Naltrexone for the management of alcohol dependence. N Engl J Med 2008;359:715-21.
6. Kranzler HR, Gage A. Acamprosate, efficacy in alcohol-dependent patients: summary of results from three pivotal trials. Am J
Addict 2008;17;70-6.
Le maintien du sevrage
Tableau I.
Bilan somatique.
Examens biologiques NFS plaquettes
ASAT, ALAT, PAlc, gGt
Albumine, TP
Ionogramme, créatininémie
Sérologies HIV, HBV, HCV
Examens paracliniques ECG
Radiographie de thorax
Radiographie sinus, panoramique
dentaire
Consultations ORL, gynécologique, cardiologique
(douleur thoracique, allongement
PR, QT)
En fonction de la clinique TDM cérébral (troubles neuro- ou
neuropsychologiques, notion de
chute)
Échographie, TDM abdominal
(cirrhose, pancréatite)
Tableau II.
Score de Cushman.
0 1 2 3
Pouls < 80 80-100 100-120 >120
PA systolique < 135 135-145 145-155 >155
Fr respiratoire < 16 16-25 26-35 >35
Tremblements 0 main Membre sup généralisés
Sueurs 0 paumes Paumes/front généralisés
Agitation 0 discrète Généralisées
contrôlables
Générali-
sées incon-
trôlables
Troubles
sensoriels
0 Gène/
bruit/
lumière
Hallucinations
critiquées
Hallucina-
tions non
critiquées
< 7 sevrage contrôlé ; 7-14 sevrage modéré ; ≥ 15 sevrage sévère.
1
/
2
100%