Traitement chirurgical du cancer de l estomac

La Lettre de L’Hépato-Gastroentérologue - n° 1 - février 199820
D
O S S I E R T H É M A T I Q U E
e traitement du cancer de l’estomac repose essentiel-
lement sur la chirurgie. En effet, actuellement ni la
radiothérapie, ni la chimiothérapie n’ont fait la preuve
de leur efficacité.
FACTEURS PRONOSTIQUES
Les deux facteurs pronostiques les plus importants sont le type
de résection chirurgicale et l’existence d’un envahissement gan-
glionnaire (1). On distingue trois types de résections (UICC
1992). La résection R
0
(no residual tumor) correspond à une
résection curative à la fois macroscopique et microscopique. La
résection R
1
(microscopic residual tumor) correspond à une
résection macroscopiquement curative mais microscopique-
ment incomplète, en particulier lorsque les recoupes duodénales
ou œsophagiennes sont envahies. Enfin, la résection R
2
(macro-
scopic residual tumor) est une résection macroscopiquement
incomplète.
Une étude multifactorielle présentée par le German Gastric
Carcinoma Study Group concernant 1 654 cancers de l’estomac
réséqués, a montré que dans le groupe qui a eu une résection de
type R
0
, le facteur pronostique le plus important est l’existence
d’un envahissement ganglionnaire. La survie à 5 ans est de 60 à
80 % en l’absence d’envahissement ganglionnaire et n’est plus
que de 20 à 30 % en présence d’un envahissement ganglionnai-
re. Un deuxième facteur pronostique est prépondérant, c’est le
pourcentage de ganglions envahis par rapport au nombre de
ganglions examinés. Un pourcentage de ganglions envahis
supérieur à 20 % est un élément péjoratif. C’est dire l’impor-
tance des curages ganglionnaires dans la technique d’exérèse
des cancers de l’estomac.
QUEL CURAGE GANGLIONNAIRE FAUT-IL EFFECTUER
EN CAS DE CANCER GASTRIQUE ?
Depuis plusieurs années, un débat chirurgical est ouvert concer-
nant les lymphadénectomies dans le cancer de l’estomac. Les
techniques et l’étendue des curages effectués ainsi que la défi-
nition des curages ne sont pas univoques selon les pays, expli-
quant les résultats très différents obtenus en termes de survie
pour un même type de tumeur (tableau I).
Ceci est lié à plusieurs raisons :
•la disposition anatomique des réseaux de drainage lympha-
tique de l’estomac qui comportent plusieurs pédicules princi-
■
Le traitement du cancer de l’estomac repose essentielle-
ment sur la chirurgie.
■
Les facteurs pronostiques les plus importants sont le type
de résection chirurgicale et l’existence d’un envahissement
ganglionnaire.
■
Les cancers médio-gastriques ou cardio-tubérositaires
nécessitent une gastrectomie totale. En revanche, une gas-
trectomie subtotale est le plus souvent suffisante en cas de
cancer antro-pylorique.
■
La splénectomie n’est indiquée qu’en cas de cancer cardio-
tubérositaire localisé sur la grande courbure avec envahisse-
ment de la séreuse et atteinte des ganglions du hile splénique.
■
La pancréatectomie reste une intervention de nécessité
réservée aux envahissements directs du pancréas.
■
La question du curage ganglionnaire à effectuer est encore
débattue : les curages extensifs améliorent globalement la
survie, mais au prix d’une augmentation de la morbidité et de
la mortalité postopératoire essentiellement liée à la splénec-
tomie et à la pancréatectomie.
P O I N T S F O R T S
P O I N T S F O R T S
L
* Chef du Département de chirurgie générale carcinologique,
Institut Gustave-Roussy, Villejuif.
Stades
I
II
IIIa
IIIb
IV
86,6
77
64
37
6
84
50
34
7
3,5
67
38
17
3
2
Japon Allemagne Etats-Unis
Tableau I. K. Estomac : survie à 5 ans (%).
D’après Maruyama, Tokyo, 1991.
Traitement chirurgical du cancer de l’estomac
•P. Lasser*

La Lettre de L’Hépato-Gastroentérologue - n° 1 - février 1998 21
paux (artère coronaire stomachique, artère hépatique, artère
splénique) ;
•la multiplicité des classifications utilisées ;
•et surtout, la valeur que l’on attribue au curage ganglionnaire :
valeur diagnostique, pronostique et thérapeutique.
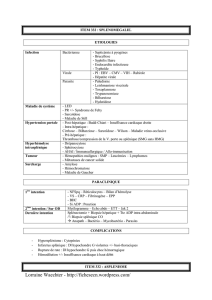
Il existe deux grandes classifications : la classification japonai-
se (Kodama) (2) et la classification TNM de l’UICC. La classi-
fication japonaise (schéma 1) distingue 16 sites ganglionnaires
numérotés de 1 à 16. Ces différents groupes sont classés en 4
catégories de N
1
à N
4
, correspondant aux groupes ganglion-
naires proximaux et distaux. À chaque groupe correspond un
type de curage D
1
(D pour Dissection) pour le groupe N
1
, D
2
pour le groupe N
2
et D
3
pour le groupe N
3
. Cette classification
est basée sur la fréquence des ganglions envahis en fonction du
siège du cancer sur l’estomac. La définition des ganglions
proximaux et distaux varie en fonction de la localisation du can-
cer et n’est pas univoque. Ainsi, un curage D
1
, D
2
ou D
3
ne
s’adressera pas aux mêmes groupes ganglionnaires et n’aura pas
la même importance selon que le cancer siège au niveau de
l’antre, du corps ou de la grosse tubérosité gastrique. Cette clas-
sification peut paraître complexe et d’application difficile mais
elle est logique. À titre d’exemple (tableau II), le groupe 1
(para-cardiaque droit) est classé N
2
pour un cancer antral et N
1
pour un cancer médio-gastrique. Les groupes 10 et 11 (hile splé-
nique et artère splénique) sont classés N
2
pour un cancer médio-
gastrique et N
3
pour un cancer antro-pylorique.
La classification TNM de l’UICC (1978) distingue trois groupes
de patients : les patients pN
1
en cas de ganglions N+ à moins de
3cm de la tumeur gastrique le long de la petite courbure ou de
la grande courbure. Les patients pN
2
en cas de ganglions N+
situés à plus de 3 cm de la tumeur, le long de l’un des trois
troncs artériels principaux de l’estomac (artère splénique, artère
hépatique et tronc cœliaque) et enfin, les patients pN
3
, en cas de
ganglions N+ siégeant à distance (para-aortiques, pancréatiques
et mésentériques).
Cette classification ne tient absolument pas compte du siège de
cancer sur l’estomac, la notion de ganglions proximaux et dis-
taux reste univoque et enfin, la notion de 3 cm est peu anato-
mique et critiquable.
Devant ces différentes classifications, les auteurs allemands ont
proposé 2 types de curage (Siewert) (3) : un curage standard qui
correspond à moins de 25 ganglions examinés et un curage éten-
du qui enlève plus de 25 ganglions. Ceci ne préjuge pas du siège
exact des ganglions prélevés et examinés, mais a le mérite d’in-
sister sur un nombre minimum de ganglions examinés. En effet,
une notion importante est que plus on examine de ganglions,
plus on trouve de ganglions envahis (Hermanek) (4),(tableau
III). Ceci explique en partie les chiffres de survie différents
observés selon que l’on pratique ou non des curages extensifs.
Les tumeurs sont certainement mieux classées lorsqu’on prélè-
ve un nombre suffisant de ganglions, et les stades II et III des
classifications japonaises sont certainement différents des
stades II et III de certaines séries anglo-saxonnes qui pratiquent
des curages limités.
QUEL TYPE DE CURAGE GANGLIONNAIRE ?
Faut-il se limiter au curage D
1
(ganglions proximaux) ou faut-il
étendre le curage et faire des curages de type D
2
, voire D
3
(gan-
glions distaux) ? En l’absence de traitement adjuvant efficace,
la seule chance de guérison du patient repose sur un acte chi-
rurgical bien fait avec un prélèvement suffisant de ganglions, en
espérant aller au-delà du dernier relais ganglionnaire envahi lors
de l’acte chirurgical.
1 Para-cardiaque droit
2Para-cardiaque gauche
3Petite courbure
4Grande courbure
5Suprapylorique
6Sous-pylorique
7Artère coronaire stomachique
8Artère hépatique commune
9Tronc cœliaque
10Hile splénique
11Artère splénique
12Pédicule hépatique
13Rétro pancréatique
14Racine du mésentère
15 Artère colique moyenne
16Para-aortique
Schéma 1.

La Lettre de L’Hépato-Gastroentérologue - n° 1 - février 199822
On a reproché aux curages extensifs une mortalité et une mor-
bidité importantes, ce que semblent confirmer deux études ran-
domisées récentes.
L’étude de Cushieri ( 5 ) portant sur 400 patients a montré une dif-
férence significative concernant la mortalité opératoire (6,5 %
versus 13,5 %) et la morbidité (28 % versus 48 %), celle-ci étant
liée à la splénectomie et la spléno-pancréatectomie.
L’étude de Bonenkamp (6) qui a randomisé 711 patients (308
ayant eu une dissection D
1
et 331 une dissection D
2
) a montré de
la même façon une différence significative concernant la morta-
lité (4 % versus 10 %) et la morbidité (25 % versus 43 %) avec
un taux significatif de réinterventions (8 % versus 18 %). Les
résultats préliminaires sur la survie (ASCO 1997) n’ont pas
montré de différence significative à 3 ans (84 % versus 85 % en
l’absence d’envahissement ganglionnaire et 46 % versus 48 %
en cas de N+) mais le recul est insuffisant.
En revanche, les études japonaises, bien que non randomisées,
ont montré un bénéfice sur la survie lorsque sont effectués des
curages extensifs, en particulier chez les patients ayant un enva-
hissement ganglionnaire proximal N
1
; survie à 5 ans : 38 % ver-
sus 61 % (Maruyama).
QUE FAUT-IL
FAIRE VIS-À-VIS
DE LA TUMEUR
GASTRIQUE ?
En c as de can-
cer antro - p y l o -
ri q u e , il fa u t
fa i r e une ga s -
t r e c t omie s ub-
totale (part i e l -
le inféri e u r e )
La gastrectomie
totale est inutile,
elle n’apporte
aucun bénéfice sup-
plémentaire concer-
nant la survie
comme l’a montré
une étude randomi-
sée de l’ARC et
AURC.
En effet, le risque
de cancer sur moi-
gnon gastrique est faible si l’on respecte une marge de sécuri-
té suffisante entre le pôle supérieur de la tumeur et la recoupe
gastrique (8 à 10 cm). Surtout, il faut s’assurer, avant d’eff e c-
tuer une gastrectomie subtotale, du caractère sain de la
muqueuse cardio-tubérositaire en pratiquant systématique-
ment des biopsies, l’existence d’une dysplasie pouvant impo-
ser une gastrectomie totale. Hormis ces cas particuliers, la gas-
trectomie subtotale est l’intervention effectuée. Le rétablisse-
ment de la continuité digestive sera réalisé avec une anse jéju-
nale, ascensionnée en pré-colique, en anisopéristaltique.
L’anastomose sera effectuée à plein canal (intervention de
Polya) ou après fermeture partielle de la tranche gastrique
(intervention de Finsterer). L’anse jéjunale peut être une anse
en Y ou une anse en Ω avec une anastomose au pied de l’anse
pour éviter le reflux biliaire.
QUEL TYPE DE CURAGE GANGLIONNAIRE FAU T-IL EFFEC-
TUER AU COURS D’UNE GAST R E C TOMIE DES 4/5 ?
Il faut faire un curage de type D
2
(exérèse des ganglions péri-
g a s t r i q u e s : groupes 3, 4, 5, 6) (N
1
) et l’exérèse des groupes 1,
7, 8, et 9 (N
2
) (groupes paracardiaque droit, coronaire stoma-
chique, cœliaque, hépatique commune). Ce type de curage
n’augmente ni la mortalité (0 à 2 %) ni la morbidité. Il est
inutile d’étendre le curage vers la rate, le hile splénique et
l’artère splénique (groupes 10 et 11°, ce qui correspond à un
curage D
3
). En effet, l’envahissement ganglionnaire est
exceptionnel à ce niveau (0 à 1 %, Noguchi) (7) et si les gan-
glions du hile splénique sont envahis en cas de cancer antro-
pylorique, il n’y a aucun bénéfice sur la survie à attendre de
leur exérèse (Sasako) ( 8 ) .
D
O S S I E R T H É M A T I Q U E
K. Antral
K. Médio-gastrique
3 PC
4 GC
5 sus-pylorique
6 sous-pylorique
3 4 5 6
+
1 para-cardiaque D.
1 para-cardiaque droit
7 coronaire stomachique
9 cœliaque
8 hépatique commune
7 coronaire stomachique
8 hépatite commune
9 cœliaque
11 A. splénique
(2 et 10)
11 A. splénique
12 pédicule hépatique
13 rétro-pancréatique
14 racine mésentère
(2 et 10)
12 pédicule hépatique
13 rétro-pancréatique
14 racine mésentère
15 para-aortique
16 colique moyenne
15
16
K. Cardio-tubéro s i t a i r e
1 para-cardiaque D.
2 para-cardiaque G.
3 PC
4 GC
Proximaux D I S T A U X
7 8 9 1 1
+
10 hile splénique
(5 et 6)
12
13
14
15
16
Tableau II. Classification japonaise (Kodama).
N
1
N
2
N
3
N
4
Hermanek P. UICC-TNM 1993.
Nb ganglions
< 5
6-15
16-25
26-35
36-45
> 45
18
29
45
55
59
66
% N+
Tableau III.
Envahissement
ganglionnaire en
fonction du nombre
de ganglions
examinés
(gastrectomies
curatives R
0
).

La Lettre de L’Hépato-Gastroentérologue - n° 1 - février 1998 23
En cas de cancer médio-gastrique ou du 1/3 supérieur
(cardio-tubérositaire)
Il faut faire une gastrectomie totale. Concernant le rétablisse-
ment de la continuité digestive, de multiples montages plus ou
moins complexes ont été décrits.
Le plus utilisé avec de bons résultats fonctionnels est l’ascen-
sion d’une anse jéjunale en Υ avec anastomose œso-jéjunale,
termino-latérale, effectuée manuellement ou à la pince méca-
nique. Pour éviter les reflux, l’anastomose au pied de l’anse
doit être située à 80 cm de l’anastomose supérieure. Faut-il
faire un réservoir gastrique pour améliorer le confort des
p a t i e n t s ? Il y a actuellement plusieurs études randomisées, cer-
taines sont en faveur du réservoir mais d’autres n’y voient
aucun bénéfice.
La question primordiale est la suivante :
Faut-il faire une gastrectomie totale simple ou faut-il faire une
gastrectomie totale élargie à la rate et au pancréas permettant le
curage des groupes ganglionnaires du hile splénique (groupe
10) et de l’artère splénique (groupe 11) ?
La place de la splénectomie et de la pancréatectomie reste
débattue. Si l’on envisage un curage ganglionnaire de type D
2
pour un cancer médio-gastrique ou cardio-tubérositaire, il faut
réséquer les groupes ganglionnaires 2 (paracardiaques), 7
(coronaire stomachique), 8 (hépatique commune) et 9
(cœliaque) qui n’imposent pas de spléno-pancréatectomie,
mais il faut également réséquer les groupes 10 et 11 qui néces-
sitent l’exérèse de la rate et du pancréas. Avant d’envisager
une gastrectomie totale élargie, il faut toujours avoir à l’esprit
la mortalité et la morbidité engendrées par une telle interven-
tion. La mortalité opératoire est faible après gastrectomie tota-
le (0 à 1 % ) ; en revanche, après gastrectomie totale élarg i e ,
elle est de 15 % .
QUELLE EST LA PLACE DE LA SPLÉNECTOMIE ?
Le risque d’envahissement ganglionnaire au niveau du hile
splénique et de l’artère splénique est très variable selon les
auteurs, selon le siège de la tumeur (médio-gastrique ou car-
dio-tubérositaire ou la totalité de l’estomac) et l’extension de
la tumeur (séreuse + ou séreuse -). Pour Fortner (9), l ’ e n v a -
hissement des ganglions du hile splénique s’observerait dans
6 4 % des cancers cardio-tubérositaires lorsque la séreuse est
envahie, mais pour Noguchi (7), le risque de N+ splénique
n’est que de 14 %.
Seule, la splénectomie permet le curage des ganglions du hile
splénique. Mais cette splénectomie est responsable d’une
mortalité opératoire plus élevée, d’une morbidité et d’une
diminution des défenses immunitaires. Il y a peu d’études
randomisées concernant le rôle de la splénectomie dans la
c h i r u rgie du cancer de l’estomac. Les études sont rétrospec-
tives et, il y a toujours un biais de sélection, le groupe des
patients ayant eu une splénectomie étant toujours plus grave
et la tumeur étant toujours plus évoluée (T
4
ou N
2
). Le t a b l e a u
I V montre quelques études récentes comparant la survie des
groupes splénectomisés et non splénectomisés. Les groupes
sans splénectomie semblent avoir une meilleure survie. Seule
l’étude de Toge (Hiroshima) est randomisée et, après avoir
éliminé les cancers cardio-tubérositaires avec un envahisse-
ment de la séreuse et les patients qui avaient en peropératoire
un envahissement ganglionnaire évident du hile splénique,
cette étude montre qu’il y a un bénéfice sur la survie pour les
stades III et IV ( 1 2 % versus 51 %) dans le groupe splénecto-
misé (10).
En conclusion, il semble que la splénectomie ne soit indi-
quée qu’en cas de cancer cardio-tubérositaire, envahissant la
séreuse, et lorsqu’il y a un envahissement évident des gan-
glions du hile splénique. Elle est inutile et nuisible dans tous
les autres cas.
QUELLE EST LA PLACE DE LA PANCRÉATECTOMIE ?
Elle permet le curage du groupe 11 (artère splénique). Certains
auteurs ont proposé le curage de l’artère splénique sans pan-
créatectomie, mais le risque de complications semble aussi
important qu’après pancréatectomie distale. La pancréatectomie
ne doit être associée à la gastrectomie totale que de nécessité, en
cas d’envahissement direct du pancréas par une tumeur gas-
trique à développement postérieur.
En conclusion, on peut proposer l’attitude chirurgicale suivante :
•Cancer antro-pylorique : gastrectomie subtotale et curage de
type D
2
.
•Cancer médio-gastrique ou cardio-tubérositaire : gastrectomie
totale simple chez les sujets âgés ou en cas de tumeur n’enva-
hissant pas la séreuse, ou en cas de tumeur siégeant sur la peti-
te courbure.
•Gastrectomie totale + splénectomie lorsque la tumeur siège sur
la grande courbure et lorsqu’elle envahit la séreuse, ou lorsqu’il
y a un envahissement ganglionnaire du hile splénique (examen
extemporané).
Auteurs
Griffitz 207 71 %
34 % stades III
4 5 %
2 5 % stades III
Cushieri 200 50 % 30 %
Noguchi 113 65 % 40 %
Hiroshima (Toge) 64
51 %
stades III-IV
12 %
68 %
stades III-IV
51 %
Nombre
de patients
Pas de
splénectomie Splénectomie
Tableau IV.Rôle de la splénectomie : survie.

La Lettre de L’Hépato-Gastroentérologue - n° 1 - février 199824
D
O S S I E R T H É M A T I Q U E
•Gastrectomie totale + spléno-pancréatectomie, toujours de
nécessité lorsque le pancréas est envahi.
CONCLUSION
Si le type de gastrectomie subtotale ou totale en fonction du
siège du cancer sur l’estomac n’est plus discuté, l’importance du
curage ganglionnaire est encore débattue.
En faveur des curages extensifs, il y a une amélioration de la
survie, en particulier pour les stades II (27 % versus 55 %) et
pour les stades IIIA (25 % versus 38 %) (Siewert) ainsi qu’une
meilleure appréciation du stade (ratio entre N+ et N examinés).
Contre les curages extensifs, on retient une mortalité et une
morbidité plus élevées, liées essentiellement à la splénectomie
et à la pancréatectomie.
On gardera à l’esprit qu’il faut adapter l’extension des curages
en fonction de l’état général et de l’âge du patient, du siège du
cancer sur l’estomac, de l’extension de la tumeur (en particulier
de l’envahissement de la séreuse) et des découvertes peropéra-
toires.
En l’absence de consensus actuel concernant les curages, il est
bien difficile de valider les études randomisées testant l’intérêt
d’un traitement adjuvant, en particulier une chimiothérapie. Un
nombre minimum de ganglions doit être examiné pour classer
valablement la tumeur. Le couple chirurgien-anatomopatholo-
giste est primordial pour l’analyse des ganglions et la précision
de leur siège. Une standardisation des curages est indispensable
dans les années à venir.■
R
É F É R E N C E S B I B L I O G R A P H I Q U E S
1.
Roder J.D., Bottcher K., Siewert J.R., Busch R., Hermanek P., Meyer H.J. and
the German Gastric Carcinoma Study Group. Prognostic factors in gastric carci -
noma. Cancer 1993 ; 72 (7) : 2089-97.
2.
Kodama Y., Sugimachi K., Soejima K. et coll. Evaluation of extensive
lymph node dissection for carcinoma of the stomach. World J Surg 1981 ; 5 :
2 4 1 - 8 .
3.
Siewert J.R., Kestelmeier R., Busch R. et coll. Benefit of lymph node dissection
for patients with gastric cancer and pN
0
and pN
1
lymph node metastases. Br J
Surg 1996 ; 83 : 1144-7.
4.
Hermanek P., Henson D.G., Hutter R.V., Sobin L.H. UICC-TNM, Supplement
1993. Springer Verlag Berlin 1993.
5.
Cushieri A., Fayers P., Fielding J. et coll. Post-operative morbidity and mor -
tality after D
1
and D
2
resection for gastric cancer. Preliminary results of the MRG
randomized controlled surgical trial. Lancet 1996 ; 347 : 995-9.
6.
Bonenkamp J.J., Songun I., Hermans J. et coll. Randomized comparison of
morbidity after D
1
and D
2
dissection for gastric cancer in 996 dutch patients.
Lancet 1995 ; 345 : 745-8.
7.
Noguchi Y., Imada T., Matsumoto A. et coll. Radical surgery for gastric can -
cer. Cancer 1989 ; 64 : 2035-61.
8.
Sasako M., Mc Culloch P., Kinoshita T., Maruyama K. New method to evalua -
te the therapeutic value of lymph node dissection for gastric cancer. Br J Surg
1995 ; 82 : 346-51.
9.
Papachristou D.N., Fortner J.G. Selection of gastrectomy for adenocarcinoma
arising in the gastric fundus. J Surg Oncol 1992 ; 21 : 165-9.
10.
Kwon S.J. Prognostic impact of splenectomy on gastric cancer. Results of the
Korean gastric cancer study group. World J Surg 1997 ; 21 : 837-44.
M o t s - c l é s . Cancer gastrique - Traitement chirurgical -
Curage ganglionnaire.
A b o n n e z - v o u s !
A b o n n e z - v o u s !
A b o n n e z - v o u s !
A b o n n e z - v o u s !
A b o n n e z - v o u s !
1
/
5
100%