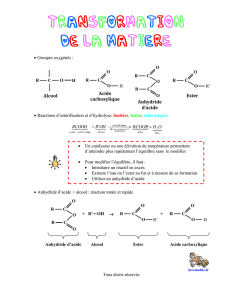
Le cycle de Krebs

Le cycle de Krebs
Le cycle de l’acide citrique
Le cycle tricarboxylique
dans les mitochondries Îconditions AÉROBIES
Acétyl-CoA
CO2
énergie
Voie finale, COMMUNE de l’oxydation des molécules
énergétiques : acides aminés, acides gras, glucides Figures tirées de
Copyright © 2004 by W. H. Freeman & Company
Lehninger Principles of Biochemistry
Fourth Edition
Chap V.

C6
C6
C5
C4
C4
C4
C4
C4
Vue générale du cycle de l’acide citrique

¾2 carbones entrent dans le cycle, 2 autres carbones en sortent
sous forme de CO2
¾4 réactions d’oxydo réduction ont lieu
- 6 électrons sont transférés sur 3 NAD+
- 1 paire d’atomes d’hydrogène (2 électrons) sont transférés
sur FAD
¾1 liaison phosphate, riche en énergie est formée à chaque
tour (1 GTP)
Régénération de NAD+et de FAD conduit à la formation de 3
ATP et de 2 ATP respectivement, dans la chaîne respiratoire
3×3 + 1×2 + 1×1 = 12 ATP

Vue détaillée du cycle de l’acide citrique

CCOO-
CH2
COO-
CH3
C
O
S-CoA
CCOO-
HO
CH2
COO-
COO-
CH2
C COO-
HO
CH2COO-
CH2S-CoAC
O
1. Condensation de l’oxaloacétate et de l’acétyl coenzyme A
Oxaloacétate
+
Acétyl-CoA
+ H2O
Citrate synthétase
Acide citrique
+ HS-CoA + H+
Intermédiaire =
Citryl-CoA
I. Les 9 étapes en détail
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
1
/
25
100%