Complications cardiaques de la radiothérapie – Radiation toxicity to

La Lettre du Cardiologue • n° 421 - janvier 2009 | 21
DOSSIER THÉMATIQUE
Complications cardiaques
de la radiothérapie
Radiation toxicity to the heart
Philippe Giraud*, Mehdi Henni*, Jean-Marc Cosset**
* Service d’oncologie-radiothérapie,
hôpital européen Georges-Pompi-
dou, Paris.
** Département d’oncologie-radio-
thérapie, institut Curie, Paris.
E
n raison de sa position anatomique et de
la relative radiosensibilité de certaines de
ses structures, le cœur constitue un organe
“critique” pour la radiothérapie thoracique. Il est
habituellement admis que les complications car-
diaques des rayonnements ionisants (RI) représen-
tent la deuxième cause de décès après la progression
de la maladie néoplasique chez les patients qui ont
reçu une irradiation médiastinale (1-3).
Parallèlement à l’amélioration des taux de survie
enregistrés pour les cancers, notamment pour la
maladie de Hodgkin, on a progressivement été
confronté aux complications cardiaques liées à la
radiothérapie, celles-ci apparaissant plusieurs années,
voire plusieurs décennies après l’irradiation (2-4).
Cependant, en raison de la grande variabilité des
symptômes, des nombreux cofacteurs cardiotoxiques
(chimiothérapie, tabagisme, etc.), et des techniques
d’irradiation très hétérogènes, voire “ancestrales”
– certaines pouvant dater d’une vingtaine d’années –,
leur évaluation précise reste complexe.
Après avoir rappelé brièvement la physiopathologie
des effets des RI sur le cœur, nous rapporterons
les principales complications aiguës et tardives
décrites dans la littérature, ainsi que les traitements
proposés.
Physiopathologie des
complications cardiaques liées
aux rayonnements ionisants
Les mécanismes physiopathologiques des effets
des RI sur le cœur sont mal connus. Ils relèvent
très vraisemblablement tous des mêmes phéno-
mènes successifs, débutant par une atteinte de la
microvascularisation induisant une ischémie tissu-
laire, responsable, à son tour, d’une fibrose cicatri-
cielle tardive (5-7). Le péricarde est le tissu le plus
souvent affecté par les RI. Son atteinte se manifeste
essentiellement sous la forme d’un épaississement
fibrotique vraisemblablement lié à des phénomènes
tardifs d’ischémie par microangiopathie, dont la
pathogénie exacte reste inconnue. D’autres méca-
nismes pourraient également être en cause, comme
la persistance d’un exsudat inflammatoire à la
surface du péricarde, induisant des réactions biochi-
miques en cascade (inhibition de l’activateur du
plasminogène, production de collagène, etc.) [8, 9].
Le myocarde est plus rarement touché que le péri-
carde, mais ses lésions sont plus graves. L’atteinte
myocardique est caractérisée par la présence de
plaques diffuses de fibrose, rarement de nécrose,
affectant plus fréquemment le ventricule gauche
que le ventricule droit en raison de sa situation plus
antérieure. Ces zones de fibrose myocardique corres-
pondent habituellement à des lits tissulaires d’aval
d’artères coronaires altérées (7, 10). La biopsie n’est
que rarement indiquée en raison du peu de corré-
lation entre l’image histologique et la répercussion
fonctionnelle (6, 7). Comme pour les autres tissus
cardiaques, les mécanismes physiopathologiques
en cause relèvent plus d’une atteinte des cellules
endothéliales des capillaires myocardiques, avec
thromboses intravasculaires et microruptures des
parois vasculaires, que d’une atteinte directe des
myocytes par les RI (5, 10). L’atteinte de l’endocarde
se manifeste le plus souvent par la formation de
plaques de fibrose. Rarement symptomatiques, ces
lésions résultent surtout d’une ischémie ou d’une
hypoxie consécutive à l’atteinte de la vascularisa-
tion artérielle. L’atteinte des artères coronaires se
caractérise par une hyperplasie fibromusculaire
endoluminale qui s’accompagne d’une aggravation
du risque d’athérosclérose et induit une atteinte
architecturale (valvulopathies) et fonctionnelle du
myocarde (troubles de conduction) [11-13]. L’exis-
tence d’une pathologie coronarienne préexistante est

22 | La Lettre du Cardiologue • n° 421 - janvier 2009
Résumé
La radiothérapie thoracique expose à la survenue de complications qui peuvent intéresser toutes les tuniques du cœur. Ces
toxicités cardiaques comprennent les péricardites aiguës et chroniques, les myocardites, les valvulopathies, les atteintes
coronariennes et les troubles de la conduction. Leurs mécanismes physiopathologiques relèvent très vraisemblablement
tous des mêmes phénomènes successifs, faisant intervenir une atteinte de la microvascularisation responsable d’une
ischémie tissulaire secondaire, celle-ci conduisant à son tour à une fibrose cicatricielle tardive. Cependant, la plupart des
complications cardiaques des rayonnements ionisants sont asymptomatiques. La péricardite chronique affecte environ 5 %
des patients, et le taux de mortalité qui lui est imputable est inférieur à 1 %. Les myocardites sont beaucoup plus rares. Très
longtemps ignorées, les atteintes des artères coronaires sont probablement responsables de la survenue tardive d’infarctus,
de valvulopathies ou de troubles de la conduction. Ces atteintes sont d’autant plus fréquentes que les patients sont porteurs
d’autres facteurs de risque cardiovasculaire ou ont été irradiés jeunes (avant 21 ans). Les facteurs de risque reconnus de ces
toxicités sont la dose totale (plus de 30 Gy), le volume de cœur irradié et la dose par fraction. Ces complications pouvant
survenir très longtemps après l’irradiation, une surveillance prolongée et stricte est nécessaire.
Mots-clés
Radiothérapie
Cœur
Toxicité
Summary
Thoracic irradiation could be
complicated by adverse effects
to every structure of the heart.
Potential injury of irradiation
can include acute and late
pericarditis, cardiomyopathy,
valvular disease and conduction
abnormalities. The pathophy-
siology of these various
syndromes is probably similar,
starting by prior microvascular
injury that leads to subsequent
myocardium ischemia, all of
which cause late fibrous scars.
However, most complications
are often asymptomatic. Late
pericarditis affects approxi-
mately 5% of the patients and
the mortality rate is under 1%.
Cardiomyopathy is rare. A long
time unrecognized, coronary
artery disease, diagnosed in 5
to 10% of the patients, begets
multifarious sequelae like
myocardial infarction, valvular
abnormalities and cardiac
rhythm changes. This coronary
artery disease is more likely to
occur if the patient was young
at the time of the irradiation
(< 21 years old) and/or if other
cardiovascular risk factors are
associated. Radiation-induced
heart complications seem to be
related to total dose (> 30 Gy),
irradiated tissue volume and
fraction size. Since cardiac
complications appear months to
years following incidental irra-
diation, appropriate screening
and long-term cardiac follow-
up are essential.
Keywords
Radiotherapy
Heart
Toxicities
très probablement un cofacteur essentiel à l’origine
de la plupart des complications décrites.
Les complications cardiaques des chimiothérapies
ne rentrent pas dans le cadre de cette revue. Cepen-
dant, nombreuses sont les molécules antimitotiques
potentiellement cardiotoxiques, et l’association de la
radiothérapie à ces molécules aggrave bien entendu
encore le risque de complications (5, 14).
Symptomatologie clinique
Le suivi des patients traités pour une maladie de
Hodgkin fournit depuis de nombreuses années des
informations des plus complètes sur la toxicité
cardiaque des RI (2, 4, 8, 9, 15). Les complications
cardiaques sont responsables de 25 % des décès qui
surviennent chez les patients guéris, et de 2 à 5 %
de l’ensemble des décès (3). En revanche, dans le
cadre du cancer du sein ou du cancer de l’œsophage,
le volume de cœur irradié étant moins important, la
tolérance est meilleure et la fréquence des compli-
cations plus faible (16, 17).
L’élément essentiel à retenir, s’agissant des compli-
cations cardiaques des RI, est la longueur du délai
de latence entre l’irradiation et l’apparition des
symptômes (quand ils apparaissent, car, si l’atteinte
cardiaque est très fréquente, elle reste souvent
asymptomatique) [2-4, 16].
La péricardite
Pendant l’irradiation, les symptômes sont surtout
marqués par l’atteinte péricardique. Cette maladie
inflammatoire bénigne est rare et ne nécessite qu’ex-
ceptionnellement l’arrêt du traitement. Les symptômes
sont semblables à ceux des péricardites aiguës classiques.
Habituellement, ils disparaissent en quelques semaines
et ne constituent pas un facteur de risque pour le
développement futur d’une péricardite chronique.
Seuls 20 % des patients qui développent une péricar-
dite aiguë présenteront secondairement, 5 à 10 ans
plus tard, une péricardite chronique constrictive (8, 9).
Cependant, une véritable péricardite aiguë peut appa-
raître dans les mois qui suivent le traitement, voire
jusqu’à 2 ans après l’irradiation (1, 8).
Une péricardite chronique peut survenir très tardi-
vement, plusieurs mois à plusieurs années après
l’irradiation. Sa fréquence est d’environ 1 à 5 %
après radiothérapie des cancers bronchiques et
mammaires, et de 5 à 10 % après radiothérapie des
lymphomes (8, 9). Le diagnostic de péricardite chro-
nique dépend surtout de l’initiative du praticien qui
demande sa recherche et des moyens d’investigation
utilisés. Dans la littérature, le taux de mortalité par
atteinte péricardique est estimé à 0,7 % chez les
patients traités pour une maladie de Hodgkin (8, 9).
Comme pour la péricardite aiguë, les symptômes de
la péricardite chronique ne sont pas spécifiques. La
majorité de ces péricardites guérissent spontané-
ment et sans séquelle. Cependant, quelques-unes
évoluent jusqu’au stade de péricardite constrictive
tardive et, dans de rares cas, vers une tamponnade
nécessitant une péricardectomie ou un drainage du
péricarde. En dehors de cette présentation inha-
bituelle, le traitement est avant tout médical, la
chirurgie étant à réserver aux cas menaçants ou
extrêmement exsudatifs (8, 15).
La myocardite
La myocardite survient en général chez des patients
qui présentent déjà une péricardite constrictive avec
des signes sévères d’insuffisance cardiaque diasto-
lique. Elle devient évidente quand les signes cardia-
ques persistent malgré le traitement de la péricardite
(5, 9). Son incidence est difficile à déterminer. Très
faible avec les nouvelles techniques de radiothérapie,
le risque augmente en cas d’association avec une
chimiothérapie, et en particulier avec les anthracy-
clines (14). Dans une série nécropsique de patients
irradiés dans leur jeune âge, une fibrose myocardique
a été retrouvée dans environ 50 % des cas (15). Dans
les nombreuses publications parues sur le suivi de
patients irradiés pour une maladie de Hodgkin, on
retrouve une diminution de la fraction d’éjection
du ventricule gauche dans 30 à 50 % des cas (2, 4).
Mais l’interprétation de ces résultats reste subjective
compte tenu des techniques d’irradiation très diffé-
rentes, des incertitudes relatives au calcul des doses
et du recul d’observation très variable. Il faut noter
que les patients traités avec les techniques les plus

La Lettre du Cardiologue • n° 421 - janvier 2009 | 23
DOSSIER THÉMATIQUE
modernes semblent garder une fonction cardiaque
normale et la conserver au cours du temps (17). Le
traitement de cette myocardite radio-induite n’est
pas spécifique et s’attache surtout à corriger les
signes d’insuffisance cardiaque (18).
Les atteintes coronariennes
Les complications coronariennes sont rares. Cepen-
dant, leur fréquence réelle est très probablement sous-
estimée, car elles sont souvent asymptomatiques ou
responsables de lésions cardiaques secondaires non
spécifiques (myocardiopathies, valvulopathies, troubles
de la conduction, etc.) [5, 11, 12]. Les autres facteurs
de risque, hypercholestérolémie ou tabagisme par
exemple, semblent potentialiser le développement des
lésions coronariennes (17). La mortalité par infarctus
du myocarde est de 2,5 % dans l’étude de Stanford sur
les maladies de Hodgkin, avec un risque relatif d’en-
viron 4 (2). Ces chiffres ont été confirmés dans d’autres
études (2-4). Comme pour les myocardiopathies, la
plupart des équipes retrouvent une fréquence et une
gravité d’autant plus importantes que les patients
ont été irradiés jeunes (15). Ces complications coro-
nariennes apparaissent généralement 5 à 6 ans après
l’irradiation, soit un temps de latence globalement
plus long que pour les autres atteintes cardiaques, avec
une nette prédominance des lésions monotronculaires
proximales. Cette caractéristique topographique incite
à dépister précocement ces lésions afin de proposer
une dilatation rapide rétablissant un bon lit d’aval
pour la revascularisation myocardique. Pour le reste,
le traitement de ces atteintes coronaires n’est pas
différent de celui des lésions dues aux causes plus
classiques (athérome, etc.) [12].
Les valvulopathies
Le principal mécanisme serait une atteinte indirecte
des valves par un processus de fibrose myocardique
périvalvulaire qui entraînerait secondairement leur
dysfonction (11). L’atteinte valvulaire peut se révéler
extrêmement fréquente si des méthodes diagnos-
tiques sophistiquées sont employées pour la recher-
cher. Son incidence est alors comprise en moyenne
entre 15 et 30 %. L’incidence cumulative est de 45 %
à 20 ans et de 60 % à 25 ans (2, 4, 11). L’atteinte
valvulaire est le plus souvent à type d’insuffisance
mitrale ou aortique. La mortalité globale par atteinte
valvulaire chez des patients irradiés sur le médiastin
peut atteindre 0,3 % (11).
Les troubles de la conduction
Le mécanisme le plus probable de ces lésions serait
une atteinte des voies de conduction secondaire
à une ischémie ou à une fibrose post-radique. Les
troubles de la conduction restent le plus souvent
asymptomatiques ; ils ne sont souvent détectés
que sur un ECG systématique, qui révèle habituel-
lement des troubles de la phase de repolarisation
dans les dérivations précordiales (13). Cependant,
des atteintes plus sérieuses telles que des troubles
de la conduction atrioventriculaire ou intraventri-
culaire ont été décrites 1 à 23 ans après une irradia-
tion (13 ans en moyenne) [1, 4, 13].
Apport de la radiothérapie
moderne
Le meilleur traitement des complications cardiaques
des RI reste la prévention. Les effets des RI sur le
cœur dépendent essentiellement de trois facteurs : la
dose par fraction, la dose totale et le volume de cœur
irradié (5, 17). La réduction de ces facteurs permet de
diminuer le risque d’atteinte cardiaque. La dose par
fraction joue un rôle non négligeable. J.M. Cosset et
al. ont montré que l’incidence cumulative des péri-
cardites à 5 ans était de 5 % pour une dose par frac-
tion de 2,5 Gy et de près de 7,5 % pour des fractions
de 3,3 Gy (9). Le risque relatif est multiplié par 2
lorsque la dose par fraction est égale ou supérieure
à 3 Gy. Cependant, le volume de cœur irradié est
probablement le facteur le plus important. Plus ce
volume est conséquent, plus le risque de complica-
tions est élevé. Si l’ensemble du péricarde est irradié,
l’incidence des complications aiguës et chroniques
atteint 20 %, contre seulement 7 % lorsque le
ventricule gauche est protégé (9). La radiothérapie
conformationnelle tridimensionnelle (figure 1),
l’irradiation avec modulation d’intensité, et notam-
ment la tomothérapie, pourraient représenter une
solution en diminuant le volume cardiaque irradié.
De même, l’asservissement respiratoire (figure 2),
nouvelle technique consistant à délivrer l’irradia-
tion à un moment précis, toujours identique, du
cycle respiratoire, permettrait de diminuer l’irradia-
tion cardiaque en éloignant le cœur des faisceaux
d’irradiation tangentiels utilisés pour le cancer du
sein (figure 3) [18, 19]. La dose totale est également
un facteur capital. L’étude des résultats des irradia-
tions en mantelet pour une maladie de Hodgkin
a montré que l’incidence cumulative des péricar-
dites sur 5 ans augmente avec la dose totale (9).

Figure 1. Irradiation
moderne, selon
une technique
conformationnelle
tridimensionnelle sus-
diaphragmatique,
du médiastin et des aires
cervicales inférieures
(faisceau antérieur en trait
jaune) pour une maladie
de Hodgkin.
Figure 2. Système
de radiothérapie asservie
à la respiration avec
blocage respiratoire
volontaire et dispositif de
feedback par lunettes vidéo
(système SDX de la société
Dyn’R, service de radio-
thérapie, hôpital européen
Georges-Pompidou, Paris).
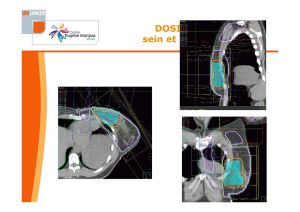
Figure 3. Distribution de dose d’une irradiation
du sein gauche par deux champs tangentiels
et de la chaîne mammaire interne gauche par
un faisceau antérieur direct sans (A) et avec (B)
asservissement respiratoire. Le trait jaune
correspond au contour du sein
en respiration normale, le trait rouge
correspond au contour en blocage inspiratoire
maximum. Pour chaque technique, l’isodose
bleue correspond à la quantité de cœur irradiée
à une dose de 30 Gy (potentiellement toxique).
A
B
24 | La Lettre du Cardiologue • n° 421 - janvier 2009
DOSSIER THÉMATIQUE
Toxicité cardiovasculaire
des traitements anticancéreux Complications cardiaques
de la radiothérapie

La Lettre du Cardiologue • n° 421 - janvier 2009 | 25
DOSSIER THÉMATIQUE
À fractionnement égal, elle est de 4 % pour une dose
de 36 Gy et de plus de 10 % pour des doses supé-
rieures à 41 Gy. Le risque relatif dépassait 3 lorsque la
dose était supérieure à 41 Gy (9). L’âge des patients
est également à prendre en compte. Les patients irra-
diés avant 20 ans à des doses supérieures à 35 Gy ont
un risque relatif de décès par infarctus du myocarde
de 44, le risque étant de 22 pour les causes cardiaques
autres (15). Pour les coronaropathies, la correc-
tion des facteurs de risque coronariens classiques
constitue une mesure préventive essentielle.
Conclusion
La radiothérapie thoracique, dont le rôle bénéfique
est par ailleurs indiscutable, peut être responsable
de complications cardiaques potentiellement graves.
Le risque est majoré chez les patients qui ont des
facteurs de risque cardiovasculaires classiques et
chez ceux qui ont été irradiés jeunes ; il augmente
encore en cas d’association à une chimiothérapie,
classiquement aux anthracyclines. Des progrès
considérables ont été réalisés sur le plan technique
pour limiter ces risques. La réduction des volumes
irradiés, les améliorations de la balistique, l’adap-
tation des doses par séance et la diminution des
doses totales ont d’ores et déjà permis de limiter
drastiquement le risque de ces complications cardia-
ques. Les premiers résultats de ces effets sont donc
probants, mais, le temps de latence de ces compli-
cations étant long, il convient de rester prudent et
de suivre très étroitement nos patients sur le long
terme. ■
1. Gaya AM, Ashford RFU. Cardiac complications of radiation
therapy. Clin Oncol 2005;17:153-9.
2. Hancock SL, Hoppe RT. Long-term complications of treat-
ment and causes of mortality after Hodgkin’s disease. Sem
Radiat Oncol 1996;6:225-42.
3. Henry-Amar M, Hayat M, Meerwaldt J et al. Causes of
death after therapy for Hodgkin’s disease entered on EORTC
protocols. Int J Radiat Oncol Biol Phys 1992;79:389-91.
4. Aleman B, Van den Belt-Dusebout A, De Bruin M et al.
Late cardiotoxicity after treatment for Hodgkin lymphoma.
Blood 2007;109:1878-86.
5. Giraud P, Cosset JM. La toxicité cardiaque de la radio-
thérapie : physiopathologie, données cliniques. Bull Cancer
2004;9:S147-53.
6. Archambeau J, Inès A, Fajardo LF. Response of swine skin
microvasculature to acute single exposures of x-rays: quan-
tification of endothelial changes. Radiat Res 1984;98:37-
51.
7. Fajardo LF, Stewart JR, Cohn KE. Morphology of radiation-
induced heart disease. Arch Pathol 1968;86:512-9.
8. Coltart RS, Thom CH, Roberts JT et al. Severe constrictive
pericarditis after single 16MeV anterior mantle irradiation
for Hodgkin’s disease. Lancet 1985;3:488-9.
9. Cosset JM, Henry-Amar M, Pellae-Cosset B et al. Peri-
carditis and myocardial infarction after Hodgkin’s disease
therapy. Int J Radiat Oncol Biol Phys 1991;21(2):447-9.
10. Fajardo LF, Stewart JR. Pathogenesis of radiation-induced
myocardial fibrosis. Lab Invest 1973;29:244-57.
11. Carlson RG, Mayfield WR, Normann S et al. Radiation-
associated valvular disease. Chest 1991;99:538-45.
12. Fajardo LF. Radiation-induced coronary artery disease.
Chest 1977;71:563-77.
13. Lindahl J, Strender LE, Larsson LE et al. Electrocardio-
graphic changes after radiation therapy for carcinoma of
the breast. Acta Radiol Oncol 1983;22:433-40.
14. Monsuez JJ, Charniot JC, Vignat N. Complications
cardiaques des maladies malignes et de leurs traitements.
EMC (Elsevier Masson SAS Paris), Cardiologie, 11-048-C-
10, 2008.
15. Hancock SL, Donaldson SS, Hoppe RT. Cardiac disease
following treatment of Hodgkin’s disease in children and
adolescents. J Clin Oncol 1993;7:1208-15.
16. Jones JM, Ribeiro GG. Mortality patterns over 34 years
of breast cancer patients in a clinical trial of post-operative
radiotherapy. Clinical Radiology 1989;40:204-8.
17. Prosnitz RG, Chen YH, Marks LB. Cardiac toxicity
following thoracic radiation. Semin Oncol 2005;32(Suppl.
3):S71-S80.
18. Remouchamps VM, Vicini FA, Sharpe MB, Kestin LL,
Martinez AA, Wong JW. Significant reductions in heart and
lung doses using deep inspiration breath hold with active
breathing control and intensity-modulated radiation therapy
for patients treated with locoregional breast irradiation. Int
J Radiat Oncol Biol Phys 2003;55(2):392-406.
19. Giraud Ph, Yorke E, Jiang SB et al. Reduction of organ
motion effects in IMRT and conformal 3D radiation delivery
by using gating and tracking techniques. Cancer Radiother
2006;10(5):269-82.
Références bibliographiques
Abonnez-vous en ligne !
Bulletin d’abonnement
disponible page 35
www.edimark.fr
1
/
5
100%