Influence du tabac sur la thyroïde et ses fonctions – Influence of

Correspondances en Métabolismes Hormones Diabètes et Nutrition - Vol. XIII - n° 2 - mars-avril 2009
69
dossier thématique
* Service d’endocrinologie,
maladies métaboliques
et nutrition, CHU de Toulouse.
P
roblème majeur de santé publique, le tabagisme
exerce des effets néfastes sur de nombreux
organes et est à l’origine d’un excès de morbi-
mortalité globale. La thyroïde peut être considérée
comme une cible directe et les effets du tabac sur cette
glande endocrine commencent à être mieux connus.
Dans cette synthèse, nous étudierons successivement
l’impact du tabagisme sur la fonction thyroïdienne et
sur le volume thyroïdien, le lien entre tabagisme et
auto-immunité thyroïdienne, et finalement les rap-
ports entre tabagisme maternel et retentissement sur
la thyroïde fœtale.
Impact du tabac sur la fonction
thyroïdienne
Plusieurs études se sont intéressées aux liens existant
entre le tabagisme, son importance (niveau de consom-
mation) et la fonction thyroïdienne, avec des résultats
parfois discordants. Chez l’adulte sain, le tabac exerce
peu d’effet sur la fonction thyroïdienne, éventuellement
un effet faiblement stimulant. Les taux de tri-iodothy-
ronine (T3l) sont en effet significativement supérieurs
chez le fumeur alors que les taux de thyroxine (T4l) sont
inchangés. La plupart des études rapportent une dimi-
nution du taux de TSH chez le fumeur, bien que d’autres
travaux n’aient pas confirmé ce lien (1). Le mécanisme
incriminé est incertain, mais plusieurs hypothèses ont
été émises : l’activation thyroïdienne par le système
sympathique induite par la nicotine, l’autonomisation
relative du tissu thyroïdien.
Parmi les patients atteints d’hypothyroïdie infraclinique
ou fruste, les fumeurs présentent des concentrations
supérieures de TSH, une T3l inférieure, un niveau de
cholestérol total et de LDL-cholestérol plus élevé que
les non-fumeurs. Par ailleurs, chez les patients atteints
d’hypothyroïdie avérée, les fumeurs et les non-fumeurs
sont caractérisés par des concentrations de TSH et
d’hormones thyroïdiennes similaires, mais les patients
fumeurs présentent plus de symptômes compatibles
avec un hypométabolisme. Ainsi, dans un contexte
d’hypothyroïdie infraclinique, le tabac semble réduire
la sécrétion des hormones thyroïdiennes et entraîner
une résistance à l’effet des hormones thyroïdiennes
susceptible d’exacerber les signes périphériques chez
ces sujets, comme chez les patients porteurs d’une
hypothyroïdie avérée (2).
Les principaux composants du tabac incriminés dans
les anomalies de la fonction thyroïdienne sont les thio-
cyanates. La détoxication des cyanides contenus dans
la fumée de cigarette élève en effet la concentration
plasmatique de thiocyanates. Or, ces molécules sont
des inhibiteurs du symporteur sodium-iodure (NIS) et
de l’organification de l’iode, entraînant une réduction
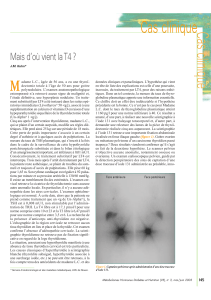
de la synthèse hormonale thyroïdienne (figure, p. 70).
Cet effet inhibiteur est dépendant des apports iodés.
En effet, l’augmentation de l’apport iodé diminue les
effets antithyroïdiens des thiocyanates (3).
Influence du tabac sur la thyroïde
et ses fonctions
Influence of smoking on the thyroid and its functions
Jean-Christophe Maiza*, Philippe Caron*
L’influence du tabagisme sur la fonction thyroïdienne reste discutée,
»
et semble modeste chez le sujet sain.
Chez les sujets porteurs d’une hypothyroïdie avérée ou fruste,
»
certains composants du tabac tels que les thiocyanates semblent
réduire la sécrétion des hormones thyroïdiennes et entraîner
une résistance à l’effet des hormones thyroïdiennes susceptible
d’exacerber les signes périphériques.
Le tabagisme constitue un facteur de risque de développer un goitre
»
euthyroïdien, essentiellement en situation de carence iodée.
Il existe une corrélation négative entre le tabagisme et le risque
»
de cancer thyroïdien.
L’incidence de la maladie de Basedow et de l’orbitopathie
»
basedowienne est majorée chez les fumeurs ; le tabac constitue
un facteur de résistance au traitement de ces pathologies.
Durant la grossesse, le tabagisme maternel expose à des anomalies
»
thyroïdiennes fœtales, tant fonctionnelles que morphologiques.
Mots-clés : Tabagisme – Thyroïde – Auto-immunité – Grossesse.
Keywords: Smoking – Thyroid – Auto-immunity – Pregnancy.
Points forts

Correspondances en Métabolismes Hormones Diabètes et Nutrition - Vol. XIII - n° 2 - mars-avril 2009
70
dossier thématique
Influence du tabac sur le volume
thyroïdien
Goitre euthyroïdien
La consommation de tabac est classiquement associée
à une augmentation du volume thyroïdien. Lors de
l’étude SU.VI.MAX, comportant des sujets âgés de 25
à 60 ans séjournant en France, le volume thyroïdien
mesuré par échographie est supérieur chez les fumeurs.
Cet effet goitrigène semble sous la dépendance des
thiocyanates, puisqu’il existe une corrélation positive
entre le volume thyroïdien et le niveau de concentration
urinaire des thiocyanates (4).
Une méta-analyse de 25 études s’intéressant au lien
entre tabac et dysthyroïdie rapporte une majoration
du risque de développer un goitre multinodulaire
non toxique chez les fumeurs, particulièrement chez
les femmes, avec un risque relatif modérément, mais
significativement, élevé de 1,29 (IC95 : 1,01-1,65) [5].
Plusieurs études antérieures suggéraient un lien entre
goitre thyroïdien et tabagisme, mais uniquement dans
les zones de carence iodée. Plus récemment, deux étu-
des rapportent l’impact du statut iodé sur le lien entre
volume thyroïdien et tabagisme. La première s’intéresse
aux variations du volume thyroïdien chez des fumeurs
dont le statut iodé est modifié par supplémentation
alimentaire sur une période de 4 ans. Cette correction
de la carence iodée a permis de réduire l’impact du
tabagisme sur le volume thyroïdien : la différence de
volume thyroïdien entre les fumeurs et les non-fumeurs
diminue de 24 % (IC95 : 19-29 %) à 12 % (IC95 : 6-18 %) avec
l’apport iodé (6). La deuxième étude compare le volume
thyroïdien de sujets fumeurs et non fumeurs dans une
région ayant bénéficié d’une correction récente de
la carence iodée : la corrélation entre le tabagisme et
le volume thyroïdien s’avère négative chez les sujets
de moins de 40 ans, mais positive chez les sujets âgés
de plus de 60 ans (7). Ainsi, le tabagisme constitue un
facteur de risque de développer un goitre euthyroïdien,
essentiellement dans les populations présentant une
carence iodée.
Cancer thyroïdien
Plusieurs travaux rapportent une diminution du risque
de cancer thyroïdien chez les patients présentant une
intoxication tabagique. Une étude cas-témoin a en
particulier évalué l’impact du tabac sur le risque de
développer un cancer thyroïdien : plus de 1 200 sujets
canadiens atteints de cancers thyroïdiens différen-
ciés ont été appariés avec 2 600 sujets témoins. Par
comparaison avec les sujets non fumeurs, le risque de
développer un cancer thyroïdien était inférieur chez
les fumeurs avec un risque relatif de 0,77 (IC95 : 0,58-
1,02) parmi la population masculine et, de 0,71 (IC95 :
0,60-0,83) parmi la population féminine. Le bénéfice
semble persister chez les anciens fumeurs (8). Chez
les femmes, la réduction du risque est plus marquée
avant la ménopause ou lorsque le tabagisme a débuté
tôt, avant l’âge de 15 ans.
Deux hypothèses sont émises pour expliquer cette
corrélation négative entre tabagisme et risque de cancer
thyroïdien. Comme précédemment décrit, le niveau de
TSH est diminué chez le fumeur et il est parfaitement
connu que le risque de développer un cancer thyroï-
dien différencié est influencé par le niveau de TSH. Par
ailleurs, le métabolisme des œstrogènes peut être impli-
qué dans la pathogénie du cancer thyroïdien et l’effet
anti-œstrogène du tabac a été démontré (9).
Tabagisme et auto-immunité thyroïdienne
Maladie de Basedow
L’incidence de la maladie de Basedow est majorée chez
les fumeurs, avec un risque relatif compris entre 1,9
(IC95 : 1,1-2,7) et 3,3 (IC95 : 2,09-5,22) par comparaison
avec les non-fumeurs et selon les études (5, 10). Les
mécanismes de cette association ne sont pas connus et
le taux d’anticorps antirécepteurs de la TSH ne semble
pas impliqué.
Par ailleurs, le risque de récidive est conditionné par
deux facteurs principaux : la persistance d’un taux élevé
d’anticorps antirécepteur de la TSH et la consommation
Figure. Impact du tabagisme sur la synthèse des hormones thyroïdiennes.
Cibles moléculaires de l’effet inhibiteur des thiocyanates sur la synthèse des hormones thyroïdiennes.
Pendrine Colloïde
Thyrocyte
(cellule
folliculaire)
Réticulum
endoplasmique
Golgi
Clathrine
Transcytose
Noyau
Lysosome
Dégradation
Endosome
Pinocytose
Thyroglobuline
HT
Tpo Thox
Nis
I–
I–
I–
Na+
Na+Na+K+
K+
ATP
ase
Capillaire
I–
II

Correspondances en Métabolismes Hormones Diabètes et Nutrition - Vol. XIII - n° 2 - mars-avril 2009
71
Influence du tabac sur la thyroïde et ses fonctions
tabagique. Glinoer et al. rapportent en effet un taux
de récidive de 18 % chez le non-fumeur contre 57 %
chez le fumeur en l’absence d’anticorps antirécepteur
de la TSH, et de 86 % chez le non-fumeur contre 100 %
chez le fumeur en cas de persistance des anticorps
antirécepteur de la TSH (11).
De même, le risque de développer une orbitopathie
basedowienne est nettement plus élevé chez le fumeur
que chez le non-fumeur, avec des risques relatifs esti-
més entre 4,4 et 7,7 selon les études (12, 13). Toutes
les études sont concordantes pour établir ce lien et le
nombre de fumeurs est nettement supérieur parmi les
patients ayant développé une orbitopathie que parmi
les sujets présentant une maladie de Basedow sans com-
plication oculaire. De plus, le risque de développer une
orbitopathie est corrélé au niveau de consommation
tabagique. Par ailleurs, la gravité de l’orbitopathie est en
rapport avec le niveau d’intoxication tabagique comme
cela a été décrit : par rapport aux non-fumeurs, le ris-
que relatif de développer une diplopie est de 1,8 (IC95 :
0,8-4,3) pour une consommation de 1 à 10 cigarettes
par jour, de 3,8 (IC95 : 1,9-9,7) pour une consommation
de 11 à 20 cigarettes par jour et de 7 (IC
95
: 3,0-16,5)
pour une consommation supérieure à 20 cigarettes
par jour (14).
Plusieurs hypothèses mécanistiques sont avancées
pour expliquer l’effet du tabac sur l’apparition d’une
orbitopahie. Il est probable que l’irritation oculaire
locale par la fumée soit un facteur aggravant. Sur le
plan immunologique, la diminution de l’activité des
lymphocytes T suppresseurs chez le fumeur pourrait
concourir au développement de l’auto-immunité cel-
lulaire responsable de l’orbitopathie basedowienne.
L’hypothèse d’une altération de la structure du récep-
teur de la TSH par le tabac a également été proposée.
Plus récemment, une étude in vitro a mis en évidence
un lien entre les produits de dégradation de la fumée
de tabac, d’une part, et l’augmentation de la produc-
tion de glycosaminoglycanes et la stimulation de
l’adipogenèse, d’autre part (15). Ainsi, les produits
chimiques issus de la fumée de cigarette, transportés
jusqu’à la cavité orbitaire par le courant circulatoire,
pourraient stimuler les fibroblastes avec pour consé-
quence une expansion du volume tissulaire. La stimu-
lation de l’adipogenèse est sous la dépendance de
l’interleukine 1 (IL-1). L’utilisation d’un antagoniste de
l’IL-1, déjà utilisé pour le traitement de la polyarthrite
rhumatoïde, pourrait donc représenter une stratégie
thérapeutique efficace en inhibant les effets stimulants
des produits de dégradation de la fumée sur l’adipo-
genèse et donc limiter la progression de l’orbitopathie
basedowienne.
Finalement, le tabagisme est un facteur de résistance au
traitement de l’orbitopathie basedowienne. L’efficacité
des traitements immunosuppresseurs (corticothérapie,
radiothérapie orbitaire) est réduite chez le fumeur. Le
risque d’apparition ou d’aggravation d’une orbitopa-
thie basedowienne après irathérapie est également
majoré chez le fumeur (16, 17). En pratique, ces données
imposent un arrêt du tabagisme actif ou passif chez les
patients présentant une maladie de Basedow, a fortiori
s’ils présentent une orbitopathie, afin de diminuer la
gravité de l’atteinte oculaire et d’augmenter l’efficacité
des traitements immunomodulateurs.
Maladie d’Hashimoto
Il semble exister une relation inverse entre la consom-
mation tabagique et le risque de maladie d’Hashimoto.
En effet, dans une cohorte hollandaise, il a été rapporté
une diminution significative de la présence d’anticorps
antithyropéroxydase (anti-TPO) chez les femmes pour-
suivant une intoxication tabagique avec un risque relatif
de 0,69 (IC95 : 0,48-0,99) par rapport aux non-fumeurs.
Des résultats similaires ont été rapportés dans l’étude
NHANES III au cours de laquelle les anticorps anti-TPO
et antithyroglobuline (anti-Tg) ont été mesurés chez
15 592 sujets indemnes de toute pathologie thyroï-
dienne aux États-Unis, ainsi que dans une étude danoise
récente rapportant un risque relatif de 0,66 (IC95 : 0,55-
0,79) en faveur des fumeurs (18). Enfin, il a été montré
récemment que le sevrage tabagique expose au risque
de développer une auto-immunité thyroïdienne, avec
une recrudescence de l’apparition d’anticorps anti-TPO
et anti-Tg (19).
Il n’existe pas d’explication rationnelle pour cette dimi-
nution du risque d’auto-immunité thyroïdienne en lien
avec l’intoxication tabagique, bien que des hypothèses
aient été émises, notamment l’effet anti-inflammatoire
de la nicotine sur le système immunitaire. Cependant, à
ce jour, aucune de ces hypothèses n’a pu être confirmée
expérimentalement.
Tabagisme maternel et fonction
thyroïdienne fœtale
L’équilibre thyroïdien est modifié pendant la grossesse
en raison des modifications du métabolisme de l’iode,
principalement caractérisées par une diminution du
pool iodé maternel liée à une augmentation de la clai-
rance rénale de l’iodure et au transfert transplacentaire
de l’iode vers le versant fœtal. Or, dans le même temps,
la thyroïde maternelle est stimulée du fait d’une aug-
mentation de la TBG sous l’effet des œstrogènes et de

Correspondances en Métabolismes Hormones Diabètes et Nutrition - Vol. XIII - n° 2 - mars-avril 2009
72
dossier thématique
la sécrétion placentaire d’HCG. La grossesse est donc
une période de fragilité pour la fonction thyroïdienne
de la mère. De plus, les paramètres de l’environne-
ment exerçant un effet sur la thyroïde sont à même
de modifier l’équilibre thyroïdien dans cette situation
particulièrement vulnérable.
Une étude récente s’est intéressée aux liens entre
les fonctions thyroïdiennes maternelle et fœtale
et le tabagisme (20). Les paramètres fonctionnels
thyroïdiens ont été explorés chez 1 428 femmes au
cours du premier trimestre de leur grossesse et chez
927 femmes durant le troisième trimestre. Dans les
deux cohortes, la concentration maternelle de TSH
était plus basse et la concentration de T3l plus élevée
chez les fumeuses, ce qui est également observé
en dehors de la grossesse. Parmi les femmes ayant
interrompu le tabagisme en début de grossesse, les
paramètres fonctionnels thyroïdiens sont identiques
à ceux des femmes n’ayant jamais fumé. La fonction
thyroïdienne du fœtus a, quant à elle, été évaluée
sur le sang du cordon lors de l’accouchement. La
TSH des fœtus nés de mères ayant poursuivi une
intoxication tabagique pendant la grossesse est signi-
ficativement plus basse. La T3l est supérieure dans
ces conditions, mais de manière non significative,
contrairement aux résultats d’une étude antérieure
(21). Enfin, les enfants nés de mères tabagiques sont
plus fréquemment hypotrophes, ce qui pourrait s’ex-
pliquer en partie par ce profil d’hyperfonctionnement
thyroïdien.
Sur le plan morphologique, il existe une relation positive
entre le taux des thiocyanates mesuré au cordon et le
rapport volume thyroïdien/poids de naissance. Une
augmentation des concentrations de thyroglobuline
a de surcroît été rapportée chez les nouveau-nés de
mères fumeuses actives ou passives (22).
Ainsi, le tabagisme maternel expose à des anomalies
thyroïdiennes fœtales, tant fonctionnelles que mor-
phologiques. Même si la relation directe entre l’hyper-
thyroxinémie et l’hypotrophie fœtale n’est pas établie
et que les conséquences à long terme sur le risque
de pathologie thyroïdienne chez les enfants nés de
mères tabagiques n’ont pas été évaluées, la normalité
des paramètres fonctionnels thyroïdiens observés à
la naissance en cas d’arrêt de l’intoxication tabagique
au début de la grossesse doit inciter à proposer une
aide au sevrage tabagique chez toutes les femmes qui
envisagent une grossesse.
■
1.Utiger RD. Effects of smoking on thyroid function. Eur J
Endocrinol 1998;138:368-9.
2.Tziomalos K, Charsoulis F. Endocrine effects of tobacco
smoking. Clin Endocrinol 2004;61:664-74.
3.Fukayama H, Nasu M, Murakami S, Sugawara M.
Examination of antithyroid effects of smoking products in
cultured thyroid follicles: only thiocyanate is a potent anti-
thyroid agent. Acta Endocrinol 1992;127(6):520-5.
4.Barrère X, Valeix P, Preziosi P, Bensimon M, Pelletier B, Galan P,
Hercberg S. Determinants of thyroid volume in healthy French
adults participating in the SU.VI.MAX cohort. Clin Endocrinol
2000;52(3):273-8.
5.Vestergaard P. Smoking and thyroid disorders-a meta-ana-
lysis. Eur J Endocrinol 2002;146(2):153-61.
6.
Vejbjerg P, Knudsen N, Perrild H et al. The impact of smoking
on thyroid volume and function in relation to a shift towards
iodine sufficiency. Eur J Epidemiol 2008;23(6):423-9.
7.Ittermann T, Schmidt CO, Kramer A et al. Smoking as a
risk factor for thyroid volume progression and incident goi-
ter in a region with improved iodine supply. Eur J Endocrinol
2008;159(6):761-6.
8.
Kreiger N, Parker R. Cigarette smoking and the risk of thyroid
cancer. Eur J Cancer 2000;36(15):1969-73.
9.
Galanti MR, Hansson L, Lund E et al. Reproductive history
and cigarette smoking as risk factors for thyroid cancer in
women: a population-based case-control study. Cancer
Epidemiol Biomarkers Prev 1996;5(6):425-31.
10.Holm IA, Manson JE, Michels KB, Alexander EK, Willett WC,
Utiger RD. Smoking and other lifestyle factors and the risk of Graves’
hyperthyroidism. Arch Intern Med 2005;165(14):1606-11.
11.
Glinoer D, de Nayer P, Bex M; Belgian Collaborative Study
Group on Graves’ Disease. Effects of l-thyroxine administration,
TSH-receptor antibodies and smoking on the risk of recurrence
in Graves’ hyperthyroidism treated with antithyroid drugs: a
double-blind prospective randomized study. Eur J Endocrinol
2001;144(5):475-83.
12.
Tziomalos K, Charsoulis F. Endocrine effects of tobacco
smoking. Clin Endocrinol (Oxf) 2004;61(6):664-74.
13.
Krassas GE, Wiersinga W. Smoking and autoimmune thyroid
disease: the plot thickens. Eur J Endocrinol 2006;154(6):777-80.
14.Pfeilschifter J, Ziegler R. Smoking and endocrine ophthalmo-
pathy: impact of smoking severity and current vs lifetime ciga-
rette consumption. Clin Endocrinol (Oxf) 1996;45(4):477-81.
15.Cawood TJ, Moriarty P, O’Farrelly C, O’Shea D. Smoking and
thyroid-associated ophthalmopathy: a novel explanation of the
biological link. J Clin Endocrinol Metab 2007;92(1):59-64.
16.Eckstein A, Quadbeck B, Mueller G et al. Impact of smoking
on the response to treatment of thyroid associated ophthal-
mopathy. Br J Ophthalmol 2003;87(6):773-6.
17.Bartalena L, Marcocci C, Tanda ML et al. Cigarette smoking
and treatment outcomes in Graves ophthalmopathy. Ann
Intern Med 1998;129(8):632-5.
18.Pedersen IB, Laurberg P, Knudsen N et al. Smoking is
negatively associated with the presence of thyroglobulin
autoantibody and to a lesser degree with thyroid peroxidase
autoantibody in serum: a population study. Eur J Endocrinol
2008;158(3):367-73.
19.
Effraimidis G, Tijssen JG, Wiersinga WM. Discontinuation
of smoking increases the risk for developing thyroid peroxidase
antibodies and/or thyroglobulin antibodies: a prospective
study. J Clin Endocrinol Metab 2009 (epub ahead a print).
20.Shields B, Hill A, Bilous M et al. Cigarette smoking during
pregnancy is associated with alterations in maternal and
fetal thyroid function. J Clin Endocrinol Metab 2008 (epub
ahead a print).
21.
McMahon MJ, Brown HL, Dean RA. Umbilical cord thio-
cyanate and thyroid function in intrauterine growth-restricted
infants of the smoking gravida. J Perinatol 1997;17(5):370-4.
22.
Chanoine JP, Toppet V, Bourdoux P, Spehl M, Delange F.
Smoking during pregnancy: a significant cause of neonatal
thyroid enlargement. Br J Obstet Gynaecol 1991;98(1):65-8.
Références
1
/
4
100%