Cas clinique M Mais d’où vient la T4 ?

Cas clinique
Cas clinique
Mais d’où vient la T4 ?
J.M. Kuhn*
M
adame L.C., âgée de 56 ans, a eu une thyroï-
dectomie totale à l’âge de 50 ans pour goitre
polynodulaire. L’examen anatomopathologique
extemporané n’a retrouvé aucun signe de malignité et,
l’étude définitive, une hyperplasie nodulaire. Un traite-
ment substitutif par LT4 a été instauré dans les suites opé-
ratoires immédiates (Lévothyrox®50 µg/j), associé à une
supplémentation en calcium et vitamine D en raison d’une
hypoparathyroïdie séquellaire de la thyroïdectomie totale
(Un-Alpha®1 µg/j).
Cinq ans après l’intervention thyroïdienne, madame L.C.,
qui se plaint d’un certain surpoids, modifie ses règles dié-
tétiques. Elle perd ainsi 25 kg sur une période de 18 mois.
Cette perte de poids importante s’associe à un certain
degré d’asthénie et à quelques accès de palpitations. La
mesure du taux de TSH plasmatique, qui s’inscrit à la fois
dans le cadre de la surveillance de cette hypothyroïdie
postchirurgicale substituée et dans le bilan étiologique
d’un amaigrissement important, est inférieure à 0,01 mU/l.
Consécutivement, le traitement substitutif par LT4 est
interrompu. Trois mois après l’arrêt du traitement par LT4,
la patiente reste asthénique, se plaint de troubles du som-
meil et toujours d’accès de palpitations. Elle pèse 68 kg
pour 1,65 m. Son rythme cardiaque est régulier à 92 pulsa-
tions par minute et sa pression artérielle à 130/60 mmHg.
Il existe un tremblement fin des extrémités. L’examen cer-
vical retrouve la cicatrice de thyroïdectomie sans aucune
autre anomalie locale. En particulier, il n’y a aucune adé-
nopathie dans les aires cervicales. L’examen ophtalmo-
logique est normal. À cette date, alors que la patiente ne
prend comme traitement que un µg de Un-Alpha®/j, la
TSH est à 0,008 mU/l, non stimulable par l’adminis-
tration de TRH. La T4 libre est à 17,1 pmol/l pour une
norme comprise entre 10 et 23 et la T3 libre à 6,47 pmol/l
pour une norme comprise entre 3,5 et 6. La recherche de
la présence d’anticorps anti-thyroïdien est négative.
L’échographie de la région cervicale ne retrouve aucun
tissu thyroïdien en lieu et place de la thyroïde. Cet examen
confirme l’absence d’adénopathie cervicale. La scinti-
graphie thyroïdienne ne retrouve pas de fixation signifi-
cative en regard de la loge thyroïdienne.
La situation, associant une hyperthyroïdie manifeste à une
absence de tissu thyroïdien cervical est très particulière.
Les causes classiques d’hyperthyroïdie à scintigraphie
blanche (thyroïdite subaiguë, hyperthyroïdie associée à
une surcharge iodée, etc.) ne peuvent être retenues, à la
fois compte tenu des antécédents de madame L.C. et des
données cliniques et paracliniques. L’hypothèse qui vient
en tête de liste des explications est celle d’une poursuite,
inavouée, du traitement par LT4, pour des raisons esthé-
tiques. Dans un tel contexte, la mesure du taux de thyro-
globuline plasmatique apporte une information essentielle.
Ce chiffre doit en effet être indétectable si l’hypothèse
précédente est la bonne. Ce n’est pas le cas pour Madame
L.C. dont le taux de thyroglobuline plasmatique atteint
1160 pg/l pour une norme inférieure à 40. Ce résultat a
amené, d’une part, à réaliser une nouvelle scintigraphie à
l’iode 131 avec balayage totocorporel et, d’autre part, à
demander une relecture des lames de la pièce de thyroï-
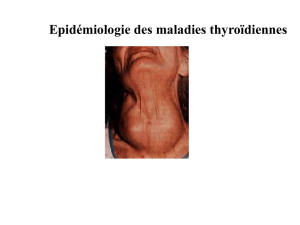
dectomie réalisée cinq ans auparavant. La scintigraphie
à l’iode 131 retrouve une importante fixation abdominale
localisée en fosse iliaque gauche (figure 1). Goitre ovarien
ou métastase pelvienne d’un carcinome thyroïdien passé
inaperçu ? Deux résultats viendront confirmer qu’il s’agit
en fait de la deuxième hypothèse. Le scanner pelvien
n’objective aucune anomalie, notamment osseuse ou
ovarienne. Un examen cœlioscopique pelvien, guidé par
la détection peropératoire des sites de captation d’une
dose traceuse d’iode 131 administrée au préalable, inno-
* Service d’endocrinologie et des maladies métaboliques, CHU de Rouen.
Figure 1. Captation pelvienne après administration d’une dose traceuse
d’iode 131.
Face antérieure Face postérieure
Métabolismes Hormones Diabètes et Nutrition (VII), no3, mai/juin 2003
145

146
Métabolismes Hormones Diabètes et Nutrition (VII), n° 3, mai/juin 2003
Cas clinique
Cas clinique
centera définitivement l’ovaire et localisera le foyer de
fixation isotopique pelvien au niveau du psoas gauche.
La relecture de l’examen anatomopathologique de la
pièce d’exérèse thyroïdienne permettra de retrouver au
sein d’un des nodules des caractéristiques moins typiques
que celles des adénomes vésiculaires habituels. Certaines
plages sont en effet plus cellulaires, avec un agencement
des microvésicules moins régulier. Les noyaux sont
arrondis et monomorphes. Dans quelques champs ont
été observées une ou plusieurs mitoses normales. Pour
l’anatomopathologiste, ces aspects incitaient à quelques
réserves sans qu’il y ait, en périphérie de la lésion, de
signe d’agressivité. Le nodule en question était bien déli-
mité du parenchyme voisin et il n’y avait ni franchisse-
ment de la capsule ni invasion vasculaire.
L’évolution ultérieure témoigne cependant que ces réserves
anatomopathologiques étaient pertinentes et qu’il est très
vraisemblable que ce soit à partir de cette lésion que ce
soit faite une dissémination vers le pelvis. Compte tenu du
diagnostic final : métastase musculaire pelvienne d’un
carcinome thyroïdien différencié, un traitement par iode
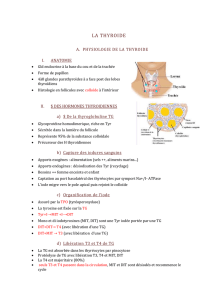
radioactif a été initié. La figure 2 illustre les variations des
taux de TSH et de thyroglobuline au cours de ce suivi.
L’association hyperthyroïdie-carcinome différencié de
la thyroïde est connue. Les cancers différenciés de la
thyroïde paraissent d’ailleurs trois à quatre fois plus
fréquents chez les patients hyperthyroïdiens que chez
ceux qui ont un équilibre hormonal thyroïdien normal (1).
La fréquence des carcinomes thyroïdiens responsables
d’hyperthyroïdie est beaucoup plus faible et, dans ce cas,
les métastases ont, en règle générale, un potentiel sécré-
toire réduit. Sur 125 patients, Gross et al. (2) ont retrouvé
des métastases sécrétrices d’hormones thyroïdiennes chez
6 patients. Dans de rares cas, la production d’hormones
thyroïdiennes par les métastases est liée à la présence
d’anticorps stimulant le récepteur de la TSH (3). Il s’agit
alors d’une association maladie de Basedow-carcinome
thyroïdien. La recherche de la présence de TSI étant
négative chez madame L.C., ce mécanisme ne peut être
retenu. L’explication la plus plausible est celle d’une
inflation de la sécrétion d’hormones thyroïdiennes par un
carcinome très différencié et expliqué soit par la masse
métastatique, soit éventuellement par la présence, au sein
de ces cellules, d’une mutation activatrice du récepteur
de la TSH (4).
Références
1.
Chigot JP, Menegaux F, Keopadabsy K et al. Thyroid cancer in patients
with hyperthyroidism. Presse Med 2000; 29 : 1969-72.
2.
Gross JL, Vasques Moraes I. Thyroid hormone-producing metastases in dif-
ferentiated thyroid cancer. J Endocrinol Invest 1996 ; 19 : 21-4.
3.
Ishihara T, Ikekubo K, Shimodahira M et al. A case of TSH receptor anti-
body-positive hyperthyroidism with functioning metastases of thyroid carcino-
ma. Endocr J 2002 ; 49 : 241-5.
4.
Camacho P, Gordon D, Chiefari E et al. A Phe 486 thyrotropin receptor
mutation in an autonomously functionning follicular carcinoma that was cau-
sing hyperthyroidism. Thyroid 2000 ; 10 : 1009-12.
Figure 2. Évolution des taux plasmatiques de thyroglobuline et de
TSH, avant (B) et après administration, lors de sevrage en T4, de
doses thérapeutiques d’iode 131.
1
/
2
100%