arthroplastie de la hanche

IUMSP
Institut universitaire de médecine sociale et préventive
Jean-Marie Januel1, Patrick S. Romano2, Phil Hider3, Cyrille Colin4,
Bernard Burnand5, William A. Ghali6
1 Institut Universitaire de Formation et de Recherche en Soins (IUFRS), Centre Hospitalier Universitaire Vaudois (CHUV), Université de Lausanne, Lausanne, Suisse
2 Department of General Medicine, Medical Center, University of California Davis, Sacramento, California, U.S.A
3 Department of Population Health, University of Otago, Christchurch, New-Zealand
4 Département Information Médicale, Evaluation et Recherche (Pôle IMER), Hospices Civils de Lyon (HCL), Lyon, France
5 Institut Universitaire de Médecine Sociale et Préventive (IUMSP), Centre Hospitalier Universitaire Vaudois (CHUV), Université de Lausanne, Lausanne, Suisse
6 Department of Community Health Sciences, Institute of Public Health, University of Calgary, Alberta, Canada

Intérêt des comparaisons internationales à
partir des mesures d’indicateurs
Evaluer la performance des systèmes de santé
oComparaisons (benchmarking)
oApprendre « des autres »
Montrer des différences
oOrganisation des systèmes de santé
oPratiques de codage
oPratiques de soins

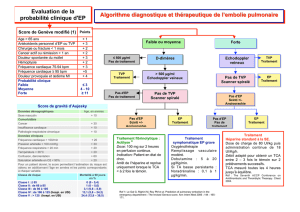
Comparer le taux d’occurrence des embolies pulmonaires
(EP) et des thromboses veineuses profondes (TVP)
survenant chez des patients hospitalisés ayant subit une
arthroplastie de la hanche (PTH, PPH) à partir des
données hospitalières de routine de plusieurs pays
Utiliser un «benchmark» externe comme valeur de
référence pour les comparaisons (evidence based practice)
Explorer les facteurs potentiels qui pourraient expliquer
les différences entre les pays (facteurs confondant pour
l’interprétation des comparaisons = biais)
Objectifs

Séjours d’hospitalisation des patients (≥ 18 ans) ayant
subit une arthroplastie de la hanche (PTH, PPH)
5 pays (Suisse, France, Canada, Nouvelle-Zélande, Etat
de la Californie aux USA)
Patient Safety Indicator (PSI) 12
Benchmark externe
Facteurs confondant « a priori » (stratification)
oDurée de séjour
oNombre de diagnostics secondaires codés
oRatio d’utilisation du doppler veineux des membres inférieurs pour la
détection systématique des TVP (code acte médical)
Etude observationnelle transversale

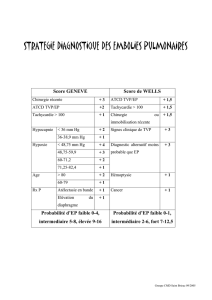
Algorithme utilisé 1,2
Codes CIM des Diagnostics Secondaires
d’EP et de TVP
Codes de procédures pour concernant les
interventions chirurgicales d’arthroplastie de
la hanche
PSI 12 =
1 Januel JM, Couris CM, Luthi JC, et al. For the International Methodology Consortium for Coded Health Information (IMECCHI).
Adaptation au codage CIM-10 de 15 indicateurs de la sécurité des patients proposés par l’Agence étasunienne pour la recherche et la
qualité des soins de santé (AHRQ). Rev Epidemiol Sante Publique 2011; 59: 341-350.
2 OECD Health Technical Report. Drosler S. Facilitating cross-national comparisons of indicators for patient safety at the health-
system level in OECD countries. Health Care Quality Indicators N°19. DELSA/ELSA/WD/http 2008.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
1
/
13
100%