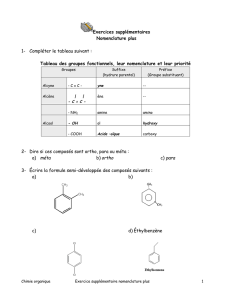
clique ici.

© iStockphoto/Thinkstock
La nomenclature des
composés chimiques
inorganiques

2
Les composés ioniques
•Un composé ionique comporte un ou des éléments métalliques et un ou des
éléments non métalliques.
•Le composé métallique donne un ou des électrons de sa couche de valence au
composé non métallique. Il devient ainsi un ion positif.
•Le composé non métallique reçoit un ou plusieurs électrons sur sa couche de valence.
Il devient ainsi un ion négatif.
+1 +1
-2
lithium lithium
oxygène
La formule chimique de ce composé est donc :
Li2O
Pour nommer un composé ionique, on commence par nommer le non-métal en
utilisant le nom de l’élément et en y ajoutant le suffixe approprié. On ajoute ensuite
l’article « de », suivi du nom du métal.
oxyde de lithium
métal métalnon-métal
Les suffixes :
N = nitrure
O = oxyde
F = fluorure
Cl = chlorure
S = sulfure
P = phosphure
Br = bromure
I = iodure
C = carbure

3
Les composés ioniques (suite)
Fe2O3
oxyde de fer
La nomenclature devient un peu plus complexe lorsque le métal du
composé est un des métaux de transition, car ces éléments ont plusieurs
charges possibles. Il est donc important d’indiquer celui dont il s’agit dans
le nom du composé.
FeO
oxyde de fer
Par exemple, le fer peut avoir une charge de 2+ ou de 3+ selon le tableau
périodique. Il faut donc s’assurer d’indiquer la charge dans le nom du
composé en l’écrivant en chiffres romains à la fin du nom. On peut alors
déduire la charge de l’élément selon sa formule chimique.
On utilise le chassé-croisé inverse pour déduire la charge. Étant donné
que l’oxygène a toujours une charge de 2-, on peut aussi utiliser la
logique mathématique.
3+ 2-
Dans le cas du FeO, si l’on utilise le chassé-croisé inverse, on obtient une charge de
1+ pour le fer et une charge de 1- pour l’oxygène. Or, comme l’oxygène a toujours
une charge de 2-, il faut utiliser la logique mathématique voulant que, si les
composés sont dans un rapport 1 pour 1 selon la formule, la charge du fer doit être
de 2+ pour annuler la charge de 2- de l’oxygène.
2-2+
(III)
Maintenant que nous connaissons les charges des composés, nous pouvons les nommer.
(II)

4
Les composés covalents
•Un composé covalent comporte deux ou plusieurs éléments non métalliques.
•Les éléments partagent des électrons pour devenir stables.
•Les éléments n’ont pas de charge.
fluor oxygène
La formule chimique de ce composé est donc :
OF2
Pour nommer un composé covalent, on commence par nommer le non-métal à la
droite en utilisant le nom de l’élément et en y ajoutant le suffixe approprié ainsi que
le préfixe de quantité. On ajoute ensuite l’article « de », suivi du nom du non-métal à
la gauche. On peut aussi lui ajouter un préfixe de quantité, au besoin.
difluorure d’oxygène
fluor
Les préfixes de quantité :
mono- (1)
di- (2)
tri-(3)
tétra- (4)
penta- (5)

5
Autres règles
Parfois, les composés contiennent des ions polyatomiques. Les ions polyatomiques
sont des regroupements communs de certains éléments ayant des noms particuliers.
Voici ceux qui seront les plus utilisés dans ce cours.
NH4+= ammonium
CH3COO-= acétate C6H5COO-= benzoate
BO33- = borate
CO32- = carbonate
HCO3-= bicarbonate ou hydrogénocarbonate
ClO4-= perchlorate
CrO42- = chromate
ClO3-= chlorate
ClO2-= chlorite
ClO-= hypochlorite
Cr2O72- = dichromate
CN-= cyanure
OH-= hydroxyde
IO3-= iodate
NO3-= nitrate
NO2-= nitrite
OOCCOO2- = oxalate
MnO4-= permanganate
HOOCCOO2- = hydrogéno-oxalate
PO43- = phosphate
HPO42- = hydrogénophosphate
SO42- = sulfate
SO32- = sulfite
HSO4-= hydrogénosulfate
HSO3-= hydrogénosulfite
CNO-= cyanate
SCN-= thiocyanate
S2O32- = thiosulfate
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
1
/
13
100%