notes - WordPress.com

Composés avec oxygène
A) Base : Composés qui renferment un ion métallique et l’ion négatif
hydroxyde (OH)-
Métal et OH
On les nomme : hydroxyde de (métal)
Ex : KOH
Ex : Ca et OH
Ex : hydroxyde de fer III
B) Oxydes : composés binaires formés d’oxygène et d’un autre élément
1) Oxydes métalliques : Métal et oxygène
On les nomme : oxyde de (métal)
Ex : K2O :
Ex : Al et O
Ex : oxyde de fer III
2) Oxydes non-métalliques : Non-métal et oxygène
On les nomme : (préfixe) oxyde de (préfixe autre que 1) (non-métal)
Ex : CO2
Ex : SO3
Ex : pentoxyde de dichlore
Ex : N2O6

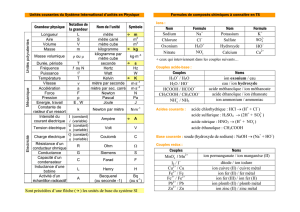
Préfixes pour le nombre d’atomes d’oxygène :
1
Mono-
6
Hexa-
2
Di-
7
Hepta -
3
Tri-
8
Octa -
4
Tétra-
9
Nona -
5
Penta-
10
Déca -
C) Acides ternaires avec oxygène (oxacides): sont formés d’hydrogène et
d’ions polyatomiques.
Hydrogène + non-métal + oxygène
(ou hydrogène + ion polyatomique)
On les nomme : acide (non-métal) ique
Ex : HFO3
Ex : HClO3
Ex : H2SO4
Ex : acide nitrique
Ex : acide carbonique
D) Sels ternaires avec oxygène : sels formés de trois éléments; formés d’un ion
métallique (ou de l’ion ammonium, NH4+) et d’un ion polyatomique.
Métal(ou NH4+) + non-métal + oxygène
(métal (ou NH4+) + ion polyatomique)
On les nomme : (ion polyatomique) de (métal)
Ex : NaClO3 :
Ex : (NH4)3PO4 :
Ex : sulfate de plomb IV

Les sels hydratés
Un sel hydraté est un sel auquel une ou plusieurs molécules d’eau s’est attachée.
Règle de nomenclature : nommer le sel et indiquer le nombre de fois que le sel est
hydraté à l’aide de préfixes grecs.
Ex : CuSO4 • 3H2O
Al2(SO4)3 • 10H2O
CaSO3 • 7H2O
LiCl • H2O

Ions polyatomiques
Valence = -1
Ion
Nom
Ion
Nom
BrO-
Hypobromite
HSO3-
Bisulfite
BrO2-
Bromite
HSO4-
Bisulfate
BrO3-
Bromate
IO-
Hypoiodite
BrO4-
Perbromate
IO2-
Iodite
CN-
Cyanure
IO3-
Iodate
CH3COO-
Acétate
IO4-
Periodate
ClO-
Hypochlorite
MnO4-
Permanganate
ClO2-
Chlorite
NO2-
Nitrite
ClO3-
Chlorate
NO3-
Nitrate
ClO4-
Perchlorate
OCN-
Cyanate
HCO3-
Bicarbonate
OH-
Hydroxyde
HS-
Hydrogénosulfure
SCN-
Thiocyanate
H2PO3-
Bihydrogénophosphite
H2PO4-
Bihydrogénophosphate
NH4 + = ammonium
Valence = -2
Ion
Nom
Ion
Nom
CO32-
Carbonate
O22-
Peroxide
C2O42-
Oxalate
SiO32-
Silicate
CrO42-
Chromate
SO32-
Sulfite
Cr2O72-
Bichromate
SO42-
Sulfate
HPO32-
Hydrogénophosphite
S2O32-
Thiosulfate
HPO42-
Hydrogénophosphate
Valence = -3
Ion
Nom
Ion
Nom
AsO33-
Arsénite
PO33-
Phosphite
AsO43-
Arséniate
PO43-
Phosphate
1
/
4
100%