Oxydoréduction en chimie organique

Oxydoréduction en chimie
organique

Rappel
De l’expérimentation à la notion de couple
redox
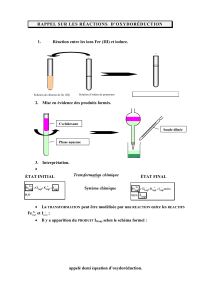
On montre que le métal zinc Zn réagit sur le
sulfate de cuivreII, Cu2+ SO42- pour former
du cuivre Cu et des ions Zn2+:
Zn(s) + Cu 2+ Cu(s) + Zn 2+

Zn est le réducteur (donneur d’électrons) et Cu2+ est
l’oxydant (capteur d’ e-) de la réaction.
Demi-équations associées:
Zn : Zn(s) Zn2+ + 2e-
Cu2+ : Cu2+ + 2e-Cu(s)
D’une façon générale, équation d’oxydoréduction:
Ox1 + Red 2= Red1+ Ox2
Ox1est plus fort que Ox2si la réaction va
spontanément dans le sens 1, c-à-d de gauche à
droite.

Oxydoréduction en chimie organique
•I. Définition
•On peut attribuer à tout élément présent dans
une molécule ou un ion un nombre d’oxydation
(N.O.) caractéristique de son état d’oxydation.
•si le N.O. de certains éléments varie au cours
d’une réaction, il s’agit d’une réaction
d’oxydoréduction.
•une augmentation en valeur algébrique du
N.O. est une oxydation pour l’élément concerné,
et une diminution une réduction.

•au cours d’une réaction d’oxydoréduction la
somme algébrique des N.O. de tous les
éléments concernés restent constante (la
variation totale des N.O. des éléments oxydés
est égale en valeur absolue à la variation totale
des N.O. des éléments réduits) .
•II. Détermination du nombre d’oxydation
d’un élément
•Composés covalents: on attribue (fictivement)
le doublet de chacune de ses liaisons à l’atome
le plus électronégatif des 2.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
1
/
16
100%