Absorbance croissance

AGREGATION DE
BIOCHIMIE - GENIE BIOLOGIQUE
Session 1999
Téléchargement du fichier au format .doc ag99mitp.zip
TRAVAUX PRATIQUES DE MICROBIOLOGIE
« Détection rapide de Salmonella spp dans un produit alimentaire »
CADRE DE L'ÉTUDE
Les salmonelloses demeurent la première cause de maladies d'origine alimentaire dans les
pays développés. Elles sont en particulier responsables des toxi-infections alimentaires
collectives (TIAC). Les produits alimentaires les plus souvent mis en cause sont les
ovoproduits, les viandes et les produits laitiers.
La recherche des Salmonella se pratique lorsqu'il y a survenue d'une TIAC, mais aussi en
routine, sur les chaînes de production agro-alimentaire concernées, dans le cadre de
démarches de type HACCP (Hazard Analysis Critical Control Point). Le critère
microbiologique relatif aux Salmonella est : « absence dans 25 grammes d'aliment ».
L'objectif de l'analyse microbiologique est donc de rechercher la présence d'au moins une
Salmonella dans un échantillon de produit. La faible quantité et le faible pourcentage de
Salmonella par rapport aux autres bactéries dans les produits alimentaires nécessite plusieurs
étapes de culture : préenrichissement, enrichissement, isolement sélectif et identification. Ces
étapes sont décrites dans la méthode de référence pour la recherche de Salmonella (NF ISO
6579). L’analyse selon cette méthode impose donc un délai de réponse important
Au cours de la manipulation, nous déterminerons, dans des conditions simples, pour
l'étape de
préenrichissement :
- la durée de la phase de latence λ,
- la vitesse spécifique de croissance en phase exponentielle Q
x expo
et la durée de cette phase.
- la croissance maximale X
max
Ces paramètres ont été choisis par analogie avec ceux pris en compte en microbiologie
prévisionnelle. Ils permettent de quantifier le développement d'un microorganisme
contaminant par l'étude de sa croissance, dans des conditions fixées et contrôlées conduisant à
une modélisation.
Pour l'étape d'enrichissement, nous étudierons l'évolution du pourcentage de Salmonella dans
une culture mixte.
Une approche plus récente combinant rapidité et sensibilité de détection fait appel à la
technologie PCR (Polymerase Chain Reaction). Elle consiste à amplifier un fragment

spécifique du génôme des Salmonella spp, puis à détecter l'amplicon par méthode immuno-
enzymatique (de type ELISA). On se propose ici de réaliser un protocole rapide qui met en
jeu trois opérations successives
:
- préenrichissement,
- amplification sélective in vitro (PCR),
- détection immuno-enzymatique (ELISA) de l'amplification.
TRAVAIL DU PREMIER JOUR
Il est indispensable de prévoir une organisation horaire précise des manipulations à
effectuer
A- Étude des étapes de la méthode de référence
Les trois manipulations de cette partie sont indépendantes mais doivent êt
re menées en
parallèle.
1- Phase de latence de l'étape de préenrichissement
Vous disposez d'un échantillon de crème anglaise contaminée par Salmonella Enteritidis à
raison de 1.10
4
bactéries par mL et conservée à 4°C pendant 24 heures. Le milieu de
préenrichissement utilisé est l'eau peptonée tamponnée (EPT).
Manipulation
- Ensemencer, au temps 0, un tube contenant 9 mL de milieu EPT par 1 mL de crème
contaminée.
- Homogénéiser.
- Incuber en bain thermostaté à 37°C.
- Toutes les 10 minutes à partir du temps 0 jusqu'au temps 90 minutes, réaliser un
dénombrement en surface :
prélever 0,1 mL de culture non diluée,
étaler en surface d'une gélose trypticase soja (GTS) à l'aide d'un étaleur stérile,
réaliser 2 essais pour chaque temps.
Pour le dernier temps (90 minutes), réaliser un dénombrement sur le prélèvement non
dilué et sur une dilution 10
-1
en eau physiologique de celui-ci.
- Incuber 24 heures à 37°C.
Cultures et milieux
- un échantillon de crème anglaise contaminée, en tube à essais ("crème n° ")
- un tube contenant 9 mL d'eau peptonée tamponnée ("EPT 9 mL n° ")
- un tube contenant 9 mL d'eau physiologique (bouchon doré noté 9 )

- 22 boîtes de gélose trypticase soja (GTS)
2- Phase exponentielle de croissance de l'étape de préenrichissement
Vous disposez d'une préculture de 18 heures de Salmonella Enteritidis en eau peptonée
tamponnée La croissance est suivie par turbidimétrie. La correspondance entre absorbance et
concentration bactérienne sera vérifiée par dénombrement direct au microscope.
2-1 Vérification de la relation entre absorbance et concentration bactérienne
Classiquement, il est établi qu'une unité d'absorbance à 600 nm correspond à 5.10
8
UFC par
mL
(
UFC : unité formant colonie, correspondant à une cellule bactérienne revivifiable ou à un
amas de cellules
).
La méthode utilisée pour le dénombrement direct est la méthode D.E.F.T. (Direct
Epifluorescent Filter Technique).
Dénombrement
Observer au microscope à épifluorescence la préparation fournie.
Faire contrôler par un examinateur.
Cette préparation a été préalablement réalisée par filtration sur membrane d'une dilution au
1/500
ème
de la préculture de Salmonella, selon le mode opératoire présenté en annexe 1.
L’absorbance de la préculture à 600 nm a été évaluée à 1,2.
Compte-rendu
1- Décrire qualitativement l'aspect de la préparation.
2- Justifier la différence de fluorescence des bactéries revivifiables et des bactéries "mortes".
3- Etablir la formule de calcul de la concentration de la préculture en « unités revivifiables »
par mL.
4- A partir du dénombrement effectué, vérifier la relation énoncée ci-dessus, entre
l’absorbance à 600 nm et la concentration bactérienne.
2-2 Etude de la phase exponentielle
Le suivi de la croissance est réalisé par turbidimétrie à 600 nm, toutes les lectures se font
directement en semi-microcuves contre le milieu de culture, le prélèvement de la culture est
donc de 1 mL au maximum.
Manipulation
- Effectuer une mesure d’absorbance de la préculture diluée au 1/4 en eau peptonée
tamponnée.
- Ensemencer l'erlen contenant 50 mL
d'EPT avec la préculture, de façon à démarrer la culture
à 0,05 unité d’absorbance à 600 nm.
Mesurer l'absorbance initiale, à t = 0 en présence d'un examinateur.
- Incuber en bain thermostaté à 37°C non agité.

- Prélever toutes les 10 minutes pendant 1 heure 30.
- Prélever ensuite toutes les 30 minutes jusqu'au temps t = 4 heures.
La limite de linéarité de la relation liant l'absorbance à 600 nm et la concentration
bactérienne est de 0,6.
Cultures et milieux
-
un tube contenant 12 mL de préculture de 18 heures de Salmonella Enteritidis ("S.Enteritidis EPT n° ")
- un flacon de 20 mL d'EPT ("EPT 20 mL")
- un erlen de 100 mL contenant 50 mL d'EPT, préchauffé en bain thermostaté à 37°C
("EPT 50 mL n° ")
Compte-rendu
1- Justifier la prise d’essai effectuée.
2- Tracer sur papier semi-logarithmique la courbe de croissance de Salmonella Enteritidis.
3- Analyser la courbe obtenue.
4- Déterminer graphiquement le temps de génération ; en déduire la vitesse spécifique de
croissance pendant la phase exponentielle en heure
-1
.
5- Déterminer graphiquement la durée de la phase exponentielle de croissance.
6- Estimer le facteur d'amplification des cellules lors du préenrichissement.
7- Calculer X
max
(UFC.mL
-1
).
3- Efficacité de la phase d'enrichissement
Vous disposez d’une préculture de Salmonella Enteritidis en bouillon nutritif ajustée à 1 unité
d'absorbance à 600 nm et d'une préculture d'Escherichia coli en bouillon nutritif également
ajustée à 1 unité d'absorbance à 600 nm.
La manipulation consiste à réaliser une suspension mixte calibrée en bouillon au sélénite
(dont la composition est donnée en annexe 2) et à suivre l'évolution du pourcentage de
chacune des 2 espèces lors de cette étape d'enrichissement, par dénombrement sur deux
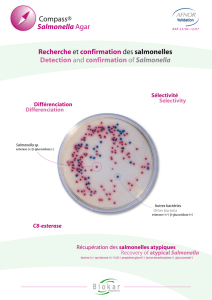
milieux sélectifs : Hektoën et Rambach (dont les compositions sont données en annexe 2).
Manipulation
- Préchauffer le tube de bouillon au sélénite à 37°C.
- Réaliser un mélange des deux précultures en ensemençant les 10 mL de ce bouillon au
sélénite avec :
100 µL de préculture de Salmonella Enteritidis,
900 µL de préculture d'Escherichia coli.
- Homogénéiser.
- Incuber à 37°C en bain thermostaté le bouillon au sélénite ensemencé.
- Effectuer au temps 0, au temps 2 heures et au temps 4 heures un dénombrement sur chacun
des 2 milieux sélectifs de la façon suivante :
A partir de 0,1 mL de culture, effectuer deux dilutions successives au 1/100 puis

une dilution au 1/10 en eau physiologique
étaler 0,1 mL de la dilution 10
-4
sur un milieu Hektoen à l'aide d'un étaleur stérile.µ
étaler 0,1 mL de la dilution 10
-5
sur un milieu Rambach à l'aide d'un étaleur stérile.
- Incuber les milieux d'isolement 24 heures à 37°C.
Cultures et milieux
- tube contenant 12 mL de préculture de 18 heures de S. Enteritidis .("S.Enteritidis A
600
=1 n° "),
- un tube contenant 10 mL de préculture de 18 heures de Escherichia coli ("E.coli A
600
=1 n° "),
- un tube contenant 9 mL de bouillon au sélénite ("sélénite n° "),
- 3 boîtes de gélose Rambach,
- 3 boîtes de gélose Hektoën,
- 6 tubes d’eau physiologique de 9,9 mL ( bouchons rose, notés 9,9),
- 3 tubes d’eau physiologique de 9 mL (bouchons dorés, notés 9).
Compte rendu
1- Expliquer le rôle de l’étape d’enrichissement en bouillon au sélénite.
2- Quelle évolution du pourcentage des deux espèces peut-on prévoir ?
3- En utilisant les données de l’annexe 2, dégager l’intérêt du milieu de Rambach par rapport
au milieu Hektoën pour la différenciation de Salmonella.
B- Détection des Salmonella par « PCR-ELISA »
La méthode consiste à amplifier une séquence de 340 paires de bases d’un gène impliqué dans
le pouvoir invasif de Salmonella spp, le gène iag A. On utilise pour cela deux amorces :
- une amorce « sens », de séquence 5’-GCA GGG ATC ACT AAG CTG TG-3’, marquée à
son extrémité 5’ par la biotine,
- une amorce « anti-sens », de séquence 5’-CGT GGG CAA CCA GCA CTA AC-
3’, marquée
à son extrémité 5’ par de la digoxigénine (DIG).
La présence éventuelle d’un amplicon sera mise en évidence par une technique immuno-
enzymatique (ELISA) utilisant un support sensibilisé par de l’avidine.
1-
Amplification par méthode PCR
L’ADN matrice utilisé est préparé à partir de la préculture de Salmonella Enteritidis ajustée à
1 unité d’absorbance à 600 nm ou de dilutions réalisées à partir de cette préculture, afin
d’étudier la sensibilité de la méthode.
Deux témoins sont effectués, l’un à partir de la préculture Salmonella Enteritidis en absence
d’amorce, l’autre à partir de la préculture d’Escherichia coli ajustée à 1 unité d’absorbance à
600 nm.
Les amplifications à réaliser sont présentées dans le tableau du paragraphe 1-3 ci-dessous.
Manipulation
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
1
/
14
100%