Voir la présentation

Cancers héréditaires
des seins et des ovaires
Viviane Feillel
IUCT - ONCOPOLE
ALBI
14 avril 2016

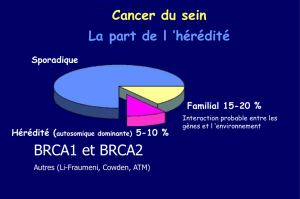
Cancer du sein : histoires familiales
1) Formes sporadiques
• Association fortuite
• Facteurs d’environnement
• Reflet de la grande fréquence
dans la population
2)Formes héréditaires: gènes majeurs de prédisposition
• Mutation germinale transmissible
• Forte agrégation familiale , âge précoce au diagnostic
3) Formes héréditaires
gènes de susceptibilité
• Polymorphismes peu connus
Effet multiplicatif – Xieurs gènes
Risque modéré à faible
<10%

Gènes majeurs de prédisposition:
BRCA (BReast CAncer)
Mutations délétères constitutionnelles
Inactivatrices
BRCA 1
Chromosome 17
BRCA 2
Chromosome 13
Gènes suppresseurs de tumeur: Rôle essentiel
Préservation de la structure chromosomique
Réparation de l’ADN, contrôle du cycle cellulaire……..

Hérédité :
Transmission autosomique dominante
Parent ( mère ou père)
Porteur d’une mutation BRCA
50% de risque d’avoir hérité
Pour chaque enfant (fille ou fils)
MUTATIONS DE PREDISPOSITION BRCA1/2

Haut risque de cancer: seins, ovaires et trompes
1
10 Ovaire< 45 ans
11 - 16 39 -59 Ovaire à 70 ans
32 (10 ans) 27 (10 ans) Sein controlat.
7
25
Sein < 45 ans
45 (40-85) 65 (40-85) Sein à 70 ans
BRCA2 BRCA1 P Générale
10 -13%
1,5%
Risque %
Sein traité conservé : risque de deuxième événement
après 7 ans post traitement
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
1
/
31
100%