P2-UE8-Masson-Mycoses exotiques (word)

UE8- De l’agent infectieux à l’hôte
Dr Masson
Date : 24/03/16 Plage horaire : 14h-15h
Promo: P2 2015-2016 Enseignant: Dr. Masson
Ronéistes : BLAISE Manon
VIDEAU Camille
Les mycoses exotiques
I. Introduction
1. Champignons filamenteux
2. Levures
3. Champignons dimorphiques
II. Mycoses exotiques
III. Mycoses liées aux champignons dimorphiques
1. Histoplasmose américaine
A. Exposition à une faible quantité de spores
B. Exposition à une grande quantité de spores
C. Forme disséminée chez les immunodéprimés
D. Diagnostic et anatomopathologie
2. Histoplasmose africaine
3. Coccidioïdomycose
4. Paracoccidioïdomycose
5. Blastomycose
6. Sporotrichose
7. Penicilliose

I. Introduction
Champignons « dimorphiques » car 2 formes : - champignon filamenteux (dans le sol)
- levure (pathogène dans les tissus)
Très rare en Europe. Ce chapitre sur les mycoses traite de pathologies peu rencontrées en pratique, il s’agit
plus de curiosité de la médecine. Les mycoses dites « exotiques » sont dues à des champignons
dimorphiques. Nous allons voir en introduction quelques variétés de champignons.
Beaucoup moins fréquents que les dermatophytes. Il s'agit de champignons très contaminants, pathogènes de
classe III.
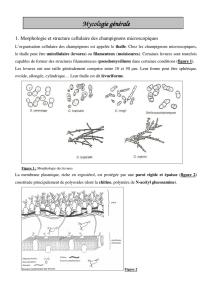
1. Champignons filamenteux On voit des filaments sur ces champignons. Le
thalle végétatif est formé de filaments, des spores
(ou conidies) qui peuvent se greffer dessus.
Les dermatophytes sont des champignons
filamenteux sur lesquels se greffent ces spores.
L’aspergillus est un champignon filamenteux
extrêmement présent dans l’environnement, on en
retrouve plusieurs milliers par mm3. Il contient
une tête aspergillaire (avec le mucus) et des
cellules spécialisées. Ces cellules spécialisées
sont appelées cellules conidiogènes ou phialides
et portent des spores (ou conidies).
Ce sont des formes de dissémination, les spores se déposent dans l’environnement. Les champignons
filamenteux sont très rarement pathogènes, ils donnent des mycoses superficielles comme dans le cas des
dermatophytes.
2. Levures Les levures sont des champignons de forme ronde (mais
il existe toutefois des formes un peu allongées).
Cette forme ronde est spécifique des levures.
Elles ont à peu près la taille d’une hématie et certaines
possèdent une capsule.
Elles ont un temps de croissance rapide (entre 48h et
72h) et se multiplient en bourgeonnant
(bourgeonnements unipolaire ou bipolaire).
La base de bourgeonnement peut être fine ou large, cela
fait partie des clés diagnostic.
Certaines levures, comme candida albicans, peuvent faire des filaments dans certaines conditions. Ce ne sont
pas de vrais filaments mais des pseudo-filaments. Ces pseudo-filaments sont retrouvés seulement à l’état
pathogène dans les produits pathologiques. Notons que Candida est considérée comme une levure stricte car
elle ne donne pas des filaments mais des pseudo-filaments.
3. Champignons dimorphiques
Il existe seulement 6 champignons dimorphiques en pathologie humaine. Ce sont les agents des mycoses
exotiques. Ils existent sous deux formes : filamenteux et levure.

- Dans le milieu extérieur ils sont sous forme filamenteuse, c’est la forme végétative. La forme filamenteuse
est la forme infectante/contaminante, elle contient des conidies ou spores qui permettent aux champignons
dimorphiques de se répandre dans le milieu extérieur. Cette forme est obtenue en culture sur un milieu usuel,
à température ambiante ou 30°C. Très contaminant notamment par voie respiratoire, par inhalation.
- Dans les lésions humaines ou animales (chez un hôte), ils sont sous forme levure. Il s’agit de la forme
parasitaire. Cette forme est obtenue en culture sur des milieux spéciaux enrichis, à 37°C.
Chez les champignons dimorphiques, on ne retrouve jamais les deux formes (levure et filamenteux) en
même temps dans une lésion, contrairement aux levures comme Candida ou Malassezia où on peut avoir la
forme levure avec des pseudo-filaments (signe de pathogénicité chez la levure). Chez les dimorphiques,
lorsqu’on est en diagnostic dans une lésion on ne retrouve que la forme parasitaire levure.
Le dimorphisme est une adaptation morphologique à l’environnement qui leur permet de croître dans des
milieux et d’assimiler des nutriments plus variés, de supporter d'autres températures pour étendre sa capacité
à vivre et survivre que des champignons non dimorphiques. Par contre le dimorphisme les rend pathogènes.
Forme filamenteuse
(Dans la nature)
Forme levure
(Dans les tissus)
Pathogène
Exemple : penicillium marneffei ! Particularité : pigment rouge caractéristique.
Le penicillium se retrouve dans la nature, à température ambiante, on en utilise certains dans le roquefort.
Chez des patients infectés par un type de penicillium particulier (penicillium marneffei), sur gélose au
sang, milieu riche à 37°C, on retrouve une forme de levure. La forme levure se retrouve uniquement dans les
tissus. Le penicillium marneffei chez les patients VIH+ donne un taux de mortalité important.

Exemple : Histoplasmose
Dans l’environnement (surtout dans le sol) ou
en culture sur milieu non riche à température
ambiante, on retrouve la forme filamenteuse
avec des micro- et macroconidies (forme
mycélienne).
Chez un hôte, l’histoplasma adopte une forme
de levure (forme pathogénique). Il n’y a plus de
macroconidies mais une petite capsule, capable
de bourgeonnement.
II. Mycoses exotiques
Ou mycoses d’importation. Elles sont absentes en France métropolitaine (et souvent d’Europe sauf pour la
sporotrichose) mais présentes de façon endémique en zones inter-tropicales. Les champignons dimorphiques
sont des champignons telluriques, c'est-à-dire qui vivent dans le sol.
● Niches écologiques :
- Sol, grotte : ex : histoplasmose
- Végétaux : ex : sporotrichose
● Niches écologiques fréquentées par les voyageurs :
- Ex : Sud des Etats-Unis/grottes/histoplasmose
- Ex : Nord Thaïlande/forêt/pénicilliose (immunodéprimés +++)
● Activités à risque :
- Ex : spéléologues/histoplasmose
- Ex : sable, poussière/coccidioïdomycose
- Ex : travail en laboratoire
Les mycoses exotiques seront contractées par les voyageurs, les résidents à l’étranger, ou les migrants. Ce ne
sont pas que des agents de pathologies opportunistes, c’est-à-dire qu’ils ne surviennent pas que sur des
terrains spécifiques, sujets immunodéprimés ou VIH+ (plus sensibles aux infections) : ils infectent aussi des
sujets sains. Ce sont de vrais agents pathogènes qui peuvent infecter des sujets sains comme des sujets
immunodéprimés.
Il existe différents types de contaminations, les principales sont : inhalation, inoculation directe et
contamination de laboratoire.
On ne trouve pas ces champignons chez le sujet sain : il n'y a pas de colonisation. Il s'agit de pathogènes de
classe III, il faut être dans un laboratoire P3 pour les cultiver (avec SAS, pression d'air négative pour aspirer
l'air de la pièce).
- Contamination par inhalation
Conidies facilement dispersées et inhalées.
Primo-infection pulmonaire.
A noter que la particularité des spores est d'être très légère donc très présente dans l'air ambiant.

- Contamination par inoculation
Traumatisme, piqûre végétale (sporotrichose)
Mycose cutanée/sous cutanée
- Contamination de laboratoire, transplantation d’organe (certains sont des pathogènes de classe 3,
exemple : histoplasma). Les pathogènes de classe 3 sont extrêmement contagieux. ! QCM
- Pas ou très peu de transmission interhumaine
III. Mycoses liées aux champignons dimorphiques
Dans cette partie nous allons aborder différentes mycoses (à retenir les maladies et le nom des
champignons!) :
● Histoplasmose américaine, « à petites formes » (petite taille, 3 à 5μ), due à Histoplasma capsulatum var.
capsulatum.
● Histoplasmose africaine, « à grandes formes » (grande taille, 10 à 15μ), due à Histoplasma capsulatum
var. duboisii.
● Coccidioïdomycose, maladie de Posadas et Wernicke, due à Coccidioides immitis, le plus virulent des
champignons pathogènes.
● Paracoccidioïdomycose, blastomycose sud-américaine, due à Paracoccidioides brasiliensis.
● Blastomycose ou blastomycose nord-américaine, due à Blastomyces dermatitidis.
● Sporotrichose due à Sporothrix schenkii. Maladie cutanée, pathologie d’inoculation due aux végétaux
morts.
● Pénicilliose due à Penicillium marneffei. Pathologie très grave (surtout chez le sujet VIH +).
Les pathologies sont très fréquemment voire constamment mortelles sans traitements.
1. Histoplasmose Américaine :
Photo d’histoplasmose végétative : elle est sous forme
de filamenteuse. Les grosses boules représentent les
macroconidies et les petites boules les microconidies
qui sont directement sur les filaments. Et c’est ça qu’on
va respirer et qui va contaminer.
L’histoplasmose est très fréquente aux Etats-Unis,
principalement dans le bassin du
Mississipi et l’Ohio, mais on en trouve ailleurs (pas en
Europe).
Les études de séroprévalence (recherche des Ac)
montrent que 80% des individus ont rencontré H.
capsulatum dans le centre ouest des USA.
Chaque année 500 000 cas d’histoplasmose sont répertoriés aux USA alors qu’en France il n’y en a
quasiment aucun (pour un médecin français c’est une rareté).
Il existe deux autres zones d’endémie majeure :
- Amérique centrale et du Sud : 2ème mycose la plus fréquente en Amérique du Sud,
Guyane, Martinique, Guadeloupe, Caraïbe.
- Asie du Sud-est : Thaïlande, le long du Mékong.
H. capsulatum est un saprophyte, il vit dans les sols enrichis en fientes d’oiseaux (poulailler), et surtout de
chauves-souris (grottes, spéléologie).
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
1
/
15
100%