Bloc atrio-ventriculaire

295
CURRICULUM
Bloc atrio-ventriculaire
Causes, diagnostic et options thérapeutiques
Vanessa Weberndörfer, Hildegard Tanner
Rhythmologie und Elektrophysiologie, Universitätsklinik für Kardiologie, Inselspital, Bern, Schweiz
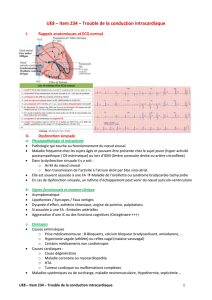
Causes
Dénitions
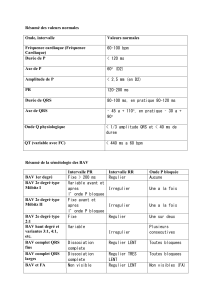
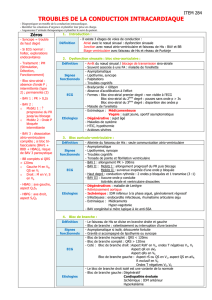
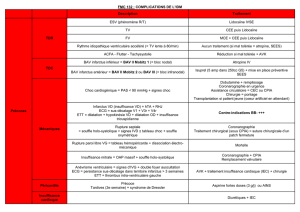
BAV du premier degré
BAV du second degré
BAV de type 1 (Wenkebach)
)
BAV de type 2 (Mobitz)
Quintessence
•
•
•
•
•
Abréviations
BAV = bloc atrio-ventriculaire
ESC = European Society of Cardiology
SNC = système nerveux central
TAVI = transcatheter aortic valve implantation
Forum Med Suisse 2014;14(14):295–299

CURRICULUM
Forum Med Suisse 2014;14(14):295–299 296
BAV 2:1 et BAV de haut degré
BAV complet
Anamnèse et manifestations cliniques
Ta bleau 1
Causes intrinsèques
Causes extrinsèques
Figure 1
Figure 2

CURRICULUM
Forum Med Suisse 2014;14(14):295–299 297
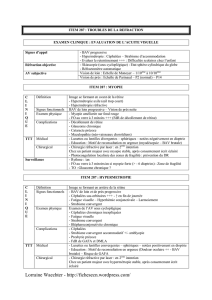
Examen électrophysiologique
Analyses biochimiques
B. burgdorferi
Tr aitement
Médicaments contre-indiqués
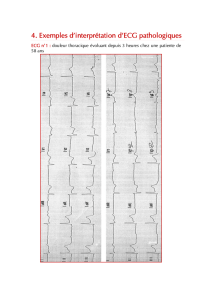
Figure 3
Figure 4
Ta bleau 2
Fréquence des symptômes Te chnique de surveillance ECG
Diagnostic
Documentation ECG

CURRICULUM
Forum Med Suisse 2014;14(14):295–299 298
Mesures
Indication pour l’implantation d’un stimulateur
cardiaque
Ta bleau 3
Ta bleau 4
traitement anti-VIH
antiémétiques
sclérose en plaques
paludisme
Ta bleau 5
Recommandations Classe d’indication Niveau de preuve
Ta bleau 6
Recommandations Classe d’indication Niveau de preuve

CURRICULUM
Forum Med Suisse 2014;14(14):295–299 299
Remerciements
Correspondance:
PD Dr Hildegard Ta nner
Oberärztin Rhythmologie und Elektrophysiologie
Universitätsklinik für Kardiologie
Inselspital
CH-3010 Bern
hildegard.tanner[at]insel.ch
Références
1
/
5
100%