LES TUMEURS STROMALES MALIGNES DU GRÊLE : À PROPOS

ARTICLE ORIGINAL
J Radiol 2001; 82 : 35-40
© Editions françaises de radiologie, Paris, 2001.
Article original
LES TUMEURS STROMALES MALIGNES DU GRÊLE :
À PROPOS DE 9 CAS
A Ousehal (1), A Abdelouafi (1), B Belaabidia (2), F Essodegui (1), B Kadiri (3) et R Kadiri (1)
ABSTRACT
Malignant stromal tumors of the small bowel: report of 9 cases
Purpose.
Analysis of imaging features of malignant stromal tumors of the small bowel and review of literature.
Material and Methods.
9 cases of malignant stromal tumor of the small bowel with histological proof were imaged at US
(8 cases), small bowel series (9 cases) and CT scan (3 cases).
Results.
There were 6 cases of leiomyosarcoma and 3 cases of malignant schwannoma. Tumors involved the jejunum in
3 patients, the ileum in 4 patients, and the duodenum in 2 patients. The main clinical presentation was an abdominal mass
(8 cases), which appeared heterogeneous and hypoechoic with eccentric lumen at US confirming its GI origin (7 cases).
Small bowel series showed a bulky cavitary mass opacified via a thin fistula (7 cases), an ileo-ileal intussusception (1 case)
and enlarged duodenal lumen (1 case). CT performed in 3 cases showed an intraperitoneal mass with soft-tissue density.
A communication with the GI tract was noted in 1 case, and in another case, it showed an intestinal intussusception. US
guided biopsy performed in 3 cases provided diagnosis in 2 cases (malignant schwannoma, leiomyosarcoma). Tumor
growth was exophytic in 8 cases and dumbbell-shaped in 1 case.
Conclusion.
The imaging features of malignant stromal tumors of the small bowel are similar. It varies with the type of
tumor growth and its size. The diagnosis may be suggested based on imaging features.
Key words:
Small Bowel. Stromal tumors. Leiomyosarcoma. Schwannoma, malignant. Ultrasound. CT. Imaging.
J Radiol 2001;82:35-40
RÉSUMÉ
But.
Analyse des aspects radiologiques des tumeurs stromales du grêle avec une revue de la littérature.
Matériel et méthodes.
Neuf cas de tumeur stromale du grêle confirmés histologiquement et explorés par échographie
(n = 8), transit du grêle (n = 9) et TDM (n = 3).
Résultats.
Il s’agit de 6 léiomyosarcomes et 3 schwannosarcomes. Le siège tumoral était jéjunal 3 fois, iléal 4 fois et duo-
dénal 2 fois. La découverte d’une masse abdominale a constitué la principale manifestation clinique (8 cas). La masse
abdominale était hypoéchogène, hétérogène et siège d’une bande hyperéchogène excentrée, confirmant sa nature diges-
tive dans 7 cas. Le transit du grêle a montré une volumineuse image cavitaire opacifiée progressivement par un fin pertuis
7 fois, une invagination intestinale iléo-iléale 1 fois et un élargissement du cadre duodénal une autre fois. La TDM réalisée
dans 3 cas a montré une masse intrapéritonéale de densité tissulaire. Une communication avec le tube digestif a été notée
dans un cas et l’aspect d’invagination intestinale dans un autre cas. La ponction biopsie échoguidée, réalisée dans 3 cas,
était concluante dans deux cas (schwannosarcome et léiomyosarcome). Le développement tumoral était exoluminal 8 fois
et en sablier 1 seule fois.
Conclusion.
L’aspect radiologique des tumeurs stromales du grêle est similaire. Elle dépend du développement de la
tumeur et de son volume. Le diagnostic peut être évoqué à l’imagerie.
Mots-clés :
Tumeurs conjonctives. Tumeurs stromales. Grêle. Léiomyosarcome. Schwannosarcome. Échographie. IDM.
Imagerie.
Les schwannosarcomes et les léiomyo-
sarcomes sont des tumeurs stromales à
cellules fusiformes. Les unes se dévelop-
pent à partir des plexus nerveux d’Auer-
bach de la paroi intestinale, les autres du
tissu musculaire lisse. Ces deux types de
tumeurs ont la même traduction clinique,
radiologique et macroscopique. L’aspect
histologique des formes indifférenciées
est similaire, imposant une étude im-
muno-histochimique (1, 2). Ces tumeurs
sont rares au niveau du grêle et excep-
tionnelles au niveau du côlon.
Leur développement longtemps asymp-
tomatique rend leur diagnostic tardif, à
un stade de tumeur volumineuse.
Le transit baryté était l’examen fonda-
mental dans la démarche diagnostique.
Actuellement, après l’échographie, la
TDM est l’examen de deuxième intention
qui permet de confirmer l’origine diges-
tive d’une masse abdominale.
Le but du travail est d’étudier les diffé-
rents aspects radiologiques à travers
une série de 9 cas de tumeurs conjonc-
tives du grêle et du duodénum.
MATÉRIEL ET MÉTHODES
Notre étude rétrospective a porté sur
9 cas de tumeur conjonctive du grêle et
du duodénum colligés sur une période
de 8 ans au service central de Radiolo-
gie CHU Ibn Rochd, tous opérés et
confirmés histologiquement. Il s’agissait
de 3 cas de schwannosarcome et 6 cas
de léiomyosarcome. Les lames ont été
revues par un pathologiste. Le diagnos-
tic a été retenu sur l’aspect histologique
et les résultats de l’immuno-histochimie
(actine muscle lisse, desmine, vimen-
tine, PS 100, CD 34).
(1) Service central de Radiologie, (2) Service d’Ana-
tomie Pathologique, (3) Service de Chirurgie Viscé-
rale I, CHU Ibn Rochd, Casablanca, Maroc.
Correspondance : A Ousehal
© 2014 Elsevier Masson SAS. Tous droits réservés. - Document téléchargé le 28/03/2014

36
A Ousehal et al. : Tumeurs malignes du grêle : à propos de 9 cas
J Radiol 2001; 82
Dans chaque cas, les éléments qui ont
été recherchés étaient : douleur abdo-
minale, hémorragie digestive, trouble du
transit, amaigrissement, taches café au
lait, masse abdominale.
Huit patients ont été explorés par une
échographie abdominale. Le transit du
grêle à la baryte, utilisant de grandes
quantités, orienté par les données de
l’échographie ou de la tomodensitomé-
trie, a été réalisé dans tous les cas.
Une tomodensitométrie abdominale a
été faite chez 3 patients avec un scan-
ner Philips LX. Les coupes ont été réa-
lisées après ingestion de Gastrogra-
fine
®
, sans et après injection de 100 ml
d’iode en bolus. L’épaisseur de coupe
était de 10 mm.
La ponction biopsie sous échographie
de la masse abdominale a été réalisée
chez 3 patients avec un trocard de 18 G
type Hepafix
®
.
RÉSULTATS
L’âge des patients variait entre 22 et
75 ans. La sex-ratio était égale à 5H/4F.
Le temps écoulé entre le début de la
symptomatologie et l’exploration radio-
logique variait entre 1 mois et 5 ans.
La découverte d’une masse abdominale
a constitué la principale manifestation
clinique. Elle a été retrouvée chez 7 pa-
tients. Une hémorragie digestive basse
bien tolérée a été notée chez 4 patients
à type de moelena 3 fois et de rectorra-
gie 1 seule fois. Le mode de révélation
était brutal chez un patient en occlusion
et présentant des douleurs abdominales
depuis un mois.
L’échographie abdominale réalisée chez
8 patients a rattaché la masse abdomi-
nale à une origine digestive dans 7 cas.
En raison d’un mode de début aigu, un
patient n’a pas pu bénéficier de l’écho-
graphie. L’aspect échographique rencon-
tré dans les 8 autres cas était celui d’une
formation hypoéchogène, hétérogène de
contours polylobés. Celle-ci était le siège
d’une bande hyperéchogène excentrée
7 fois
(fig. 1)
. Dans le dernier cas, l’écho-
graphie a montré une masse tissulaire se
projetant sur la tête du pancréas sans di-
latation des voies biliaires.
L’abdomen sans préparation a montré
des niveaux hydroaériques chez un pa-
tient en occlusion et une clarté anfrac-
tueuse chez un autre patient.
Le transit du grêle a été réalisé dans
9 cas. La localisation de la tumeur était
jéjunale 3 fois, iléale 4 fois et duodénale
2 fois. L’aspect radiologique réalisé était
celui d’une volumineuse image d’addition
dans 7 cas. Celle-ci était volumineuse,
sous forme d’une flaque de baryte à con-
tours anfractueux sans plissement mu-
queux individualisable en son sein
(fig. 2
et 3)
. Elle était opacifiée progressive-
ment par un fin pertuis à partir d’une
anse intestinale
(fig. 4)
. Elle était asso-
ciée à des images nodulaires en regard
de l’ulcération dans 1 cas de schwanno-
sarcome. À côté de cet aspect cavitaire,
le transit du grêle a montré également
une invagination intestinale iléo-iléale,
sans pouvoir préciser la cause dans un
cas (observation n
°
9) et un élargisse-
ment du cadre duodénal sans caractère
spécifique dans un autre cas (observa-
tion n
°
8).
La TDM, réalisée dans 3 cas, a montré
dans un cas une volumineuse masse
tissulaire polylobée, excavée, communi-
cante avec la lumière digestive (pas-
sage de gaz et de Gastrografine
®
en son
sein)
(fig. 5)
. Les parois de la masse
étaient très épaissies et nodulaires. La
TDM a objectivé chez le patient pré-
sentant une invagination intestinale, en
plus des signes d’invagination, une
masse tissulaire bilobée iléale de siège
intra et extraluminal
(fig. 6)
. Enfin, chez
le 3
e
patient, la TDM a montré une masse
se projetant en regard de la tête du pan-
créas, de densité hétérogène, sans re-
tentissement sur les voies biliaires et
pancréatiques, associée à un discret re-
maniement de la paroi du 3
e
duodénum
(fig. 7)
.
Une ponction biopsie échoguidée de la
masse a été réalisée chez 3 patients.
Elle a permis de faire le diagnostic d’un
cas de schwannome et un cas de léi-
myosacrome. Le matériel prélevé était
non représentatif dans l’autre cas, en rai-
son de la nécrose tumorale.
L’analyse macroscopique des pièces
d’exérèse opératoire a montré que le
développement tumoral était exoluminal
dans 8 cas et en sablier dans 1 cas.
Le
tableau I
regroupe l’ensemble des
observations.
DISCUSSION
Les léiomyosarcomes et les schwanno-
sarcomes sont des tumeurs conjoncti-
ves, les unes dérivent du tissu muscu-
laire lisse, les autres du tissu nerveux
(3, 4). Ces tumeurs peuvent toutes les
deux se développer dans la paroi du
tube digestif et avoir un siège sous-sé-
reux, sous-muqueux, intraluminal ou en
sablier (5-7).
Le léiomyosarcome représente 10 %
des tumeurs malignes de l’intestin grêle
(8, 9).
Les schwannosarcomes sont plus rares,
ne représentant que 0,2 à 0,6 % des tu-
meurs malignes du grêle (7, 10, 11).
L’âge de survenue est généralement si-
tué entre 45 et 60 ans (12). Le sexe
masculin est le plus touché dans la lit-
térature, comme c’était le cas dans no-
tre série.
Les léiomyosarcomes sont localisés fré-
quemment à l’iléon et constituent la tu-
meur la plus fréquente du diverticule de
Meckel (13-15). Les schwannosarco-
mes siègent par ordre de fréquence dé-
croissant dans le jéjuno-iléon, le duodé-
num et, enfin, l’estomac et le rectum
(16).
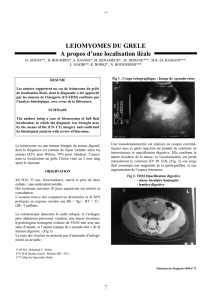
Fig. 1 : Femme de 55 ans. Léiomyosarcome du jéjunum.
L’échographie montre une volumineuse masse hypoéchogène de
contour polylobé, siège d’une bande hyperéchogène excentrée
(flèche).
Fig. 1:
55-year-old woman. Leiomyosarcoma of jejunum.
US shows a bulky hypoechoic mass with lobulated margins
containg an eccentric hyperechoic band (arrow).
© 2014 Elsevier Masson SAS. Tous droits réservés. - Document téléchargé le 28/03/2014

A Ousehal et al. : Tumeurs malignes du grêle : à propos de 9 cas
37
J Radiol 2001; 82
Fig. 2 : Femme de 22 ans. Schwannosarcome de l’iléon.
Le transit du grêle montre une image cavitaire de contour po-
lylobé, opacifiée par un fin pertuis à partir d’une anse iléale.
Fig. 2:
22-year-old woman. Malignant schwannoma of
ileum.
Small bowel series shows a cavitary mass with lobulated mar-
gins opacified via a thin fistula coming from the ileum.
Fig. 3 : Femme de 40 ans. Schwannosarcome de l’iléon.
Le transit du grêle montre une volumineuse image cavitaire
mesurant plus de 20 cm de grand axe de contour polylobé.
Fig. 3:
40-year-old woman. Malignant schwannoma of
ileum.
Small bowel series shows a large cavitary mass, over 20 cm
in diameter, with lobulated margins.
Fig. 4 : Femme de 55 ans. Léiomyosarcome du jéjunum.
Le transit du grêle montre une image d’addition opacifiée à partir
de la 2e anse jéjunale par un fin pertuis (flèche).
Fig. 4:
55-year-old woman. Malignant schwannoma of ileum.
Small bowel series shows a cavitary mass communicating with
the second jejunal loop via a thin fistula (arrow).
© 2014 Elsevier Masson SAS. Tous droits réservés. - Document téléchargé le 28/03/2014

38
A Ousehal et al. : Tumeurs malignes du grêle : à propos de 9 cas
J Radiol 2001; 82
Le diagnostic clinique est souvent tar-
dif, ce qui explique que la plupart de
ces tumeurs soient découvertes à un
stade avancé de masse abdominale (3,
17, 18).
L’hémorragie digestive est le signe clini-
que le plus fréquemment retrouvé (13,
19). Elle peut être très ancienne, inex-
pliquée pendant plusieurs années. La
découverte d’une masse abdominale
est retrouvée dans 40 % des cas (5, 6,
20).
L’abdomen sans préparation a un inté-
rêt très limité. Il peut montrer une opa-
cité de tonalité hydrique responsable
d’un refoulement des clartés digestives
(8). Les calcifications tumorales sont
trouvées surtout dans le léiomyosar-
come (5). Une clarté anfractueuse qui
ne ressemble à aucune structure diges-
tive peut être vue au sein de l’ulcération
Fig. 5 : Homme de 57 ans. Léiomyosarcome du duodénum.
a : Scanner sans injection d’iode et après ingestion de Gastrografine® : volumineuse formation tumorale largement nécrosée,
contaminée par l’air digestif et la Gastrografine® à paroi très épaisse.
b : Transit du grêle confirmant la nature digestive de la masse développée à partir du 2e duodénum et opacifiée par un fin pertuis
(flèche).
Fig. 5:
57-year-old-man. Leiomyosarcoma of duodenum.
a: CT scan, after intravenous and oral contrast administration. Bulky tumor with large necrotic area and thick wall, outlined by oral
contrast and bowel gas.
b: Small bowel series confirms the GI origin of the mass developed from the second duodenum and opacified via a thin fistula (arrow).
ab
Fig. 6 : Homme de 54 ans. Léiomyosarcome de l’iléon.
Le scanner montre une masse bilobée iléale avec une
composante endoluminale cernée par la Gastrografine® et une
composante exoluminale, découverte à la suite d’une invagi-
nation intestinale.
Fig. 6:
54-year-old-man. Leiomyosarcoma of ileum.
CT scan shows a bilobed ileal mass. Its endoluminal compo-
nent is outlined by oral contrast while its exophytic component
was visible only after ileal intussusception.
Fig. 7 : Homme de 71 ans. Léiomyosarcome du 3e duodénum.
Le scanner montre une volumineuse formation tissulaire bien
limitée siège de zone de nécrose.
Fig. 7:
71-year-old man. Leiomyosarcoma of 3rd stage of
duodenum.
CT scan shows a bulky well-defined soft tissue density mass
with necrotic areas.
© 2014 Elsevier Masson SAS. Tous droits réservés. - Document téléchargé le 28/03/2014

A Ousehal et al. : Tumeurs malignes du grêle : à propos de 9 cas
39
J Radiol 2001; 82
tumorale communicante avec la lumière
du tube digestif, comme c’était le cas
d’un patient dans notre série.
En échographie, les tumeurs conjoncti-
ves malignes du grêle déterminent le
plus souvent une volumineuse masse
tissulaire de contours polylobés, hypo-
échogène homogène ou hétérogène
(21-23). L’aspect échographique de la
masse est variable selon l’existence ou
non d’une communication avec la lu-
mière digestive. Ainsi, le centre de la
masse peut être liquidien en cas de né-
crose tumorale et hyperéchogène ex-
centré en cas de communication avec le
tube digestif (21). Cet aspect échogra-
phique les distingue des LMNH intesti-
naux, qui sont habituellement très
hypoéchogènes, voire anéchogènes.
L’échographie permet de faire le bilan
d’extension local et régional à la recher-
che de métastases. Elle permet égale-
ment de guider les ponctions biopsies
pour confirmer le diagnostic (15).
Le transit du grêle est l’examen fonda-
mental dans le diagnostic des tumeurs
conjonctives du grêle. Cependant, des
faux négatifs ont été rapportés dans la
littérature en raison du développement
sous-séreux de la tumeur (4, 19). La
sensibilité de l’examen est améliorée
par le double contraste. L’aspect radio-
logique varie en fonction de l’implanta-
tion tumorale dans la paroi et du degré
d’invasion des tuniques adjacentes à
partir de la couche d’origine (4, 10).
Lorsque la tumeur a un développement
intraluminal, ce qui est rare, elle se tra-
duit par une image lacunaire arrondie
bien limitée, recouverte par les plis de la
muqueuse. Ces plis sont étirés et parfois
légèrement effacés lorsque la tumeur est
Tableau I :
Fiche synoptique des observations.
Table I:
Summary of patient data.
Obs Âge/
Sexe Chirurgie Échographie TDM TG Anatomo-
pathologie
140
FRectorragie
Melæna
Masse
abdominale
Masse
digestive — Image
cavitaire
du jéjunum
Schwanno-
sarcome
222
FDouleur
abdominale
Melæna
Masse
abdominale
Taches café
au lait
Masse
digestive — Image
cavitaire de
l’iléon
Schwanno-
sarcome
365
HRectorragie
Dysurie
Masse
abdominale
Masse
digestive — Image
cavitaire
de l’iléon
Léiomyo-
sarcome
455
FDouleur
abdominale
Masse
abdominale
Masse
digestive — Image
cavitaire
du jéjunum
Léiomyo-
sarcome
573
HDouleur
abdominale
Masse
abdominale
Masse
digestive — Image
cavitaire
du duodénum
Schwanno-
sarcome
664
FDouleur
abdominale
Masse
abdominale
Masse
digestive Masse
digestive Image
cavitaire
de l’iléon
Léiomyo-
sarcome
757
HDouleur
abdominale
Melæna
Masse
abdominale
Masse
digestive Masse
digestive
nécrosée
du duodénum
Image
cavitaire
du duodénum
Léiomyo-
sarcome
871
HNodules
cutanées Masse
hypoéchogène
polylobée
polylobée
Masse
tissulaire
sur le
duodénum
Syndrome
de masse Léiomyo-
sarcome
954
HOcclusion — Invagination
surintestinale
tumeur
Invagination
intestinale Léiomyo-
sarcome
F : Femme ; H : Homme ; TG : Transit du grêle.
volumineuse (7, 15, 23, 24). Une tumeur
à développement exoluminal, réalise une
empreinte extrinsèque sur l’anse diges-
tive (4). Les tumeurs à développement
sous-muqueux ont tendance à effacer les
plis normaux et à éroder la muqueuse,
responsable ainsi d’une ulcération cen-
trale avec un profond cratère faisant com-
muniquer la tumeur avec la lumière di-
gestive (7, 9, 18, 24). Cette ulcération
explique les hémorragies digestives qui
inaugurent le plus souvent le tableau cli-
nique. Les tumeurs à développement ex-
traluminal sous-séreux, au stade de né-
crose tumorale, peuvent communiquer
avec le tube digestif, déterminant une fla-
que remplie de baryte, suspendue, com-
muniquant avec la lumière digestive par
un fin pertuis (25). Les parois de la flaque
sont en général épaissies et les plis mu-
queux en regard ont un aspect finement
nodulaire au niveau du raccordement de
la tumeur avec la lumière intestinale. Cet
aspect, rencontré dans 7 cas de notre
série, est considéré comme un signe très
évocateur.
Les tumeurs conjonctives du grêle se pré-
sentent en TDM comme une tumeur vo-
lumineuse à développement exoluminal
préférentiel, de contours polylobés, de
densité hétérogène avec des zones de
nécrose (13, 17). L’injection du contraste
par voie veineuse permet de rehausser
de façon nette les portions charnues hy-
pervasculaires et laisse un centre hypo-
dense (23, 26, 27). Cet aspect est consi-
déré comme caractéristique si la tumeur
se raccorde en pente douce avec l’anse
digestive correspondante. Une ulcération
profonde de la muqueuse digestive en re-
gard de la tumeur est fréquemment ren-
contrée (10). Sa contamination par la
Gastrografine
®
signe sa communication
avec la lumière digestive (13). Les calci-
fications tumorales sont parfois notées au
sein de la tumeur (5, 10, 26). Dans cer-
tains cas, la tumeur peut être totalement
nécrosée et apparaît comme une forma-
tion liquidienne pseudokystique à paroi
fine (17). La tomodensitométrie permet
aussi de faire un bilan d’extension local
et régional.
Le principal diagnostic différentiel d’une
tumeur maligne conjonctive du grêle est
le lymphome dans sa forme anévris-
male, qui se traduit par l’existence d’une
image cavitaire dont les caractéristiques
diffèrent des tumeurs conjonctives (17,
25). La cavité au cours du lymphome
malin non hodgkinien se trouve dans
l’axe de l’anse digestive et elle est sou-
vent associée à des anomalies du plis-
sement muqueux. L’échographie dans
le lymphome montre un épaississement
circonférentiel et symétrique de la paroi
de l’anse épaissie.
Le diagnostic de tumeurs conjonctives
du grêle est souvent tardif. L’aspect ra-
diologique observé est variable en fonc-
© 2014 Elsevier Masson SAS. Tous droits réservés. - Document téléchargé le 28/03/2014
 6
6
1
/
6
100%