la thromboprophylaxie chez les patients médicaux

-
Bulletin d’information Volume 11, no 3
Département de pharmacie du CSSS de Laval Octobre 2008
LA THROMBOPROPHYLAXIE CHEZ LES PATIENTS MÉDICAUX
Rédigé par : Josée Martineau, B. Pharm., M. Sc., BCPS et Marc-André Sauriol, B. Pharm., résident en pharmacie
Révision : Édith Gilbert, B. Pharm., M.Sc., BCPS et Stéphanie Caron, B. Pharm., M. Sc.
INTRODUCTION
Les patients hospitalisés pour diverses conditions médicales
peuvent présenter plusieurs facteurs de risque au dévelop-
pement d’une thromboembolie veineuse (TEV). Ce phéno-
mène, quoique bien connu, est parfois négligé lors de la
prestation de soins, particulièrement chez la population
médicale. On estime que l’utilisation de thromboprophylaxie
(TBP) varie de 15 à 45 % chez les patients médicaux à risque
élevé1. Nombreux sont les patients qui développent une TEV
quelques semaines à quelques mois après leur retour à la
maison et l’absence de TBP lors de leur hospitalisation en est
souvent la cause. L’héparine non fractionnée (HNF), les
héparines de faible poids moléculaire (HFPM) ainsi que les
méthodes mécaniques peuvent être utilisées pour la TBP.
SITUATION À L’HÔPITAL DE LA CITÉ-DE-LA-SANTÉ
Il existe peu de données québécoises documentant
l’utilisation de la TBP auprès des patients médicaux. Afin de
dresser un portrait de la situation locale actuelle, une éva-
luation par critères explicites a été menée à l’Hôpital de la
Cité-de-la-Santé en 2007 par Dr Martin Archambault2.
L’analyse des données a permis de constater que seulement
45 % des patients à risque de TEV recevaient une TBP. Il
s’agit d’une statistique préoccupante puisque 50 à 70 % des
thromboses symptomatiques et 70 à 80 % des EP mortelles
se produisent chez les patients médicaux3. On a attribué le
faible taux d’utilisation à l’oubli de l’évaluation systématique
du risque thromboembolique du patient. Le rapport a émis
quelques recommandations dont une portant sur la nécessité
de développer des méthodes visant à promouvoir l’usage
optimal de la TBP. Parallèlement, l’American College of
Chest Physicians, dans son dernier consensus, a émis une
recommandation de grade 1A encourageant l’instauration de
mesures actives visant à promouvoir l’usage de la TBP au
sein de tout centre de soins généraux. Dans cette optique, le
département de pharmacie a développé un programme de
TBP qui sera implanté sur les unités de médecine à partir de
cet automne.
LE PROGRAMME DE THROMBOPROPHYLAXIE
Ce programme implique divers éléments :
Un formulaire d’ordonnance préimprimé pour les unités
de médecine
Des séances de formation continue adressées au
personnel médical et pharmaceutique
Du matériel promotionnel tel un aide-mémoire plastifié
format de poche et affiches
Une équipe de résidents en pharmacie qui identifiera les
patients médicaux susceptibles de bénéficier d’une TBP
et abordera le sujet avec le médecin traitant
LA PROPHYLAXIE DE LA THROMBOEMBOLIE VEINEUSE
Généralités
Les TEV incluent plusieurs manifestations telles que la
thrombose veineuse profonde (TVP) des membres inférieurs
et supérieurs, l’embolie pulmonaire (EP) et d’autres rares
manifestations thromboemboliques viscérales comme la
thrombose des veines sus-hépatiques (syndrome de Budd-
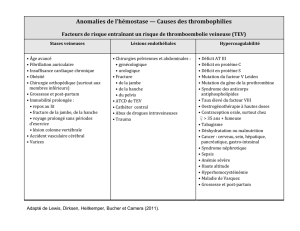
Chiari) ou la thrombose des veines cérébrales. La pathophy-
siologie d’une TEV repose sur plusieurs facteurs de risque
cardinaux dont les trois principaux ont été identifiés il y a plus
de 100 ans par Virchow (stase veineuse, hypercoagulabilité
et dommage endothélial)4,5. La stase veineuse est associée
à l’immobilisation prolongée, l’obésité, l’insuffisance
veineuse, l’hypovolémie, l’insuffisance cardiaque et les états
de choc. L’hypercoagulabilité peut être associée à des
facteurs héréditaires comme les déficiences en
antithrombine, en protéines C et S ou des polymorphismes
de facteurs de la coagulation (facteur V Leiden et mutation du
facteur II G20210A). Elle peut aussi être acquise dans le
cadre d’un cancer, d’un syndrome myéloprolifératif, du
syndrome antiphospholipide et même de façon paradoxale
suite au développement d’anticorps anti-héparine.
Finalement, le dommage endothélial peut être de nature
chimique ou chirurgicale.

-
L’American College of Chest Physician, dans son consensus
de 2008 (Chest 2008), recommande l’utilisation de la TBP
pharmacologique pour diminuer de façon significative les
événements thromboemboliques (grade 1A)3. Sans TBP,
l’incidence de TVP acquise en milieu hospitalier est approxi-
mativement 10 % à 40 % en soins médicaux. L’objectif prin-
cipal de la TBP est la réduction de la mortalité et de la mor-
bidité associée à l’embolie pulmonaire et secondairement, la
réduction de la TVP proximale de par son association étroite
avec l’incidence d’embolie pulmonaire et du syndrome
postphlébitique. En troisième lieu, la TBP permet aussi la
prévention de la TVP distale. Bien que celle-ci soit moins
importante sur le plan de la mortalité hospitalière, elle peut
cependant être associée à l’insuffisance veineuse chronique.
Identification des patients à risque de thromboembolie
veineuse
Les facteurs de risque de thrombose veineuse acquis et
congénitaux sont cumulatifs. Certaines thrombophilies
héréditaires prédisposent au développement de TEV. Entre
autres, la déficience en antithrombine et la mutation du fac-
teur V de Leiden ont été décrites comme des facteurs de
risque importants7. Le risque de TEV double à chaque
décennie chez les patients à partir de l’âge de 40 ans8.
L’immobilisation est fréquente autant durant le séjour hos-
pitalier qu’après le congé de l’hôpital et contribue de manière
importante au risque de TEV. Son impact, pris de façon
isolée, est difficile à établir compte tenu des comorbidités
associées et de la définition variable de ce facteur de risque.
L’obésité, définie par un indice de masse corporelle supé-
rieur à 30 kg/m2, augmente de 1,5 à 3 fois le risque de TEV9.
L’installation de cathéters veineux centraux est associée à
une augmentation du risque de TEV dans le réseau veineux
du cathéter, ce qui peut mener à des embolies pulmonaires10.
Par contre, la majorité des événements sont asymp-
tomatiques et de signification clinique incertaine. En ce qui
concerne l’hormonothérapie, les contraceptifs de deuxième
et de troisième génération augmentent respectivement le
risque de TEV de trois à quatre fois. Le risque est principale-
ment influencé par la durée d’utilisation et par la dose
d’oestrogène11. Chez les femmes recevant une
hormonothérapie substitutive, un risque de TEV quatre fois
supérieur a été observé. Une étude de cohorte population-
nelle mentionne que les maladies inflammatoires aigues
de l’intestin sont associées à un risque trois fois supérieur
de TVP et EP12. Une sous-analyse de l’étude MEDENOX
(The prophylaxis in medical patients with enoxaparin) a rap-
porté que l’incidence de TVP chez les patients hospitalisés
dans le cadre d’une infection sérieuse était de 15,5 %
lorsque aucune TBP n’était administrée13,14. Le syndrome
antiphospholipide se manifeste parfois par la présence
d’une thrombose veineuse ou artérielle ou par la présence de
morbidités obstétricales telles les pertes fœtales à répétition
ou la mort in utero. La thrombocytopénie induite par
l’héparine (TIH), peut contribuer au développement de TEV
de l’ordre de 36 % à 52 %15.
Les patients hospitalisés en soins médicaux sont à risque
de TEV de par les pathologies pour lesquelles ils sont traités.
L’infarctus du myocarde est associé à une incidence de
TEV pouvant aller jusqu’à 24 %, variable en fonction du
degré d’anticoagulation nécessaire pour traiter la pathologie
coronarienne3. Cette forte incidence est reliée au fait que les
patients sont plus âgés, immobilisés et qu’ils peuvent
développer de l’insuffisance cardiaque. De plus, l’obésité,
souvent présente chez ces patients, peut causer une stase
veineuse aux membres inférieurs3. L’insuffisance cardia-
que et respiratoire contribue également à l’augmentation du
risque thromboembolique16. Chez les patients en phase aiguë
d’AVC ne recevant pas de TBP, une analyse a montré que la
prévalence de TVP est de 53 % et celle d’EP de 6 %. Un
épisode passé de thromboembolie est considéré comme
étant un puissant facteur de risque de récurrence3. Le risque
de thrombose chez les patients atteints d’un cancer est sept
fois supérieur17. Ce risque augmente davantage en relation
avec les traitements chirurgicaux, radio-oncologiques,
chimiothérapeutiques ou hormonaux. Un cancer actif compte
pour 20 % des nouveaux épisodes de TEV diagnostiqués6.
La TEV est l’une des complications les plus fréquentes chez
les patients atteints de cancer et représente une problémati-
que particulière puisque ces patients sont également à risque
accru de saignement. Les sites tumoraux présentant les plus
grands risques de TEV sont le cerveau, l’ovaire, le pancréas,
le colon, l’estomac, les poumons, la prostate et le rein3,17.
Moyens mécaniques
Le but des méthodes mécaniques est de s’opposer à la
stase veineuse pour accélérer le flux sanguin dans les
membres inférieurs. Les moyens mécaniques actuellement
disponibles sont la contention élastique (bas de support) et la
compression pneumatique intermittente. Les moyens
mécaniques ont un effet additif au traitement antithromboti-
que justifiant leur emploi combiné dans certaines circonstan-
ces à très haut risque6. Lorsque l’utilisation des antithrombo-
tiques est contre-indiquée, ou que les risques hémorragiques
surpassent les bénéfices, la prévention par les moyens
mécaniques est parfois la seule alternative.
Mesures pharmacologiques
Les antithrombotiques sont employés dans le but de pré-
venir la formation de thrombus veineux ou à la limite d’en

-
limiter l’extension. Ils agissent au niveau des mécanismes de
l’hémostase, d’où leur potentiel hémorragique. Pour chaque
patient, il est important d’évaluer les bénéfices par rapport
aux risques. Les contre-indications à l’emploi d’un anti-
thrombotique sont : un saignement actif, un désordre de
coagulation majeur, un décompte plaquettaire inférieur à 50 x
109/L, un saignement intracrânien de moins de cinq jours, et
une TIH (pour l’HNF et les HFPM)3. Les principaux agents
thromboprophylactiques au formulaire de l’Hôpital de la Cité-
de-la-Santé sont l’HNF et l’énoxaparine. L’étude MEDENOX
a démontré chez les patients en soins médicaux qu’une TBP
avec l’énoxaparine 40 mg sous-cutané die est plus efficace
que le placebo en prévention de la TEV13. L’administration de
HNF tid serait plus efficace que l’administration bid mais
causerait plus de saignements18. Des évidences cliniques
suggèrent que les HFPM sont aussi efficaces que l’HNF tid
avec les avantages de causer moins de saignements, d’être
associées à une incidence moindre TIH et d’être plus écono-
miques15,19,20. De plus, le temps de demi-vie des HFPM étant
plus long, il est possible de les administrer une fois par jour
comparativement à l’HNF qui doit être donnée deux ou trois
fois par jour.
En ce qui concerne la durée de traitement, la TBP doit être
poursuivie jusqu’à une mobilisation adéquate ou jusqu’au
congé de l’hôpital. Pour les patients à plus haut risque, certai-
nes études ont montré une réduction supérieure de
l’incidence de TVP lorsque la TBP était prescrite pour 30
jours21. Une prophylaxie peut être suggérée au congé de
l’hôpital si le patient présente plusieurs facteurs de risque3.
L’utilisation de l’acide acétylsalicylique (AAS) et autres anti-
plaquettaires est préconisée lors d’événements vasculaires
majeurs ou de maladies athérosclérotiques, mais aucune
évidence ne suggère un bénéfice en TBP3.
La feuille d’ordonnance préimprimée de thrombopro-
phylaxie
L’ordonnance préimprimée a été conçue afin de faciliter la
prescription TBP. Vous remarquerez deux éléments impor-
tants :
1. L’absence d’HNF : l’énoxaparine sera préconisée pour
les raisons mentionnées précédemment.
2. La présence de deux posologies d’énoxaparine : 40 mg
s.c. die et 30 mg s.c. die pour les patients ayant une clai-
rance de la créatinine inférieure à 30 mL/min.
CONCLUSION
La TEV est une complication fréquente chez les patients
hospitalisés pour des soins médicaux et elle est facilement
évitable si des mesures sont instaurées pour en diminuer le
risque. Le tout implique une évaluation du patient dès son
hospitalisation et l’application des mesures prophylactiques
lorsqu’il y a présence de facteurs de risque. La décision
d’initier une TBP doit aussi tenir compte des contre-indica-
tions possibles et de la fonction rénale du patient. L’emploi
des méthodes mécaniques comme seul moyen de TBP
devrait être considéré uniquement en présence d’une contre-
indication à l’utilisation des agents recommandés. Enfin, nous
croyons que le programme implanté par le département de
pharmacie cet automne permettra d’optimiser l’usage de TBP
chez les patients médicaux et nous espérons que la
démarche clinique de l’évaluation systématique du risque
thromboembolique perdure une fois le projet terminé.

-
RÉFÉRENCES
1. Kahn S, Panju A, Geerts W. et coll. Multicenter Evaluation of
the Use of Venous Thromboembolism Prophylaxis in Acutely
Ill Medical Patients in Canada. Thromb Res 2007; 119(2):146-
154.
2. Archambault M. Comité d’évaluation de l’acte médical du
département de médecine générale et familiale : Prophylaxie
des maladies thromboemboliques. CSSS de Laval 2007 (rap-
port interne).
3. Geerts W, Bergqvist D, Pineo G et coll. Prevention of Venous
Thromboembolism: American College of Chest Physicians
Evidence-Based Clinical Practice Guidelines (8th Edition).
Chest 2008; 133:381-453.
4. Dickson BC. Venous thrombosis: on the history of Virchow’s
triad. UTMJ. 2004; 81:166-171.
5. Virchow R. Neuer fall von todlichen. Emboli der lungenarteri.
Arch Pathol Anat. 1856; 10:225-8.
6. Anderson FA Jr, Wheeler HB. Venous thromboembolism: risk
factors and prophylaxis. Clin Chest Med 1995; 16:235-51.
7. Bick RL. Hypercoagulability and thrombosis. Med Clin North
Am 1994; 78:635-65.
8. Anderson FA Jr, Wheeler HB, Goldberg RJ et coll. A popula-
tion based perspective of the hospital incidence and case-
fatality rates of deep vein thrombosis and pulmonary
embolism. The Worschester DVT Study. Arch Intern Med
1991; 151:933-8.
9. Samama MM. An epidemiologic study of risk factors for deep
vein thrombosis in medical outpatients: The Sirius study. Arch
Int Med 2000; 160:3415-20.
10. Bern MM, Lokich JJ, Wallach SR et coll. Very low doses of
warfarin can prevent thrombosis in central venous catheters. A
randomized prospective trial. Ann Intern Med 1990; 112:423-8.
11. Lidegaard O, Edstrom B, Kreiner S. Oral contraceptives and
venous thromboembolism: A five-year national case-control
study. Contraception.2002; 65:187-196.
12. Bernstein CN, Blanchard JF, Houston DS et coll. The
incidence of deep venous thrombosis and pulmonary
embolism among patients with inflammatory bowel disease: A
population-based cohort study. Thromb Haemost 2001;
85:430-4.
13. Samama MM, Cohen AT, Damon JY et coll. A comparison of
enoxaparin with placebo for the prevention of venous
thromboembolism in acutely ill medical patients. NEJM 1999;
341:793-800.
14. Alikhan R, Cohen AT, Combe S et coll. MEDENOX Study.
Risk factors for venous thromboembolism in hospitalized
patients with acute medical illness: analysis of the MEDENOX
Study. Arch Intern Med 2004; 164: 963–8.
15. Warkentin TE. Think of HIT. Hematology 2006; 1: 408.
16. Kleber FX, Witt C, Vogel G et coll. Randomized comparison of
enoxaparin with unfractionated heparin for the prevention of
venous thromboembolism in medical patients with heart failure
or severe respiratory disease. AHJ 2003; 145 : 614-21.
17. Heit JA, Silverstein MD, Mohr DH et coll. Risk factors for deep
vein thrombosis and pulmonary embolism: A population-based
case-control Study. Arch Intern Med 2000; 160:809-15.
18. King C, Holley A, Jackson J et coll. Twice vs Three Times
Daily Heparin Dosing for Thromboembolism Prophylaxis in the
General Medical Population: A Metaanalysis. Chest 2007;
131:507-1.
19. Bergmann JF, Neuhart E. A multicenter randomized double-
blind study of enoxaparin compared with unfractionated
heparin in the prevention of venous thromboembolic disease
in elderly in-patients bedridden for an acute medical illness.
Thromb Haemost. 1996; 76:529-34.
20. Hirsh J, Raschke R. Heparin and low-molecular-weight
heparin. Chest. 2004; 126:188S-203S.
21. Hull RD, Schellong SM, Tapson VF et coll. Extended-duration
venous thromboembolism prophylaxis in acutely ill medical
patients with recent reduced mobility: The EXCLAIM study.
2007 Congress of the International Society on Thrombosis and
Hemostasis; July 7-13, 2007; Geneva, Switzerland. Late-
breaking clinical trials, abstract O-S-001.

-
62-1200-022 ORDONNANCES – THROMBOPROPHYLAXIE MÉDICALE 1 de 1
Date : 2008-09-29
DOSSIER MÉDICAL Copie jaune : Pharmacie Copie rose : Unité de soins
ORDONNANCES
THROMBOPROPHYLAXIE MÉDICALE
CRITÈRES D’UTILISATION :
Insuffisance cardiaque décompensée
OU
Insuffisance respiratoire aiguë
OU
Durée d’alitement prévue ≥ 3 jours ET au moins un des critères suivants :
Antécédent de thromboembolie
Septicémie
Maladie inflammatoire de l’intestin
Cancer actif et/ou ses traitements (hormonothérapie, chimiothérapie et radiothérapie)
Maladie neurologique aiguë (ex. : sclérose en plaques, syndrome de Guillain-Barré, AVC, etc.)
D’autres facteurs peuvent être considérés lors de l’évaluation du risque thrombotique (cf. verso)
CRITÈRES D’EXCLUSION :
Présence de coagulopathie ou de saignement actif
Patient recevant un anticoagulant oral
Patient sous héparine ou HFPM à dose thérapeutique
Antécédent de thrombocytopénie induite par l’héparine
Décompte plaquettaire inférieur à 50 x 109/L
POSOLOGIE :
Énoxaparine (LovenoxMD) 40 mg s.c. die
Énoxaparine (LovenoxMD) 30 mg s.c. die si Clcr < 30 mL/min
Poursuivre la thromboprophylaxie ad mobilisation ou jusqu’au congé pour certains patients à haut risque.
RAPPEL :
1. Favoriser la mobilisation précoce lorsque possible.
2. Si patient à haut risque de saignement, favoriser les moyens mécaniques.
3. Si présence d’un cathéter épidural toujours aviser l’anesthésiste.
Date : ______________ Heure : _____________ Signature : _____________________________________ No de permis : ______________
 6
6
1
/
6
100%