Rappel : parameters cinétiques

Rappel : paramètres cinétiques
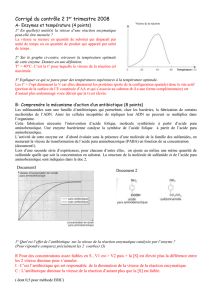
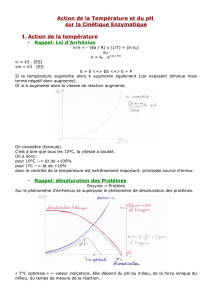
Les réactions enzymatiques obéissent à l’équation de Michaelis-Menten
k1 k2
E + S
⇌
ES
Æ
E + P
k-1
][
][
max
0
S
M
K
SV
v
+
=
][
max EkV cat
= 2
k
cat
k
=
1
)( 21
k
kk
M
K
+
=−
kcat : vitesse de renouvellement (« turnover number »)
- le nombre de molécules de substrat transformées en produit par unité de temps et par
site actif, lorsque l’enzyme est saturé par le substrat
KM : constante de Michaelis-Menten
- concentration en substrat où v0 = ½ Vmax
- caractérise l’interaction de l’enzyme avec un substrat donné
- KM = constante de dissociation du complexe ES lorsque l’équilibre entre (E + S) et
ES est rapide (k-1 >> k2)
kcat/KM : constante de spécificité
Indicateur de l’efficacité catalytique de l’enzyme envers un substrat donné
BCM 2504 Cinétique et mécanisme des protéases Page 1.8

Application => mécanisme à 3 étapes
Pour expliquer la cinétique « bi phasique » observée lors de l’hydrolyse du p-nitrophényl acétate
par la chymotrypsine, il faut faire intervenir un intermédiaire supplémentaire où le substrat forme
un lien covalent avec l’enzyme durant la réaction.
k2 = constante de vitesse d’acylation
k3 = constante de vitesse de déacylation
Équation complète décrivant la libération du p-nitrophénolate lors de l’hydrolyse du PNPA :
BCM 2504 Cinétique et mécanisme des protéases Page 1.9

A. Implication de Ser195
L’enzyme acétylée (Enz-CO-CH3) est stable à faible pH et a pu être isolée. Une analyse d’acides
aminés a permis de découvrir que le groupement acétyl était lié à la sérine 195.
Utilisation du diisopropylfluorophosphate (DFP)
La chymotrypsine contient 27 résidus sérine mais un seul, le résidu 195, réagit avec le DFP. De
même, le DFP inactive les autres protéines à sérine en faisant également une liaison covalente
avec la sérine active (attaque nucléophile).
Le fluorure de phénylméthanesulfonyl (PMSF) peut aussi être utilisé à cette fin.
BCM 2504 Cinétique et mécanisme des protéases Page 1.10

B. Implication de His57
Utilisation du N-tosyl-L-phénylalanylchlorométhylcétone (TPCK)
Les marqueurs d’affinité ont des structures semblables à celles des substrats naturels, mais
réagissent d’une manière irréversible avec l’enzyme.
La chymotrypsine est inactivée par le N-tosyl-L-phénylalanylchlorométhylcétone (TPCK). Ce
réactif est pourvu d’un groupe aromatique qui peut s’ajuster au site de spécificité de l’enzyme.
Un groupement nucléophile du site actif (His57) peut alors attaquer le groupement
chlorométhylcétone du TPCK. Il s’agit d’une inhibition irréversible compétitive, car l’addition
de substrat protège l’enzyme contre l’inhibition et le marquage. Le mécanisme détaillé implique
possiblement une réaction avec Ser195 pour former un intermédiaire réactionnel.
N-Tosyl L- phenylalanyl Alkylated derivative of
chloromethyl ketone hystidine 57 at active site of chymotrypsin
(inactive)
BCM 2504 Cinétique et mécanisme des protéases Page 1.11

C. Existence d’une triade catalytique
C’est la résolution cristallographique de la structure tertiaire de la chymotrypsine par diffraction
aux rayons X qui a permis de situer le noyau imidazole de l’His57 à environ 3.8 Ǻ de la Ser195.
À proximité de l’His57 on trouve également le groupe carboxylate de l’Asp 102 situé à 2.8 Ǻ du
groupe imidazole. La conformation de ces trois résidus est stabilisée par une série de liaisons
hydrogène.
Ce réseau de liaisons hydrogène augmente le caractère nucléophile de la Ser195 dont dépend
l’activité de l’enzyme.
Le rôle de l’Asp102 a été vérifié par mutagénèse dirigée. On a remplacé l’Asp102 par un résidu
isostérique non chargé : l’Asn. Le mutant Asp102Asn a des propriétés cinétiques qui diffèrent
largement de celles de l’enzyme sauvage. Son KM n’est pas très différent mais le paramètre kcat
se trouve diminué d’un facteur de 5000. Il est donc clair que le résidu Asp102 est important pour
la catalyse enzymatique, mais pas absolument nécessaire.
Dans le cas du mutant Asp102Asn, le pKa de l’His57 est abaissé de 1.5 unités de pH. Ceci
souligne l’importance du microenvironnement d’un résidu ionisant quant à la valeur de son pKa.
Le mutant Asp102Asn réagit 10000 fois moins vite avec le DFP que l’enzyme sauvage, et 10
fois moins vite avec le RLCK. La nucléophilicité de la Ser195 est donc nettement diminuée, par
contre, la réactivité de l’His57 semble moins affectée pour la réaction avec le TLCK. L’effet
principal de la mutation de l’Asp102 se situe au niveau de la réactivité de la Ser195 qui confère à
la Ser195 son caractère nucléophile élevé.
BCM 2504 Cinétique et mécanisme des protéases Page 1.12
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
1
/
11
100%