MANIFESTATIONS THORACIQUES DU CANCER DU SEIN TRAITE

MANIFESTATIONS
THORACIQUES DU CANCER DU
SEIN TRAITE

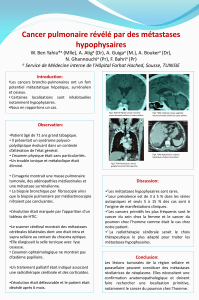
INTRODUCTION
La TDM est l’examen de choix pour le suivi d’un
cancer du sein traité
Les lésions thoraciques découvertes sont
fréquentes et très variées.
Elles peuvent correspondre à des complications
réversibles, définitives, à des récidives
locorégionales ou métastases.

OBJECTIFS PEDAGOGIQUES
Connaître les modifications de la paroi
thoracique après traitement chirurgical du
cancer du sein.
Connaître les complications thoraciques des
différentes modalités thérapeutiques.
Reconnaître les signes de récidives
locorégionales et de métastases thoraciques.

Modifications de la paroi thoracique après
chirurgie du cancer du sein
Mastectomie radicale:
Ablation de la glande mammaire + muscles pectoraux +
curage axillaire jusqu’au niveau du ligament osto-
claviculaire + /- curage de la chaine mammaire interne
Pas de supériorité prouvée sur survie sans récidive vs
morbidité élevée
Mastectomie radicale modifiée:
Pathey: laisse en place le muscle grand pectoral et
enlève le petit pectoral atrophie du grand pectoral
par lésion du nerf pectoral latéral

•Auchinclloss: laisse les 2 muscles en place: car seul
2 % des patients auront besoin d’un curage
ganglionnaire axillaire apical, non accessible sans
ouverture ou résection du muscle petit pectoral
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
1
/
28
100%