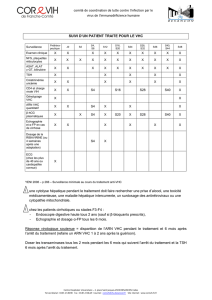
Nouvelles-éclair sur la santé

Nouvelles-éclair sur la santé
Bulletin trimestriel
Page 1 sur 10 | 4e TRIMESTRE DE 2014
Le Comité d’évaluation des médicaments examine les nouveaux médicaments
et les agents à surveiller au cours des réunions d’octobre à décembre 2014
Le Comité d’évaluation des médicaments (CEM) d’Express Scripts Canada revoit chaque mois tous les avis de conformité
émis par Santé Canada pour les nouveaux médicaments. Le CEM s’assure ainsi de leur rôle thérapeutique et vérifie leurs
répercussions sur le secteur privé. Les prix indiqués dans le présent document sont approximatifs et sont fournis uniquement
à titre d’information générale; ils ne sont pas destinés à servir de référence fiable aux fins de traitement des demandes de
règlement ni aux fins de remboursement des médicaments. Nous présentons ce bulletin trimestriel à nos clients à titre de
service à valeur ajoutée et espérons qu’ils le jugeront instructif, pertinent et utile.
NOUVEAUX MÉDICAMENTS
Duavive (acétate de bazédoxifène et œstrogènes conjugués)
Présentation DIN et concentration Fabricant Classe AHFS
Comprimés 02432854 – 20 mg/0,4 mg Pfizer Canada Inc. 68:16.12 – Agonistes et
antagonistes des estrogènes
Notes cliniques
Duavive est un produit d’association à dose fixe combinant des œstrogènes conjugués et du bazédoxifène. Les œstrogènes conjugués sont un
mélange de plusieurs œstrogènes d’origine équine qui comprennent notamment des conjugués de sulfate d’œstrone sodique, de sulfate d’équiline
sodique et de sulfate sodique. Le bazédoxifène est un modulateur sélectif des récepteurs d’œstrogènes qui possède une sélectivité tissulaire et
exerce des effets agonistes et antagonistes sur ces récepteurs au niveau de divers organes.
L’œstrogène non compensé augmente le risque de cancer de l’endomètre chez les femmes qui ont un utérus. À l’heure actuelle, les progestines
représentent le seul traitement approuvé en appoint à l’œstrogénothérapie pour réduire le risque d’hyperplasie de l’endomètre, qui peut être
à l’origine d’un cancer de l’endomètre. Duavive est le premier médicament qui utilise un agent autre qu’une progestine, le bazédoxifène, pour
atténuer les effets proliférants de l’œstrogène dans l’utérus. Les effets anti-œstrogéniques du bazédoxifène dans le tissu mammaire pourraient
potentiellement protéger ce tissu contre le cancer.
Place dans le traitement
Duavive offre une alternative thérapeutique contre l’ostéoporose, les symptômes vasomoteurs et d’autres symptômes liés à la ménopause.
Il pourrait réduire les risques chez les femmes susceptibles de présenter un carcinome du sein ou de l’endomètre.
Indication(s)
*La version canadienne de la monographie du produit n’est
pas disponible; les renseignements sont tirés de l’information
posologique approuvée par la FDA pour Duavee.*
Chez les femmes qui ont un utérus :
• traitement des symptômes vasomoteurs modérés à sévères
associés à la ménopause;
• prévention de l’ostéoporose chez les femmes ménopausées.
Posologie
Un comprimé une fois par jour.
Autres options de traitement
Premarin + Evista (raloxifène)*
*produits génériques offerts

Nouvelles-éclair sur la santé
Bulletin trimestriel
Page 2 sur 10 | 4e TRIMESTRE DE 2014
Le Comité d’évaluation des médicaments examine les nouveaux médicaments
et les agents à surveiller au cours des réunions d’octobre à décembre 2014
Prix comparatifs
Médicament Coût annuel estimatif
Duavive prix non disponible
Premarin®120 $
PMS-Raloxifene 170 $
Répercussions / Suggestions pour la gestion des régimes
Renseignements insuffisants.

Nouvelles-éclair sur la santé
Bulletin trimestriel
Page 3 sur 10 | 4e TRIMESTRE DE 2014
Le Comité d’évaluation des médicaments examine les nouveaux médicaments
et les agents à surveiller au cours des réunions d’octobre à décembre 2014
DymistaMC (chlorhydrate d’azélastine et propionate de fluticasone)
Présentation DIN et concentration Fabricant Classe AHFS
Pulvérisation à dose mesurée 02432854 – 137 µg/50 µg Meda Pharmaceuticals Ltd. 52:08.00 – Anti-inflammatoires
O.R.L.O.
Notes cliniques
La pulvérisation nasale Dymista contient à la fois du chlorhydrate d’azélastine (un antagoniste des récepteurs de l’histamine H1) et du propionate
de fluticasone (un corticostéroïde synthétique).
Le chlorhydrate d’azélastine a fait preuve d’un effet antagoniste sur les récepteurs de l’histamine H1 dans des tissus isolés, chez des modèles
animaux et chez l’humain.
Le propionate de fluticasone est un corticostéroïde trifluoré de synthèse possédant une activité anti-inflammatoire. Le mécanisme précis par
lequel le propionate de fluticasone atténue les symptômes de la rhinite allergique n’est pas connu. Il a été démontré que les corticostéroïdes
exercent une grande variété d'effets sur plusieurs types de cellules (p. ex., mastocytes, éosinophiles, neutrophiles, macrophages et lymphocytes)
et plusieurs médiateurs (p. ex., histamine, éicosanoides, leucotriènes et cytokines) impliqués dans le processus inflammatoire.
Place dans le traitement
Dymista est un produit d’association à dose fixe combinant un antihistaminique H1 et un corticostéroïde sous forme de vaporisation nasale.
Il offre une nouvelle option thérapeutique dans les cas où ces deux types de médicaments sont nécessaires pour le traitement de la rhinite
allergique saisonnière.
Prix comparatifs
Indication(s)
Pour le traitement symptomatique de la rhinite allergique
saisonnière (RAS) modérée à sévère et le traitement des
symptômes oculaires connexes chez les adultes et les
adolescents de 12 ans et plus lorsque la monothérapie
par antihistaminiques ou par corticostéroïdes intranasaux
n’est pas considérée comme suffisante.
Posologie
Une pulvérisation dans
chaque narine deux fois
par jour.
Autres options de traitement
Antihistaminiques intranasaux : vaporisant
nasal Livostin (lévocabastine)
Corticostéroïdes intranasaux : béclométhasone;
budésonide; Omnaris (ciclésonide); flunisolide;
propionate de fluticasone; Avamys (furoate
de fluticasone); mométasone; Nasacort AQ
(triamcinolone)
Médicament Coût par part
DymistaMC, pulvérisation nasale prix non disponible
Livostin®, vaporisant nasal 28 $ par flacon de 15 ml
Apo-Fluticasone, vaporisateur nasal 22 $ par flacon de 120 doses
Répercussions / Suggestions pour la gestion des régimes
Renseignements insuffisants.

Nouvelles-éclair sur la santé
Bulletin trimestriel
Page 4 sur 10 | 4e TRIMESTRE DE 2014
Le Comité d’évaluation des médicaments examine les nouveaux médicaments
et les agents à surveiller au cours des réunions d’octobre à décembre 2014
GazyvaTM (obinutuzumab)
Présentation DIN et concentration Fabricant Classe AHFS
Injection intraveineuse 02434806 – 25 mg/mL Hoffmann La Roche Ltée 10:00.00 – Antinéoplasiques
Notes cliniques
La leucémie lymphoïde chronique (LLC) compte parmi les troubles lymphoprolifératifs chroniques (néoplasmes lymphoïdes). Elle se caractérise
par une accumulation progressive de lymphocytes habituellement monoclonaux et non fonctionnels.
L’obinutuzumab est un anticorps monoclonal humanisé recombinant anti-CD20 de type II (isotype IgG1) modifié par glyco-ingénierie. Il cible
spécifiquement la boucle extracellulaire de l’antigène transmembranaire CD20 qui est exprimé à la surface des lymphocytes B matures et
précurseurs des lymphocytes B malins et non malins, mais pas sur les cellules souches hématopoïétiques, les prolymphocytes B, les plasmocytes
normaux et les autres tissus sains.
Place dans le traitement
Gazyva offre une nouvelle option thérapeutique pour les patients atteints de LLC non traitée auparavant et a été associé à une amélioration de la
survie sans progression par rapport aux traitements existants.
Prix
Indication(s)
Traitement de la leucémie lymphoïde
chronique (LLC) non traitée auparavant,
en association avec le chlorambucil.
Posologie
Cycle 1 : 100 mg au 1er jour, 900 mg au
2e jour, puis deux doses hebdomadaires de
1000 mg (jours 8 et 15)
Cycles 2 à 6 : 1000 mg au 1er jour de chaque
période de 28 jours (total de 5 doses)
Autres options de traitement
Associations fludarabine-
cyclophosphamide-rituximab, fludarabine-
rituximab et rituximab-chlorambucil.
Médicaments Coût estimatif du traitement*
GazyvaTM 45 000 $
fludarabine/cyclophosphamide/rituximab 26 000 $
*6 cycles
Répercussions / Suggestions pour la gestion des régimes
Répercussions moyennes. Nous recommandons l’autorisation préalable pour s’assurer que ce médicament est utilisé de façon appropriée.

Nouvelles-éclair sur la santé
Bulletin trimestriel
Page 5 sur 10 | 4e TRIMESTRE DE 2014
Le Comité d’évaluation des médicaments examine les nouveaux médicaments
et les agents à surveiller au cours des réunions d’octobre à décembre 2014
HarvoniMC (lédipasvir-sofosbuvir)
Présentation DIN et concentration Fabricant Classe AHFS
Comprimés 02432226 – Lédipasvir (90 mg)
et sofosbuvir (400 mg) Gilead Sciences Canada 08:18.32 – Analogues des
nucléosides et des nucléotides
Notes cliniques
L’infection aiguë par le virus de l’hépatite C (VHC) désigne la présence de signes ou symptômes cliniques d’hépatite C pendant les six mois qui
suivent l’exposition présumée au virus. On parle d’infection chronique en cas de présence prolongée du VHC. L’exposition par voie parentérale
constitue le mode de transmission le plus efficace du VHC. Le but du traitement est l’éradication de l’ARN du VHC, qu’il est possible de prévoir
si on obtient une réponse virologique soutenue (RVS), qui est définie par l’absence d’ARN du VHC confirmée par une réaction en chaîne de la
polymérase pendant trois à six mois après l’arrêt du traitement. L’obtention d’une RVS est associée à une probabilité d’absence d’ARN du VHC
de 99 % lors du suivi à long terme et permet donc de considérer que l’infection par le VHC est guérie.
Harvoni contient deux inhibiteurs de la réplication du VHC. Le lédipasvir est un antiviral à action directe qui inhibe la réplication de l’ARN du
VHC et la production de virions en ciblant la protéine NS5A du VHC. On croit que la protéine NS5A joue plusieurs rôles dans la médiation de
la réplication virale, les interactions avec les cellules hôtes et la pathogenèse virale. Le sofosbuvir est un inhibiteur pan-génotypique de l’ARN
polymérase ARN-dépendante (ADAP) NS5B du VHC. La NS5B est la sous-unité initiatrice et catalytique essentielle du complexe multiprotéique
membranaire nécessaire à la réplication de l’ARN du VHC et joue un rôle crucial dans le cycle de réplication virale.
La réponse virologique soutenue (RVS) était le principal paramètre évalué pour déterminer la guérison de l’infection par le VHC, qui était définie
par l’atteinte d’un taux d’ARN du VHC inférieur à la limite inférieure de quantification (LIQ) à 12 semaines après l’arrêt du traitement. Le taux de
RVS12 (c.-à-d. la proportion de sujets dont l’infection par le VHC était guérie12 semaines après l’arrêt du traitement) a varié de 94 % à 99 %.
Place dans le traitement
L’association lédipasvir-sofosbuvir offre une option de traitement contre l’infection chronique par le VHC, en particulier lorsque les médicaments
à base d’interféron ou de ribavirine ne peuvent pas être utilisés en raison d’une intolérance ou après l’échec de traitements antérieurs par ces
médicaments ou par des inhibiteurs de la protéase. En outre, les taux de guérison élevés jouent en faveur de son utilisation comme traitement de
première intention chez les patients jamais traités auparavant.
Indication(s)
Pour le traitement d’une
infection chronique par le virus
de l’hépatite C de génotype 1
chez l’adulte.
Posologie
Un comprimé une fois par jour. La durée du traitement peut
être de 12 ou 24 semaines selon que le patient a déjà suivi
ou non un traitement et selon la présence ou l’absence de
cirrhose. Un traitement de 8 semaines peut être envisagé
chez les patients n’ayant jamais suivi de traitement, ne
souffrant pas de cirrhose et ayant un taux d’ARN du VHC
inférieur à 6 millions d’UI/ml avant le début du traitement.
Autres options de traitement
Sofosbuvir (Sovaldi) en association
avec le peginterféron et la ribavirine;
siméprévir (Galexos) en association
avec le peginterféron et la ribavirine.
 6
6
 7
7
 8
8
 9
9
 10
10
1
/
10
100%