Eau pH1

Généralités 2
Extraction
Coefficient de Partage KP
Coefficient de Distribution KD
1

G2 Extraction définitions
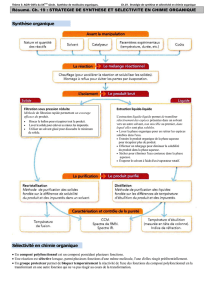
Le café est le produit d’une extraction liquide-
solide de café moulu.
La vinaigrette est un mélange biphasique dans
lequel le sel est extrait dans la phase aqueuse,
le vinaigre.
Une anesthésie est une extraction gaz-liquide:
l’anesthésique inhalé est extrait dans le sang
2

L’extraction d’un produit d’un solvant A dans un solvant B a
lieu entre deux solvants non miscibles.
En règle générale, il s’agit d’une phase aqueuse et d’une
phase organique.
La phase aqueuse peut être d’acidité variable (pH 1 à 14)
Il y a de nombreux solvants organique pouvant servir de
phase organique à condition de ne pas être miscible à
l’eau!
3
G2 Extraction définitions

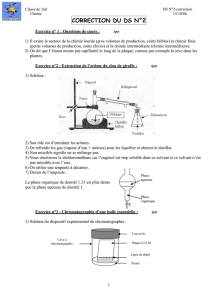
1) Où est quel phase?
A: le premier solvant présent dans
l’ampoule reste au bas de l’ampoule
B: c’est toujours la phase aqueuse qui se
situe au bas de l’ampoule
C: c’est le solvant à plus haut poids
volumique qui se situe au bas de l’ampoule
2) Pourquoi dégazer à l’étape 2?
A: pour éviter une explosion due à
l’accroissement de pression interne
B: c’est optionnel
C: pour laisser respirer les solutions
3) Pourquoi enlever le bouchon à l’étape 3?
A: pour ne pas le perdre
B: pour laisser entrer l’air permettant ainsi
un écoulement laminaire par le robinet
C: c’est optionnel
4
http://culturesciences.chimie.ens.fr/node/891
G2 Extraction

5
G2 valeur de KPet lipophilie
Tout composé, en présence d’une solution biphasique comprenant une phase organique et
une phase aqueuse, se partagera selon sa solubilité dans chacune des phases en présence.
Le coefficient de partage est défini comme:
KP= [composé]phase organique / [composé]phase aqueuse
Un composé plus soluble dans la phase organique que dans la phase aqueuse aura un KP>1
montrant un caractère hydrophobe ou lipophile. A l’inverse un composé plus soluble dans la
phase aqueuse que dans la phase organique aqueuse aura un KP<1 montrant un caractère
hydrophile.
En général, dans la littérature on parle de log P: logP est synonyme de logKP.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
1
/
16
100%