definitif-Exam204 2

UNIVERSITE PIERRE ET MARIE CURIE
LC204 2009-2010
EXAMEN DE CHIMIE ORGANIQUE
11 juin 2010, session 1 - Durée de l’épreuve : 2 heures
L’épreuve contient 4 pages. Elle comporte 3 problèmes indépendants dont la durée de traitement est fournie
à titre indicatif. Les problèmes 1 et 2 seront traités sur 2 feuilles différentes. Le problème 3 sera à rédiger
directement sur la feuille d’énoncé qui sera rendue. L’usage des documents est interdit. Votre copie doit être
rédigée à l'encre bleue ou noire uniquement.
Problème 1 (20 minutes) : On se propose d’étudier les premières étapes de la synthèse d’une
phéromone de mouches des fruits à partir du bromodiol A:
HO OH
Br base : NaH
1 équivalent
réactifs?
OPh
O
A
B
D
1) CH3MgBr
E
C (C4H8O2)
2) H3O+
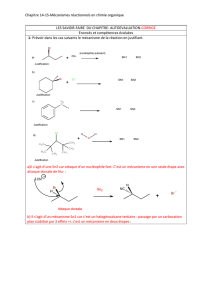
1) Dessiner l’intermédiaire B résultant de l’action d’un équivalent de base sur A et qui conduit
à C par cyclisation. Dessiner le dérivé C avec sa stéréochimie.
2) Donner les réactifs permettant de former D à partir de C.
3) Préciser les charges partielles sur les atomes en gras du réactif CH3MgBr.
4) Dessiner la structure de E avec sa stéréochimie. Ecrire le mécanisme permettant d’expliquer
sa formation à partir de D.
5) Ecrire le carbocation unique F qui se forme lorsque le dihydropyrane est mis en milieu
acide. Préciser la raison de cette sélectivité pour F, et justifier brièvement en comparant
l’autre carbocation potentiel F’ qui aurait pu se former.
O
H+
Dihydropyrane
carbocation F
6) Ecrire le mécanisme de la réaction entre l’alcool E et [F] qui donne G après extraction.
OPh
G
O O
E
1) [ F ]
2) hydrolyse

Problème 2 (1h10) : Synthèse de la cétone sabinique.
CO2H
iPr
A
B
KMnO4 concentré
C
C11H18O6
à chaud
CMeOOC
MeOOC CO2Me
iPr
D
?1) MeONa
2) H2O, [H+]
E1, E2, E3, E4
C12H18O5
OCO2Me
iPr
F
HO OH , [H+]G
G
H
H3O+
I
-iPr :
CH2Cl
iPr
J
O
1) LiAlH4SOCl2
pyridine
RAPPEL :
CH2Cl
iPr
J
O
K
OiPr
2) neutralisation
MeOH, H+
1) HCl 6mol/L, !
C11H20O3
EtONa
2) MeOH, [H+]
-CH(CH3)2
E1, E2, E3, E4
1) Préciser la configuration du carbone asymétrique du composé A en numérotant les
substituants selon les règles de CIP. Une solution de ce composé induit-elle une déviation
du plan de la lumière polarisée ?
2) Donner la structure de B. Préciser le mécanisme de sa formation.
3) Donner la structure de C.
4) Indiquer les réactifs nécessaires à la transformation de C en D.
5) Donner le mécanisme mis en jeu au cours de la formation d’une des quatre cyclopentanones
E1, E2, E3, et E4.
6) La transformation permettant de former F, à partir du mélange de E , est en fait le résultat de
trois réactions : nommer ces réactions avec les termes chimiques appropriés.
7) Donner la structure des composés G, H, I et préciser le mécanisme de l’étape de formation
de G.
8) Préciser quel intermédiaire est formé par action de la base sur J. Proposer un mécanisme
pour la formation de la cétone sabinique K.

A remplir directement sur la feuille N° d’anonymat :
Problème 3 (30 minutes) : Une synthèse d’une hormone humaine, la progestérone, a été présentée
par W.S. Johnson. Cette synthèse a pour particularité de mimer ce qui se passe dans la nature, elle
est appelée biomimétique :
AB
HO +
réactif ?
carbocation C
cascade
de
cyclisations
H2O
O
E
O
OOF
réactif(s)?
D (C21H32O)
H2O
+
1) Noter dans la case un réactif qui permet de former le carbocation B à partir de l’alcool A.
2) Dessiner dans les crochets la structure du carbocation C résultant de la cascade de réactions
décrite par les flèches de mécanisme indiquées sur la formule de B.
3) Dessiner la structure de D résultant de l’attaque nucléophile de l’eau sur l’intermédiaire C.
4) Noter dans la case le (ou les ) réactif(s) permettant de former le dérivé F à partir de la cétone E.

5) Ecrire la structure de l’espèce carbanionique G, formée par action de la soude NaOH sur la
tricétone F, et qui conduit à la formation du composé H1.
6) En utilisant la numérotation des atomes inscrite sur la formule de F, indiquez ci-dessous les sites
nucléophile et électrophile de G permettant d’expliquer la formation de H1.
Pour former H1 : atome nucléophile = n° atome électrophile = n°
7) Sur la formule de G, expliciter les flèches de mécanisme de la réaction G donne H1.
8) Ecrire la structure de la progestérone résultant de l’action d’acide à chaud sur le composé H1.
O
O
OF
NaOH
OO
O
O
OH
OH
O
OH
O
H1H2 H3
hydrolyse
H3O+, !
Progestérone
1
2
3
45
67
G
9) Question bonus(hors barème) si vous avez du temps: lors de l’action de la base sur la
tricétone F puis hydrolyse, 2 produits secondaires minoritaires H2 et H3 auraient pu se former.
En observant les liaisons créées dans H2 et H3, expliciter de la même façon les sites qui auraient
été impliqués.
Pour former H2 : atome nucléophile = n° atome électrophile = n°
Pour former H3 : atome nucléophile = n° atome électrophile = n°
1
/
4
100%