Coût biologique de la résistance aux antibiotiques : vancomycine

La Lettre de l’Infectiologue - Tome XV - n° 7 - septembre 2000
285
MISE AU POINT
a résistance aux antibiotiques est un problème qui va
sans cesse en s’aggravant. Toutes classes d’antibio-
tiques confondues, on assiste, en effet, à une constante
progression non seulement de la proportion de souches résis-
tantes, mais aussi du nombre de mécanismes conférant la résis-
tance. Ces deux phénomènes sont d’ailleurs étroitement liés.
Ainsi, la capacité de multiplication d’une souche résistante est
l’indicateur du profit qu’elle retire de l’expression de cette résis-
tance pour sa survie et sa propagation dans un environnement
hostile. En contrepartie, les modifications génétiques et méta-
boliques nécessaires à la résistance sont une mesure de l’in-
vestissement concédé par la bactérie pour acquérir la capacité
de multiplication en présence d’une concentration définie d’an-
tibiotique. Mettant de côté les bactéries qui requièrent d’em-
blée une CMI élevée parce qu’elles sont intrinsèquement résis-
tantes à un antibiotique, on peut distinguer celles qui montrent
une CMI progressivement croissante, généralement par muta-
tions successives de la cible de l’antibiotique, de celles pour
lesquelles la CMI augmente par paliers suite à l’acquisition de
matériel génétique étranger.
Combinant ces deux modalités de modification génétique,
les entérocoques vancomycine-dépendants représentent un
exemple de l’adaptabilité des bactéries aux changements que
l’homme impose à leur environnement. Devenues incapables
de croître en l’absence de vancomycine, elles posent de façon
critique la question du coût de la résistance : quel prix la bac-
térie est-elle prête à payer pour survivre aux antibiotiques ?
Paradoxe de l’évolution, la dépendance pourrait n’être en fait
qu’une étape transitoire vers une résistance de très haut niveau
(figure 1). C’est du moins ce que suggère l’histoire d’une
Coût biologique de la résistance aux antibiotiques :
vancomycine-dépendance, le prix ultime bactérien ?
* Unité de pharmacologie cellulaire et moléculaire, Université catholique
de Louvain, Bruxelles, Belgique.
** Unité des agents antibactériens, Institut Pasteur, Paris.
!
F. Van Bambeke*, P. Courvalin**
RÉSUMÉ.
Depuis quelques années, on isole chez des patients traités par les glycopeptides des entérocoques dépendant de la présence de van-
comycine pour leur croissance. L’analyse moléculaire du mécanisme responsable de ce phénotype a révélé dans chaque cas une mutation inac-
tivant la D-alanine:D-alanine ligase impliquée dans la synthèse des précurseurs du peptidoglycane. Ces bactéries requièrent donc la présence
de vancomycine pour induire l’expression des gènes conférant la résistance aux glycopeptides en permettant la synthèse de précurseurs ter-
minés par D-alanine-D-lactate. Les entérocoques dépendants posent donc de façon critique la question du prix que les bactéries sont prêtes
à payer pour s’adapter aux modifications de leur environnement. De manière préoccupante, ces souches, a priori vulnérables en raison de
leurs exigences de croissance, sont capables d’acquérir, par mutation supplémentaire, un phénotype de résistance de haut niveau tout en per-
dant leur caractère dépendant. En effet, ont été obtenus in vitro des révertants ayant recouvré une D-alanine:D-alanine ligase fonctionnelle,
mais exprimant à un haut niveau les protéines de résistance, et des révertants constitutifs synthétisant du D-alanine-D-lactate en l’absence de
vancomycine.
Mots-clés :
Entérocoques - Vancomycine-dépendance - Vancomycine-résistance - D-alanine:D-alanine ligase.
L
VmSVmrVmDVmR
1 000
100
10
1
CMI
Transposon
Mutation
Mutation
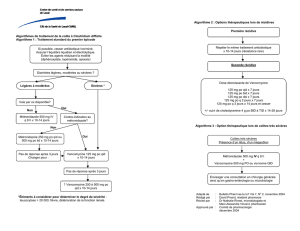
Figure 1. Antibiogramme avec un disque de vancomycine et
CMI de la vancomycine pour un isolat clinique de Enterococcus
faecalis présentant divers phénotypes :Vm
S
,sensible aux glycopep-
tides ; Vm
r
,résistant de bas niveau à la vancomycine ; Vm
D
,dépen-
dant de la présence de vancomycine dans le milieu pour sa crois-
sance ; Vm
R
,révertant in vitro hautement résistant.

patiente chez laquelle a été isolé un entérocoque dépendant de
la vancomycine pour sa croissance [(1) pour la description cli-
nique ; (2) pour la description mécanistique].
Cette patiente, hospitalisée pour une pancréatite fulminante
compliquée d’une septicémie puis d’une pneumonie nosoco-
miale contractée dans une unité de soins intensifs, a reçu une
antibiothérapie prolongée à large spectre comprenant de l’imi-
pénème, de la gentamicine, de la ciprofloxacine et de la van-
comycine. Cette dernière a été administrée de J14 à J61. À J68,
un Enteroccocus faecalis résistant à la vancomycine, de géno-
type vanB (CMI de la vancomycine, 32 µg/ml ; CMI de la tei-
coplanine, < 1 µg/ml) est isolé des urines, des fèces, de plaies,
d’abcès et des voies respiratoires. Le traitement par cipro-
floxacine et gentamicine est maintenu, tandis que la vancomy-
cine est, elle, réadministrée à nouveau de J74 à J150. À J79, la
culture des urines est négative pour l’entérocoque résistant.
Pourtant, l’examen microscopique direct des urines montre la
persistance de coques à Gram positif. Une culture primaire des
urines sur une gélose au sang permet de mettre en évidence
quelques colonies, qui disparaissent à la première subculture.
Ces colonies retrouvent leur capacité de croissance autour d’un
disque imprégné de vancomycine ou de D-alanine-D-alanine
(D-Ala-D-Ala). Le même organisme est isolé cinq fois dans les
urines entre J79 et J145. À J145, on isole à nouveau un enté-
rocoque résistant à la vancomycine dans le sang (CMI non
déterminée). Le traitement par la vancomycine est alors inter-
rompu et remplacé par de l’imipénème, qui éradique enfin l’in-
fection. En parallèle, la mise en culture de l’entérocoque dépen-
dant en l’absence de vancomycine a rapidement permis de
sélectionner au laboratoire des révertants (c’est-à-dire des
mutants de la souche dépendante ayant perdu le caractère
dépendant, mais ayant conservé une résistance élevée à la
vancomycine).
VANCOMYCINE-DÉPENDANCE OU LA GENÈSE
D’UN PROCARYOTE “DROGUÉ” :
MÉCANISMES MOLÉCULAIRES ÉTAPE PAR ÉTAPE
Vancomycine et activité antibiotique (3)
Les glycopeptides (vancomycine et teicoplanine) inhibent la
synthèse de la paroi bactérienne en perturbant les réactions de
réticulation (transpeptidation, transglycosylation) des précur-
seurs du peptidoglycane (figure 2). La synthèse du peptido-
glycane commence dans le cytoplasme bactérien par la forma-
tion de pentapeptides terminés par un dimère d’acides aminés
de la série D (D-Ala-D-Ala). La formation de ce dimère néces-
site l’action d’une enzyme appelée la D-alanine:D-alanine
ligase (Ddl). Le dimère se fixe ensuite sur un précurseur
tripeptide-acide muramique qui, après addition d’une acétyl-
glucosamine, se lie à un transporteur lipidique permettant son
exposition sur la face externe de la membrane. Le précurseur
est alors soumis à l’action de transglycosylases qui catalysent
la formation de ponts entre glucides et de transpeptidases qui
assurent la condensation des chaînes peptidiques en éliminant
la D-alanine terminale. La vancomycine, incapable en raison
de sa taille de pénétrer dans la bactérie, reconnaît les extrémi-
tés D-Ala-D-Ala des précurseurs pentapeptidiques exposés à
la face externe de la membrane. Elle s’y lie avec une haute affi-
nité par l’intermédiaire de cinq ponts hydrogène, prévenant
l’accès des enzymes qui catalysent les étapes de réticulation.
286
La Lettre de l’Infectiologue - Tome XV - n° 7 - septembre 2000
MISE AU POINT
Voie acquise
de synthèse
du peptidoglycane
Voie chromosomique
de synthèse
du peptidoglycane
D-lactate
UDP
UDP
D-Ala:D-Lac
ligase
P-P
D-alanine
UDP
UDP
D-Ala:D-Ala
ligase
P-P
P-P
VmS
VmR
VmD
P-P
O
X
H
CH3O
N
O
H
CH3
H
C
O-
D-Ala-D-Ala
NH
O
X
H
CH3O
O
O
H
CH3
C
O-
D-Ala-D-Lac
NH
Liaison de forte affinité
activité de l'antibiotique Liaison de faible affinité
résistance à l'antibiotique
D-alanine
D-lactate
Autre acide aminé
Acide muramique
N-acétylglucosamine
Vancomycine
Figure 2. Comparaison des voies de synthèse des précurseurs du
peptidoglycane chez des entérocoques vancomycine-sensibles (Vm
S
),
vancomycine-résistants (Vm
R
) ou vancomycine-dépendants (Vm
D
).
Chez l’entérocoque sensible, la voie chromosomique de synthèse
conduit à la production de précurseurs terminés par le dimère D-
alanine-D-alanine (D-Ala-D-Ala) auquel la vancomycine se lie avec
une forte affinité (panneau inférieur). Chez l’entérocoque résistant,
une voie de synthèse alternative et inductible par de faibles concen-
trations de vancomycine permet la synthèse de précurseurs termi-
nés par D-alanine-D-lactate (D-Ala-D-Lac) auxquels la vancomy-
cine se lie avec une faible affinité (panneau inférieur). Chez
l’entérocoque dépendant, la voie de synthèse chromosomique est
non fonctionnelle suite à l’inactivation de l’enzyme dimérisant la
D-alanine (Ddl ou D-Ala:D-Ala ligase). La synthèse des précurseurs
n’est alors possible que par la voie alternative inductible par la van-
comycine.

Vancomycine et résistance bactérienne (génotype vanB) (4)
Connaissant le mode d’action des glycopeptides, on comprend
qu’une résistance puisse résulter de la production de précur-
seurs de faible affinité pour la vancomycine. Ainsi, le rempla-
cement de la D-alanine terminale par un D-lactate suffit à
réduire l’affinité de l’antibiotique pour sa cible d’un facteur
1000, parce que la reconnaissance moléculaire ne met plus en
jeu que quatre ponts hydrogène (figure 2).
La synthèse de la paroi à partir de précurseurs terminés par
D-Ala-D-Lac nécessite la mise en place d’une nouvelle voie
métabolique (figure 3). Celle-ci requiert des enzymes, d’une
part pour la synthèse des précurseurs terminés par D-Ala-D-
Lac (produits des gènes vanHet vanB ;ce dernier, qui donne
son nom au génotype de résistance, spécifie la ligase per-
mettant la réaction de condensation de D-Ala avec D-Lac
[figure 2]), et d’autre part pour la destruction des précur-
seurs terminés par D-Ala-D-Ala (produits des gènes vanX
et vanY).
La résistance résulte de l’acquisition de matériel génétique
étranger codant pour des protéines qui doivent agir de
manière coordonnée. L’ensemble des gènes correspondants
(figure 3) est porté par un transposon, élément génétique
mobile de onze kilobases, capable de s’intégrer dans le chro-
mosome ou dans un plasmide. Sur la base de la séquence des
gènes de résistance, on distingue actuellement cinq géno-
types (vanA, vanB, vanC, vanD et vanE) qui diffèrent par le
niveau de résistance conféré et le type de précurseur produit
(D-Ala-D-Lac ou D-Ala-D-sérine). Le génotype vanB, qui
nous concerne ici, confère une résistance de niveau variable
à la vancomycine uniquement [le niveau de résistance dépend
essentiellement du rapport entre la quantité de précurseurs
terminés par D-Ala-D-Ala et ceux terminés par D-Ala-D-
Lac, qui résulte du niveau d’expression des gènes de résis-
tance ; la résistance à la teicoplanine n’apparaît que lorsque
ce rapport est très largement en faveur du D-Ala-D-Lac (4)].
Outre les gènes codant pour les enzymes impliquées dans la
résistance, le transposon porte aussi ceux responsables de la
La Lettre de l’Infectiologue - Tome XV - n° 7 - septembre 2000
287
MISE AU POINT
-P-P-
-P-P-
vanR vanS vanY vanW vanH vanB vanX
RÉGULATION RÉSISTANCE
Pyruvate
VanH
D-lactate
VanB VanX
Ddl
UDP
UDP
UMP
P-P-
P-
UDP
UDP
P-P-
VanY
P-P-
Cytosol Membrane Paroi
Pi
Transglycosylase
Transpeptidase
Figure 3. Structure de l’opéron conférant la résistance à la vancomycine de type VanB et activité des enzymes produites.
vanS et vanR codent pour un système régulateur à deux composants dans lequel VanS est le senseur détectant la présence de vancomycine dans
le milieu et VanR le régulateur activant la transcription des gènes conférant la résistance. VanX et VanY hydrolysent le dipeptide D-Ala-D-Ala
et les précurseurs terminés par D-Ala-D-Ala, respectivement ; VanH et VanB permettent la synthèse du depsipeptide D-Ala-D-Lac. La fonction
de VanW est inconnue. Les symboles sont les mêmes que dans la figure 2.

régulation de leur expression. Dans ce système à deux com-
posants, le senseur (produit du gène vanS) détecte la présence
de vancomycine au contact de la bactérie et le régulateur (pro-
duit du gène vanR) active la transcription des gènes de résis-
tance lorsqu’il est lui-même phosphorylé par le senseur. La
résistance s’exprime donc de façon inductible. Une question
qui se pose est l’origine des gènes constituant ce transposon.
Une hypothèse, basée sur des comparaisons de séquences,
suggère que ceux requis pour la résistance (vanH, vanB et
vanX) pourraient provenir des micro-organismes producteurs
de glycopeptides qui peuvent synthétiser leur paroi égale-
ment à partir de précurseurs terminés par D-Ala-D-Lac (5)
afin d’échapper à l’action antibiotique de leur propre méta-
bolisme secondaire.
!Rapport coût-bénéfice. La présence de la résistance exige l’ac-
quisition d’un opéron et donc une transmission de matériel géné-
tique entre bactéries. Le niveau de résistance de la bactérie hôte
dépend du niveau d’expression des gènes et de leur nombre de
copies. Lorsque ces gènes sont intégrés dans le chromosome, pré-
sents en une copie par bactérie, la résistance est de plus bas niveau
que s’ils sont portés par un plasmide présent en multicopies. Dans
le type VanB, l’expression des gènes est étroitement régulée (4),
entraînant des CMI relativement basses de la vancomycine
(32µg/ml) [figure 4] (2). La sensibilité à la teicoplanine est
maintenue, car cet antibiotique n’est pas un inducteur. Le bilan
coût-bénéfice est facile à établir : plus la bactérie investit en termes
de production d’enzymes, plus les concentrations en vancomy-
cine auxquelles elle peut résister seront élevées.
288
La Lettre de l’Infectiologue - Tome XV - n° 7 - septembre 2000
MISE AU POINT
BÉNÉFICE COÛT
Phénotype CMI
(Vm)
CMI
(Te)
Événement
génétique
Acides aminés
de la DdI
en 251-253
Précurseurs
produits
Vm(-) Vm(+)
Niveau d'expression
de l'opéron vanB
Vm(-) Vm(+)
Vm 1 < 1
S
Vm 32 < 1 transposon
r
Vm 512 64 mutation ddI
D
Vm Te 1 024 256 mutation vanS
RR
Vm Te 512 8 mutation ddI
RS
DAK
DAK
E
EYK
E
D251 E251
K253
D-Ala-D-Ala-P
ADP
D-Ala-D-Ala-P
ADP
D-Ala:D-Ala ligase fonctionnelle
La charge (+) de K253 facilite
le transfert du phosphate de l'ATP
pour la dimérisation de la D-alanine
D-Ala:D-Ala ligase non fonctionnelle
En l'absence de K253, le transfert
du phosphate de l'ATP et la dimérisation
de la D-alanine ne peuvent se faire
Figure 4. Phénotype et génotype d’un entérocoque résistant de bas niveau à la vancomycine (Vm
r
), d’un mutant vancomycine-dépendant (Vm
D
)
isolé in vivo, et de révertants de ce dernier obtenus in vitro (2, 9). Les révertants ont perdu le caractère dépendant et sont soit résistants de haut
niveau à la vancomycine mais sensibles à la teicoplanine (Vm
R
,Te
S
), soit résistants de haut niveau à la vancomycine et à la teicoplanine (Vm
R
,
Te
R
).Le bénéfice et le coût peuvent être déduits des CMI et de la nature des modifications génétiques et du niveau de production des protéines
de résistance, respectivement.
"Phénotype. Les CMI de la teicoplanine ont été déterminées en présence de 4 µg/ml (Vm
S
,Vm
r
) ou de 10 µg/ml (Vm
D
,Vm
R
) de vancomycine
comme inducteur. Les proportions relatives de précurseurs terminés par D-Ala-D-Ala ou D-Ala-D-Lac sont indiquées en vert et en rouge res-
pectivement. L’activité des protéines de résistance (mesurée par l’activité de VanX) est présentée en fraction de l’activité maximale mesurée
pour le révertant Vm
R
Te
R
.
"Génotype.Seules sont indiquées les modifications de séquence de la D-Ala:D-Ala ligase (Ddl) détectées en position 251-253 relatives à la
séquence de l’enzyme parentale (Vm
r
). La modélisation moléculaire (panneau inférieur) de l’enzyme sauvage et celle du mutant dépendant
indiquent comment la mutation DAK-E inactive la Ddl et comment la mutation E-EYK restaure son activité.
.../...

La Lettre de l’Infectiologue - Tome XV - n° 7 - septembre 2000
291
MISE AU POINT
Vancomycine et dépendance bactérienne
L’entérocoque vancomycine-dépendant (phénotype VmD) se
caractérise par son aptitude à pousser uniquement en présence
de vancomycine, ce qui suggère qu’il ne peut synthétiser les
précurseurs de sa paroi que si la vancomycine induit la pro-
duction des protéines de résistance. Autrement dit, la voie de
synthèse chromosomique “normale” des précurseurs du pepti-
doglycane doit être inactivée. De fait, si l’on identifie les pré-
curseurs produits, on constate que la souche dépendante syn-
thétise 100 % de précurseurs terminés par D-Ala-D-Lac en
présence de vancomycine (figure 4). La comparaison des voies
de synthèse des précurseurs (chromosomique sensible et alter-
native résistante) révèle que l’enzyme qui diffère est la ligase
qui catalyse la dimérisation de la D-alanine dans les souches
sensibles ou la fixation du D-lactate à la D-alanine dans les
souches résistantes (figure 2). Le caractère dépendant doit donc
être lié à une inactivation de la D-Ala:D-Ala ligase. La
séquence du gène de structure de cette enzyme a été détermi-
née pour plusieurs souches dépendantes et a révélé dans chaque
cas une mutation qui affecte un résidu hautement conservé (2,
6, 7) ou provoque l’apparition d’un codon d’arrêt conduisant à
la production d’une protéine tronquée (8). Dans le cas choisi
ici à titre illustratif (2), une délétion de six paires de bases
conduit au remplacement par un glutamate (E) d’un triplet
d’acides aminés comportant une lysine (K) hautement conser-
vée parmi les D-Ala:D-Ala, D-Ala:D-Lac ou D-Ala:D-Sér
ligases. La mutation entraîne donc la perte de deux acides ami-
nés et la substitution d’un troisième acide aminé chargé posi-
tivement par un résidu chargé négativement. Au niveau molé-
culaire, ce changement a des répercussions majeures sur
l’activité de l’enzyme. En effet, le résidu lysine joue un rôle
important dans la réaction enzymatique, facilitant par sa charge
le transfert du phosphate depuis l’ATP vers la D-alanine comme
préliminaire à la réaction de dimérisation (9).
!Rapport coût-bénéfice. L’investissement génétique condui-
sant au phénotype dépendant est minime (une mutation), de
même que l’effort métabolique (niveau d’expression des
protéines de résistance très bas). Le bénéfice est majeur en
termes de résistance, puisque la CMI de la vancomycine passe
de 32 à 512 µg/ml et celle de la teicoplanine, en présence de
vancomycine comme inducteur, atteint 64 µg/ml. Ce gain s’ex-
plique par le fait que seul le depsipeptide D-Ala-D-Lac est pro-
duit. L’activité des protéines de résistance, mesurée par celle
de VanX, est cependant faible (figure 4). Toutefois, la bactérie
se trouve fortement pénalisée dans sa croissance, puisqu’elle
ne peut se multiplier qu’en présence de vancomycine.
Vancomycine-dépendance et réversion
La souche résistante isolée en fin de traitement chez la patiente
n’ayant malheureusement pas été conservée, on ne peut affir-
mer qu’il s’agit d’un révertant de la souche dépendante. Cette
éventualité mérite toutefois d’être retenue. En effet, in vitro, la
culture de mutants dépendants en l’absence de vancomycine
permet de sélectionner aisément des révertants ayant perdu leur
caractère dépendant et acquis un niveau élevé de résistance à
la vancomycine et, dans certains cas, à la teicoplanine (figures 1
et 4, tableau I). À ces deux phénotypes correspondent deux
mécanismes, que l’on peut proposer sur la base de l’analyse
des précurseurs produits et des niveaux d’expression des pro-
téines de résistance. Le phénotype restant sensible à la teico-
planine (VmRTeS) est associé à la production de D-Ala-D-Ala
en l’absence d’inducteur mais à la production essentiellement
de D-Ala-D-Lac en présence d’inducteur, associée à une acti-
vité importante des protéines de résistance. Ces propriétés indi-
quent que la D-Ala:D-Ala ligase est à nouveau fonctionnelle.
La séquence du gène ddl présente en effet une nouvelle muta-
tion à la position altérée chez le mutant dépendant, restaurant
un triplet d’acides aminés différent de celui de la souche sau-
vage mais présentant la lysine critique en position 253 (figure 4)
(2). Le phénotype résistant à la vancomycine et à la teicopla-
nine (VmRTeR) est associé à la production exclusive de D-Ala-
D-Lac et à un niveau élevé d’expression des protéines de résis-
tance, aussi bien en l’absence qu’en présence d’inducteur. Ces
données indiquent que ces révertants conservent une ligase inac-
tive, ce que confirme la détermination de la séquence du gène
correspondant (figure 4), mais que l’expression de leurs gènes
de résistance est désormais constitutive. Cela leur confère la
possibilité d’exprimer leurs protéines de résistance, et donc de
synthétiser du D-Ala-D-Lac, en l’absence de vancomycine. Ce
phénotype est dû à une mutation ponctuelle au niveau du sen-
seur VanS qui conduit à l’activation permanente de l’activateur
de la transcription (figure 5, page 293) (2).
!Rapport coût-bénéfice. L’investissement génétique est à
nouveau limité, impliquant dans les deux cas une seule muta-
tion. L’investissement métabolique est cette fois important,
imposant un niveau d’expression élevé des protéines de résis-
tance. Cependant, le gain pour la bactérie est majeur, puisqu’il
lui assure une résistance de haut niveau à la vancomycine et à
la teicoplanine, tout en abolissant les contraintes de croissance
de la cellule parentale dépendante (figure 4). Deux mutations
successives (c’est-à-dire une première dans le gène ddl confé-
rant le caractère dépendant et une seconde dans le gène vanS
ou le gène ddl assurant la réversion) suffisent donc pour confé-
rer à l’entérocoque au départ faiblement résistant un niveau de
résistance très élevé aux glycopeptides.
VANCOMYCINE-DÉPENDANCE :
UNE CURIOSITÉ DE LABORATOIRE
OU UNE MENACE POTENTIELLE EN CLINIQUE ?
La nécessité de la présence d’antibiotique pour la croissance
bactérienne est pour le moins un paradoxe étonnant. La litté-
rature rapporte des exemples isolés de dépendance aux bêta-
lactamines (10), aux aminosides (11) ou à la polymyxine (12).
Ces isolats ont été considérés comme des curiosités ne justi-
fiant aucun effort diagnostique ou thérapeutique étant donné
que leur mode de croissance particulier assure en principe leur
élimination spontanée. Depuis la description du premier enté-
rocoque dépendant des glycopeptides pour sa croissance en
1994 (1), de telles souches ont été isolées chaque année chez
des patients qui, en général, ont reçu un traitement prolongé
par la vancomycine (tableau I, page 292) et des antibiotiques
.../...
.../...
 6
6
 7
7
 8
8
 9
9
1
/
9
100%