ANNEXE 1 : ECBTG

Cancéro D1 GB Louise GENESTIER Emilie SAHUGUET
Thomas BACHELOT 12/02/08
25
100 %
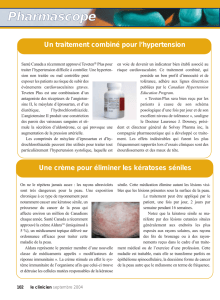
Estimation actuarielle et DS
%
- Suppression ovarienne
- Contrôle
0
0
Âge < 50
66,6 %
54,3 %
6,1 %
(DS 2,9)
8,3 %
(DS 3,0)
72,7 %
62,7 %
10,4 %
(DS 3,1)
46,3 %
56,7 %
Années
80
60
40
5
20
10
15
ANNEXE 1 : ECBTG
Meta Analyse EBCTG (Chiffres 2000)
Quel est le bénéfice relatif en cas de suppression ovarienne définitive ?
- Bénéfice relatif chez les femmes < 50 ans
- Quinze essais incluant 4 900 patientes
Nombre de cas
Réduction du risque annuel (%)
de rechute
de décès
Castration
vs contrôle
1 295
31
2p = 0,00006
31
2p = 0,00003
Castration + CT
vs CT
3 587
7
NS
3
NS
NS = Non Significatif
CT = Chimiothérapie
La castration définitive est efficace. Elle diminue le risque annuel de rechute et de décès par
cancer du sein de 31 % et de décès quelle que soit la cause de 28 %. Ces résultats sont très
significatifs. La méta-analyse a montré que le bénéfice absolu se confirme au fil du temps
(avec un suivi de 15 ans), tant pour les rechutes que pour la survie globale et la survie
spécifique. Celle-ci augmente de 10 % à 15 ans (59,4 vs 49,1 %).
En revanche, la castration n’apporte pas de bénéfice supplémentaire quand elle est associée à
la chimiothérapie (CT).
On considère la castration chez une femme avec un cancer du sein et avant rechute comme un
traitement adjuvant (= traitement donné après la chirurgie pour éviter une rechute
métastatique). Ici l’hormonothérapie permet un gain de 13% sans rechute.
Estimation actuarielle et DS
- Suppression ovarienne
- Contrôle
0
57,3 %
49,6 %
9,2 %
(DS 3,1)
12,2 %
(DS 3,2)
66,5 %
61,8 %
Âge < 50
13,4 %
(DS 3,2)
45,6 %
59,0 %
D’après R. Peto et le Trialists’ Collaborative Group
20
40
60
80
100
5
10
%
0
15
Années
Suppression ovarienne
vs contrôle (1)
Survie sans récidive
Suppression ovarienne vs
contrôle (2)
Survie globale

Cancéro D1 GB Louise GENESTIER Emilie SAHUGUET
Thomas BACHELOT 12/02/08
26
Traitement adjuvant par tamoxifène : Durée du traitement
• Soixante-trois essais incluant 48 310 patientes
Durée
du traitement
Nombre de
cas
Réduction du risque annuel
(%)
de rechute
de décès
1 an
9 128
18
2p = 0,00001
11
2p = 0,0001
2 ans
24 169
23
2p < 0,00001
14
2p < 0,00001
5 ans
15 013
31
2p < 0,00001
18
2p < 0,00001
Le traitement adjuvant par tamoxifène diminue les rechutes et les décès de façon significative.
L’étude indirecte de l’influence de la durée du traitement adjuvant par tamoxifène suggère
qu’un traitement de 5 ans est plus efficace qu’un traitement de 2 ans, lui-même plus efficace
qu’un traitement d’1 an.
Tamoxifène : pas de bénéfice d’un traitement au delà de 5 ans
NSABP B-14 Femmes ménopausées ou non, N-
Tam 5 ans
(N=593)
Tam 10 ans
(N=579)
P
Survie Sans Récidive
82%
78%
0.03
Survie
94%
91%
0.07
(Tam = Tamoxifène)
L’étude NSABP B-14 chez des malades avec des tumeurs RE + et sans envahissement
ganglionnaire axillaire montre une détérioration de la survie sans rechute et de la survie
lorsqu’on prolonge la durée d’administration du tamoxifène adjuvant à dix ans au lieu de cinq.
C’est à la suite de cette étude que la durée standard d’administration du tamoxifène a été de 5
ans en adjuvant.
20
40
60
80
100
5
10
Estimation actuarielle et DS
%
- Suppression ovarienne
- Contrôle
0
0
15
Âge < 50
78,0 %
63,8
%
2,3 %
(DS 1,5)
0,4 %
(DS 2,6)
80,3
%
64,2
%
-3,2 %
(DS 3,6)
52,5
%
55,8
%
Années
Suppression ovarienne + CT
vs même CT
Survie sans récidive

Cancéro D1 GB Louise GENESTIER Emilie SAHUGUET
Thomas BACHELOT 12/02/08
27
Traitement adjuvant par tamoxifène : étude des rechutes des femmes RE–
Nombre
de cas
Tamoxifène
Contrôle
Significativité
Tamoxifène +
CT
vs même CT
8 000
28,2 %
28,6 %
NS
Tamoxifène
vs contrôle
4 000
38,4 %
39,9 %
NS
L’utilisation du tamoxifène chez les femmes dont les tumeurs sont RE– ne modifie pas le
nombre de rechutes
Tamoxifène 5 ans vs contrôle (1) : Survie sans récidive (patientes RE+)
20
40
60
80
100
5
10
Estimation actuarielle et DS
%
- Tamoxifène
- Contrôle
0
0
15
RE+
Années
73,7
%
62,7
%
11,5 %
(DS 0,9)
13,4 %
(DS 1,1)
85,2
%
76,1
%
13,4 %
(DS 1,4)
54,9
%
68,2
%

Cancéro D1 GB Louise GENESTIER Emilie SAHUGUET
Thomas BACHELOT 12/02/08
28
0
5
10
0
1
0
2
0
3
0
4
0
5
0
0
5
10
0
1
0
2
0
3
0
4
0
5
0
27,1 %
Contrôle
= 5 ans TAM
29,0 %
Contrôle
30,9 %
30,0 %
= 5 ans TAM
21,3
19,
9
23,
6
19,
5
Perte 1,9 %
(erreur type 1,5)
logrank 2p > 0,1 ; NS
R
ec
h
ut
e
R
ec
h
ut
e
= 5 ans tamoxifène versus sans
RECHUTE
RE - RP-
= 5 ans tamoxifène versus sans
RECHUTE
RE - RP +
Gain 10 ans 0,9 %
(erreur type 3,1)
logrank 2p < 0,1 ; NS
%
+ SE
%
+ SE
Années
Années
Mise à jour 2006
Traitement adjuvant par tamoxifène :
20
40
60
80
100
5
10
Estimation actuarielle et DS
%
- Tamoxifène
- Contrôle
0
0
15
RE+
Années
86,3 %
69,4 %
3,2 %
(DS 0,7)
7,4 %
(DS 1,1)
89,5 %
76,8 %
7,9 %
(DS 1,5)
57,0 %
64,9 %
0
5
10
0
10
20
30
40
50
0
5
10
0
10
20
30
40
50
Contrôle
44,4 %
28,3 %
= 5 ans TAM
Contrôle
38,2 %
24,5 %
= 5 ans TAM
34,3
18,5
25,1
14,8
Gain 10 ans 16,1 %
(erreur type 2,2)
logrank 2p < 0,00001
Gain 10 ans 13,6 %
(erreur type 1,2)
logrank 2p < 0,00001
Rechute
Rechute
= 5 ans tamoxiféne versus sans
RECHUTE
RE + RP-
= 5 ans tamoxifène versus sans
RECHUTE
RE + RP +
%
+ SE
%
+ SE
Années
I.A. Stéroïdien :
Inhibition irréversible
Tamoxifène 5 ans vs
contrôle (2) : survie
globale (patientes RE+)

Cancéro D1 GB Louise GENESTIER Emilie SAHUGUET
Thomas BACHELOT 12/02/08
29
• Tumeurs RE+
• Tamoxifène 5 ans
→ Bénéfices relatifs en fonction de l’âge
Tranche
d’âge
(années)
Nombre de
cas
Réduction du risque annuel (%)
de rechute
de décès
< 50
5 447
34
24
50-59
3 870
35
20
60-69
3 742
50
27
> 70
1 321
38
26
Total
14 380
41
24
Les bénéfices obtenus par un traitement adjuvant de 5 ans de tamoxifène chez les patientes
RE+ sont retrouvés quels que soient l’âge et le statut ganglionnaire.
→ Influence de l’envahissement ganglionnaire
Nombre de
cas
Réduction du risque annuel
(%)
de rechute
de décès
Ganglions
négatifs
5 600
43
22
Ganglions
envahis
2 580
37
26
→ influence de la CT
Nombre
de cas
Réduction du risque annuel
(%)
de rechute
de décès
Tamoxifène vs
contrôle
4 969
43
22
Tamoxifène + CT vs
CT
3 211
35
30
L’association du tamoxifène à la CT augmente le bénéfice en réduisant les rechutes (35 %) et
les décès (30 %) alors que l’association d’une castration à la CT n’améliore pas les résultats
obtenus par la CT seule.
Effets du traitement par tamoxifène :
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
1
/
17
100%