Partie théorique: 1-Réaction d`oxydo

1
Partie théorique:
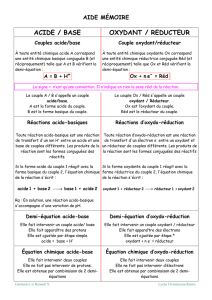
1-Réaction d'oxydo-réduction:
Une réaction d'oxydo-réduction est une réaction chimique au cours de
laquelle se produit un transfert d'électrons. L'espèce chimique qui capte
les électrons est appelé « oxydant » ; celle qui les cède, « réducteur ».
Les réactions d'oxydo-réductions constituent une grande famille
comprenant de nombreuses réactions chimiques, puisqu'elles
interviennent dans les combustions, certains dosages métallurgiques, la
corrosion des métaux, l'électrochimie ou la respiration cellulaire. Ces
réactions jouent en particulier un rôle fondamental en biologie, dans la
transformation de l'oxygène au sein des corps vivants. Elles sont
également massivement utilisées par l'industrie humaine, à l'exemple de
l'obtention de la fonte à partir de minerais composés d'oxyde de fer, par
réduction, puis de fer et d'acier à partir de la fonte, par oxydation.
2-Définitions:
*Première définition:
Suite à des expériences avec le mercure, Lavoisier met en évidence en
1772 le rôle du dioxygène dans certaines réactions d'oxydo-réduction. Il
pose les premières définitions :
L'oxydation signifie « combinaison avec l'oxygène ». Par exemple :
2 Hg + O2 → Hg2O2
Une réduction est « l'extraction d'un métal de son oxyde », définition
déjà utilisée en métallurgie. Par exemple :
SO2 → S + O2
Dans le langage courant, l'oxydation est la réaction chimique dans
laquelle un composé se combine avec un ou plusieurs atomes
d'oxygène. Comme l'oxydation du fer qui produit la rouille :
4Fe + 3O2 → 2 Fe2O3.
Ce n'est qu'au XXe siècle, après la découverte de l'électron (J.J. Thomson,
1897) et l'introduction du modèle atomique de Bohr (1913) que les
réactions chimiques ont été réexaminées à la lumière de ces nouveaux
modèles et que des similitudes observées permirent de dégager

2
progressivement le concept actuel d'oxydo-réduction qui s'exprime en
termes de transferts d'électrons.
Les réactions d' oxydo-réduction par voie sèche ( échange de dioxygène )
sont efficacement décrites par les diagrammes Ellingham. L' outils
principal des réactions redox en milieu aqueux étant la formule de
Nernst.
* Définitions plus modernes:
Pour faciliter l'étude des réactions, on utilise un outil qui associe (parfois
abstraitement) à chaque atome d'un composé un nombre d'oxydation
(n.o.) qui symbolise la valeur de la charge portée. (Fe2+ a un nombre
d'oxydation de 2.)
Une oxydation est une perte d'électrons (donc une augmentation du
n.o., les électrons étant chargés négativement). Par exemple :
Cu → Cu2+ + 2 e-
Ce don d'électrons ne se produit que s'il existe un corps susceptible de
les accepter.
Le phénomène inverse (acceptation des électrons) est appelé la
réduction.
Une réduction est un gain d'électrons (donc une diminution du n.o., les
électrons étant chargés négativement). Par exemple :
I2 + 2 e- → 2 I-
Ainsi, les « combinaisons avec l'oxygène » ne sont qu'un cas particulier
des réactions d'oxydo-réduction. Voici deux réactions avec le cuivre :
2Cu + O2 → 2CuO
Cu2+ + 2 Cl- → CuCl2
La première combine le cuivre et le dioxygène tandis que la seconde
combine l'ion cuivre et l'ion chlorure. L'ion chlorure et le dioxygène ont
un point commun : ce sont des éléments plus électronégatifs que le
cuivre.

3
L'oxydation d'un corps s'accompagne toujours de la réduction d'un autre
(les électrons ne peuvent pas circuler seuls et sont nécessairement
captés), on parle d'une réaction d'oxydo-réduction. L'oxydation est une
demi-réaction de l'oxydo-réduction et la réduction est l'autre demi-
réaction.
3-Vocabulaire :
Prévision du sens d'une réaction d'oxydo-réduction en utilisant la règle
du gamma
Dans une oxydo-réduction,
l'élément qui perd un ou des électron(s) est appelé « réducteur »,
l'élément qui capte un ou des électron(s) est appelé « oxydant ».
Le réducteur s'oxyde (réaction d'oxydation), l'oxydant se réduit (réaction
de réduction). L'oxydo-réduction se compose donc de deux demi-
réactions : une oxydation et une réduction.
Oxydation
réducteur(1) = oxydant(1) + ne- (les flèches n'apparaissent que si
la réaction est totale, quand K > 10 000)
Réduction
oxydant(2) + ne- = réducteur(2)

4
Oxydo-réduction (« somme » de l'oxydation et de la réduction)
oxydant(2) + réducteur(1) → oxydant(1) + réducteur(2)
Exemple :
Ce4+ + e- = Ce3+
Fe2+ = Fe3+ + e-
d'où la réaction bilan :
Ce4+ + Fe2+ → Ce3+ + Fe3+
Un réducteur oxydé (=forme oxydée) est un oxydant, et un oxydant
réduit (=forme réduite) est un réducteur. On définit ainsi le couple
oxydant-réducteur (aussi appelé « couple redox ») qui se compose de
l'oxydant et du réducteur conjugué (l'oxydant réduit). On le note sous la
forme : oxydant/réducteur.
En biochimie, et notamment à propos de la synthèse des molécules
prébiotiques, on parle de réactions se produisant dans une atmosphère
oxydante, c'est-à-dire en présence d'oxygène, par opposition à une
atmosphère réductrice, contenant par exemple du gaz carbonique.
Certain composés chimiques peuvent se comporter aussi bien en
oxydant qu'en réducteur. C'est notamment le cas de l'eau oxygénée,
dont on dit qu'elle se dismute, et qui par conséquent ne peut être
conservée longtemps :
H2O2 = 2H+ + O2 + 2e- (oxydation)
H2O2 + 2H+ + 2e- = 2H2O (réduction)
Soit au final :
2H2O2 → 2H2O + O2 (oxydo-réduction)
On a par exemple les couples oxydant-réducteur Cu2+/Cu et Zn2+/Zn, qui
donnent la réaction en solution aqueuse :
Zn(s) + Cu2+(aq) → Zn2+(aq) + Cu(s) (oxydo-réduction)
Cette réaction peut se décomposer en une réduction et une oxydation :
Zn(s) = Zn2+(aq) + 2e- (oxydation)
Cu2+(aq) + 2e- = Cu(s) (réduction)

5
Les deux demi-réactions d'oxydation et de réduction peuvent réellement
être séparées dans certains cas (c'est-à-dire qu'elles ne se produisent
pas au même endroit), ce qui permet de générer un courant électrique
(c'est ce qui se passe dans les piles électriques). Dans les autres cas, par
exemple dans l'exemple donné, elles n'ont qu'un intérêt formel (les
électrons libres n'existent pas dans l'eau).
Partie pratique:
1-But du TP :
Mettre en oeuvre un dosage direct d’oxydo-réductio.
2-principe du dosage :
On souhaite réaliser le dosage des ions ferreux Fe2+ par les ions
permanganate MnO4-, l’ion Fe2+ est le réducteur associé au couple
oxydant réducteur Fe3+/ Fe2+.
L’ion MnO4- est l’oxydant associé au couple oxydant réducteur
MnO4-/Mn2+ .
3-Manipulation :
- introduire à la pipette jaugée, un volume V1=10mL de la solution de
sulfate de fer(2) de concentration inconnue (C1) dans un erlenmeyer.
- ajoute avec précaution 2mL de la solution d’acide sulfurique de
concentration Co=1moL/L.
- dose avec une solution de permanganate de potassium de
concentration C2=0.02mol/L en agitant .
- Note le volume correspondant à l’éuivalence V2 lorsque la teinte rose
persiste.
- refaire l’essai trois fois.
 6
6
 7
7
 8
8
1
/
8
100%