5ème colloque national sur les maladies neuromusculaires

5
EME
COLLOQUE
NATIONAL
SUR LES
MALADIES
NEUROMUSCULAIRES
COLLOQUE AFM
DU 21AU 25
JUIN 1993
COMPTE
RENDU
FLASH

DYSTROPHIES
MUSCULAIRES DE
DUCHENNE ET DE BECKER :
DEUX AFFECTIONS
ALLÉLIQUES
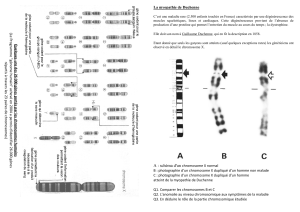
La pathologie moléculaire du gène DMD est
responsable des maladies de Duchenne et
Becker. Localisé dans la région Xp21 du
bras court du chromosome X, il code pour la
protéine située sous la surface de la mem-
brane musculaire : la dystrophine.
Duplications et délétions du gène DMD sont
responsables d’environ 70 % des cas de
dystrophies de Duchenne et de Becker. Ni la
taille ni la localisation des délétions ne sont
corrélées à la sévérité du phénotype.
Les 30 % restant s’expliquent pour la plupart
par des mutations ponctuelles difficiles à
mettre en évidence lors d’examens de routi-
ne (confirmation diagnostique, conseil géné-
tique).
L’utilisation d’anticorps permet d’apprécier
la qualité de la répartition sous-membranaire
(immunocytochimie sur les coupes de biop-
sie musculaire) et la taille (immunoélectro-
phrorèse ou Western blot) de la dystrophine.
Dans la forme dite de Becker : la dystrophine
existe en bonne quantité mais a une taille
anormale ; dans la maladie de Duchenne : la
quantité de dystrophine présente est infé-
rieure à 5 % de la quantité de dystrophine
présente dans un muscle normal.
DE L’IMPORTANCE DU
COMPLEXE
GLYCOPROTÉIQUE ASSOCIÉ
À LA DYSTROPHINE.
Il a été démontré que dans le tissus où la
dystrophine est absente, il existe une dimi-
nution importante (90 % de la normale) des
2
Les progrès de la biologie
moléculaire et de la physiologie
ont conduit à une approche
nosologique nouvelle des maladies
neuromusculaires.
Les recherches précisent de mieux en
mieux les facteurs de régulation
impliqués dans la myogénèse ou
dans l’épigénèse de la jonction
neuro-musculaire. Les études sur la
physiologie du muscle ont clarifié le
rôle des rétinoïdes et des androgènes
ainsi que celui de la plasticité
musculaire.
Les travaux sur l’acétylcholinestérase
et le médiatophore facilitent la
compréhension du fonctionnement de
la jonction neuro-musculaire. La
physiopathologie des syndromes
myasthéniques congénitaux et les
propriétés des canaux ioniques
musculaires sont de mieux en mieux
connues.
On ne parle plus du rôle de la
dystrophine mais de celui du
complexe dystrophine-
glycoprotéines.
La génétique fait son entrée dans des
domaines où la notion d’hérédité était
jusqu’alors controversée, en
cardiologie par exemple avec les
cardiomyopathies familiales.
Recueil minutieux de données
familiales, certitude diagnostique des
maladies et outils de cartographie
performant permettent aux
chercheurs de localiser les gènes
selon des stratégies de moins en
moins hasardeuses (maladies liées à
l’X, dystrophie des ceintures,
amyotrophies spinales, ataxie de
Friedreich), voire d’identifier la
pathologie moléculaire (maladie
deCharcot-Marie-Tooth, paralysies
périodiques et myotonies
congénitales, dystrophie facio-
scapulo-humérale, myotonie de
Steinert, dystrophie musculaire de
Duchenne/Becker).
Révision des critères de diagnostic,
meilleure connaissance des maladies,
études sur la qualité de vie
participent à l’amélioration de la prise
en charge à l’aube de la mise au point
de thérapeutiques nouvelles.
1
Physiopathologie
des maladies
neuromusculaires :
vers une
compréhension
moléculaire
De la physiopathologie
au traitement
Les hypothèses actuelles sur
le(s) rôle(s) de la dystrophine
au niveau de la cellule
musculaire vont du lien
mécanique entre le
cytosquelette des fibres
musculaires et la matrice
extracellulaire à la régulation
des canaux calcium mécano-
sensibles en passant par le
repliement de la membrane
cellulaire lors de la contraction
de la fibre musculaire.Certains
pensent que l’absence de
dystrophine rend la cellule
musculaire sensible à des
facteurs banals tels que les
radicaux libres, l’hyperthermie
ou les toxines excitatrices…

constituants d’un complexe glycoprotéique
transmembranaire.
L’importance du rôle physiopathologique
de ce complexe glycoprotéique a été
confirmée par la découverte du fait que la
dystrophie musculaire récessive sévère de
l’enfant (SCARM), qui se voit aussi chez les
filles et dont l’expression clinique mime de
façon moins sévère celle de la maladie de
Duchenne, est liée à l’absence d’une des
glycoprotéines du complexe : le 50kDA
DAG.
Le gène de la dystrophie dite “maghrébine”
du fait de sa grande fréquence en Afrique
du Nord) qui s’exprime comme une maladie
de Duchenne autosomique récessive, a été
récemment localisée dans la région péri-
centrométrique du chromosome 13
(13q12). On ne sait pas encore s’il s’agit de
la même maladie que la dystrophie sévère
de l’enfant avec déficit en 50 kDA DAG.
MYOTONIES CONGÉNITALES :
UN MÊME GENE EN CAUSE
Une liaison génétique entre le gène CCL-1,
(localisé sur le bras long du chromosome 7
(7q35), codant pour le canal chlore
musculaire) et les myotonies congénitales
dominante (maladie de Thomsen) et
récessive (myotonie récessive généralisée
de Becker) a été démontrée.
Une mutation déletère de ce gène a été
retrouvée dans la myotonie récessive
généralisée de Becker. On attend la
caractérisation de la mutation délétère dans
la myotonie congénitale dominante
(Thomsen).
PARALYSIES PERIODIQUES
La paralysie périodique hyperkaliémique
(avec ou sans myotonie ou avec paramyo-
tonie) ainsi que la paramyotonie congénita-
le sont des maladies génétiques de trans-
mission autosomique dominante associées
à des anomalies du canal sodium musculai-
re. Le gène SCN4A code pour la sous-unité
αdu canal sodium musculaire. Il est locali-
sé sur le braslong du chromosome 17
(17q23), proche du gène de l’hormone de
croissance.
Les mutations responsables de la paramyo-
tonie congénitale semble survenir dans la
même région du canal sodium. Cela ne
semble pas être le cas pour les paralysies
périodiques hyperkaliémiques. La poursuite
des études familiales permettra d’approfon-
dir l’étude des corrélations phénotype
(forme de la maladie exprimée)/génotype
(type de mutation génétique).
Il n’existe pas de liaison génétique entre le
gène SCN4 A et la paralysie périodique
hypokaliémique (maladie de Westphall).
DYSTROPHIE MYOTONIQUE
DE STEINERT :
L’ANTICIPATION EXPLIQUÉE
Le défaut génétique localisé en 19q13-3 est
une répétition anormale d’une séquence
CTG, 50 à plusieurs milliers de fois chez les
personnes malades contre 5 à 35 fois chez
les sujets sains. Statistiquement, il existe
une corrélation entre la taille de l’amplifica-
tion de la séquence et la gravité de
l’expression clinique. Au fil des générations,
le nombre de séquences CTG répétées
augmente dans la plupart des cas, expli-
quant la survenue de formes de plus en
plus graves, de génération en génération
(phénomène d’anticipation). Cependant, la
corrélation n’est pas suffisamment forte
pour prévoir la sévérité de la maladie d’une
personne sur la seule base du nombre de
répétitions.
La séquence protéique que l’on a déduite
de la structure du gène est celle d’une pro-
téine kinase, d’où le nom de myotonine
protéine kinase. Sa fonction est encore
inconnue. Elle rendrait compte de l’atteinte
multisystémique (insulino résistance res-
ponsable d’une mauvaise utilisation systé-
mique du glucose ?).
MALADIES DE CHARCOT
MARIE TOOTH
De transmission autosomique dominante,
la CMT est la forme la plus fréquente de
neuropathie sensitivo-motrice héréditaire.
L’anomalie en cause est une duplication
d’un gène localisé sur le bras court du
chromosome 17 (17p12.2) qui code pour
une protéine constitutive de la myéline : la
protéine PMP 22.
On a découvert qu’une délétion de ce
même gène était responsable de la paraly-
sie récidivante tronculaire ou neuropathie
tomaculaire, qui se manifeste par des épi-
sodes de paralysie régressifs, liés à la com-
pression des troncs nerveux.
La CMT Ib est une forme plus rare, de
transmission autosomique dominante, dont
le gène est localisé sur le chromosome 1
(en 1q21-23).
Enfin il existe des formes dites CMT Ic,
autosomiques dominante ou récessive qui
ne sont liées ni au chromosome 17 ni au
chromosome 1.
Par ailleurs on sait qu’il existe deux formes
de CMT liées au chromosome X dont une
est localisée sur le bras long du chromoso-
me X (Xq13).
EN ATTENDANT L’IDENTIFI-
CATION DU GENE DES A.S.I.
La caractérisation récente de facteurs de
croissance possédant une puissante activi-
té neurotrophique sur les motoneurones
ouvre des perspectives prometteuses dans
le traitement de maladies neuro-dégénéra-
tives comme les amyotrophies spinales
infantiles.
On sait depuis 30 ans environ que la survie
des motoneurones, au cours de leur déve-
loppement, dépend de facteurs neurotro-
phiques délivrés par le muscle (la culture in
vitro des motoneurones n’est posible qu’en
présence d’extraits de muscle). On a pu
isoler depuis plusieurs facteurs, qui sont
des protéines basiques de structure assez
proche appelées encore neurotrophines :
NGF, BNDF, NT5, NT3. Deux de ces fac-
teurs sont probablement responsables de
la croissance physiologique du motoneuro-
ne.
Des publications récentes ont montré que
le BDNF (et dans une moindre mesure la
NT-3) peut réduire in vivo la mort neuronale
induite par axotomie. L’administration de
CNTF a amélioré significativement l’évolu-
tion d’un modèle murin d’amyotrophie spi-
nale (mutation pmn/pmn).
Chez l’homme, si l’injection de neurotro-
phines aux sites périphériques semble peu
réaliste (ce sont des macromolécules
instables), le transfert, dans le cerveau, de
myoblastes exprimant les neurotrophines,
ou même la thérapie génique sont des stra-
tégies thérapeutiques envisageables. 3

4
2
La chasse
aux gènes
D
u diagnostic clinique à l’identification
des gènes impliqués dans les mala-
dies génétiques, la “chasse aux gènes”
est une véritable enquête policière.
Le génome est un vaste territoire peuplé
par quelques 100 000 gènes dont cer-
tains, “hors-la-loi”, sont responsables de
maladies. Quadriller ce terrain par un
réseau d’”indicateurs” est désormais
possible grâce à la carte génétique et à la
carte physique.
L’ENQUETE
La première étape consiste à donner le
signalement précis de la maladie car
celle-ci constitue un indice essentiel dans
la recherche des gènes coupables.
Puis, les campagnes de prélèvement per-
mettent de recueillir de nombreux “témoi-
gnages”. A partir des enquêtes familiales,
les enquêteurs recherchent si leurs
“indics”(les marqueurs posés comme
repères) sont en relation avec le coupable
(le gène fautif), ce qui leur permet de le
localiser. Cette étude de liaison génétique
(linkage) est d’autant plus efficace que les
enquêteurs ont à disposition un panel
important de familles, car ils peuvent dès
lors repérer des marqueurs génétiques de
plus en plus proches du gène, et donc
cerner le coupable dans une maison fer-
mée où il ne tardera plus à se rendre (car-
tographie fine). La dernière étape consis-
te à attraper le coupable (identification), à
le faire avouer (séquençage) et à retrou-
ver “l’arme du crime” (identification de la
protéine).
LES COUPABLES
Les gènes présentent des anomalies dif-
férentes : des délétions (absence de
matériel génétique), des mutations (chan-
gement de nucléotides), des duplications
(une partie du matériel génétique est dou-
blée). On a découvert récemment un nou-
veau type d’anomalie : il s’agit de l’ampli-
fication d’un triplet de nucléotides, c’est à
dire d’une répétition anormalement éle-
vée d’une séquence constituée de 3
bases.
Il arrive que l’enquête aboutisse à l’identi-
fication de plusieurs coupables dont la
contribution peut-être“alternative” c’est à
dire que le coupable est différent selon
les individus(hétérogénéité génétique
comme dans la cardiomyopathie hyper-
trophique, la myopathie des ceintures ou
la maladie de Charcot Marie Tooth) ou
simultanée, c’est à dire que les cou-
pables se sont organisés en gang chez
un même individu (polygénie). L’enquête
se complique alors pour reconnaître le
chef du gang.
Enfin, des enquêtes portant sur des
maladies différentes peuvent désigner le
même coupable : le gène de la dystrophi-
ne est responsable des myopathies de
Duchenne et de Becker ; le gène PMP22,
de la maladie de Charcot Marie Tooth
(duplication) et de la paralysie tronculaire
récidivante familiale (HNPP) (délétion); le
gène du récepteur aux androgènes, du
syndrome du testicule féminisant (muta-
tion) et du syndrome de Kennedy (amplifi-
cation d’un triplet de nucléotides)..
.
LES GENES COUPABLES DE 13 MALADIES ONT ÉTÉ ATTRAPÉS
(IDENTIFIÉS)
Maladie de Duchenne-Becker
Dystrophie Musculaire Sévère de l’Enfance autosomique récessive
Myotonie Congénitale (Maladie de Thomsen)
Myotonie Récessive Généralisée ou Myotonie de Becker
Paralysie Périodique Hyperkaliémique (Adynamie de Gamstorp)
Hyperthermie Maligne
Glycogénose de type III (Maladie de Pompe)
Glycogénose de type V (Maladie de Mac Ardle)
Glycogénose de type VII (Maladie de Tarui)
Syndrome de Kennedy ou Atrophie Bulbo Spinale
Maladie de Charcot Marie Tooth type 1 a
Paralysie Tronculaire Récidivante
Dystrophie Myotonique de Steinert
LES GENES COUPABLES DE 3 MALADIES SONT CERNÉS
(LOCALISATION FINE)
Amyotrophies Spinales
Myopathie des Ceintures
Dystrophie Facio-Scapulo-Humérale.
LES GENES COUPABLES DE 5 MALADIES SONT JUSTE LOCALISÉS
MAIS PAS ENCORE CERNÉS
Maladie d’Emery Dreifuss
Myopathie Congénitale Myotubulaire
Myopathie Congénitale à Centrale Core
Myopathie Congénitale à Bâtonnet ou Myopathie à Némaline
Maladie de Charcot Marie Tooth lié à l’X

5
3
Diagnostic
génétique
L’ANNONCE DU
DIAGNOSTIC
EST UN CHOC INÉVITABLE
L’annonce du diagnostic d’une maladie géné-
tique pour laquelle il n’existe pas de traite-
ment constitue une véritable rupture entre le
passé et l’avenir, une perte de l’espérance
que non seulement soi-même mais aussi les
autres nourrissaient pour sa propre vie.
“L’annonce crée le handicap” (C.Delaporte).
Le fait d’être porteur d’une maladie génétique
revêt à lui seul un caractère intolérable,
d’autant plus inacceptable que la maladie est
héréditaire. L’annonce du diagnostic
s’accompagne souvent d’une “surdité” aux
explications des médecins, précédant sou-
vent la négation pure et simple de la maladie.
LE CONSEIL GÉNÉTIQUE :
UNE AFFAIRE DE
SPÉCIALISTES
L’information délivrée par l’équipe médicale
est ici capitale, car elle conditionne la recon-
naissance de la maladie par celui qui la
porte... mais aussi par sa famille
L’information délivrée dans les consultations
de génétique ne peut pas être du ressort d’un
seul homme, à la fois médecin consultant de
l’individu, et “généticien”, consultant en
quelque sorte de la famille avec tous les
aspects généraux que cela implique
(enquêtes familiales, etc...). Une enquête de
S.Aymé a mis en évidence que la teneur de
l’information était différente selon les modali-
tés d’exercice des médecins(vacataire ou
temps partiel ; universitaire ou libéral).
LA DIFFUSION DE
L’INFORMATION DANS LA
FAMILLE
Le patient, une fois le diagnostic d’une patho-
logie transmissible posé, a souvent du mal à
communiquer l’information au sein de sa
propre famille : les collatéraux, susceptibles
eux aussi d’être porteurs de l’anomalie géné-
tique, ne sont pas systématiquement invités à
se faire eux-mêmes tester. Les individus por-
teurs font donc une rétention d’information.
Une étude menée par S.Aymé (centre de
génétique, Marseille) dans les familles de 283
individus porteurs de translocations ou
d’inversions chromosomiques a montré que
seules 44% des 1816 personnes potentielle-
ment à risque (repérées sur les arbres généa-
logiques) sont venues se faire tester
entre 1975 et 1989. Dans 18% des
familles, le taux d’exploration (nombre
d’individus de la famille qui sont venus se
faire tester est nul : la rétention d’infor-
mation totale). Dans 14 % des familles,
ce taux est de 100%. Dans près de la
moitié des familles se situant entre ces
deux extrêmes, le taux d’exploration est
inférieur à 50%.
Les raisons pour lesquelles les individus por-
teurs n’informent pas leurs collatéraux sont
liées aux tempéraments : les femmes trans-
mettent mieux l’information à leur famille que
ne le font les hommes. les personnes ayant eu
plusieurs enfants ne se sentent plus concer-
nées par la reproduction, et agissent ”comme
s’ils essayaient d’oublier ce problème”. Enfin,
moins les gens sont informés, moins ils infor-
ment.
DES QUESTIONS
DIFFICILES...
Le diagnostic présymptomatique d’ une mala-
die pour laquelle il n’existe pas de traitement,
comme la chorée de Huntington, ne se justifie
que lorsque c’est la personne elle-même qui
le demande.
Le diagnostic prénatal permet a priori aux
couples de mettre au monde des enfants
qu’ils n’auraient jamais eus,compte-tenu des
risques. Le revers est, en cas d’anomalies
dépistées, l’interruption de grossesse, impro-
prement qualifiée de “thérapeutique”. Cela
soulève un problème éthique d’autant plus
important lorsqu’il s’agit d’une maladie
d’apparition tardive... “c’est avoir bien peu de
foi dans la science et dans la médecine pour
penser que d’ici là on ne saura toujours pas la
soigner “(A. Kahn)
“Cette surdité impose une seconde
consultation dans laquelle le malade
exposera toutes les questions qui lui
sont passées à l’esprit, et dans
laquelle le médecin sera en position
d’écoute” (M.Fardeau).
“C’est très difficile de trouver le mot
juste qui garde à l’affection son
caractère potentiellement dangereux,
sans pour autant mettre un label han-
dicapant pour la vie entière”
(S.Aymé).
 6
6
1
/
6
100%