Identification d`une signature de miRNA sériques

Les miARNcir ont été extraits à partir 300µl de sera (4) avec le kit
NucleoSpin miRNA Plasma (Macherey-Nagel). Un profilage à haut débit a
été réalisé par RT-qPCR avec les plaques TaqMan®Array Human
MicroRNA v3.0 (Life Technologies) sur un système ViiA™7 (Applied
Biosystems). Chaque plaque TLDA (TaqMan ®Low Density Array A et B)
permettait l’analyse de 384 miARN et une quantification de 754 miARN
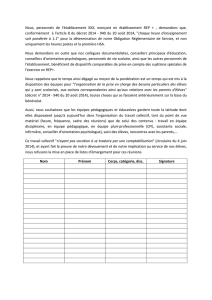
humains au total. Les données ont été analysées (Figure 1) pour générer
un classificateur.
Conclusion et perspectives
Un classificateur basé sur l’analyse par RT-qPCR d’un panel de 8 miARNcir
sériques présents avant tout traitement a été généré.
Ce classificateur permet de prédire de façon spécifique la réponse à la RCT
chez des patients atteints de cancers du rectum localement avancés.
La validation clinique des performances de ce classificateur est en cours
d’évaluation à partir d’échantillons issus de cohortes rétrospectives (ICM,
Montpellier; Uppsala, Suède (essai Rapido) et d’études ancillaires prospectives
multicentriques PRODIGE 23 (Unicancer) et GRECCAR 12 (CHU Bordeaux).
Identification d’une signature de miRNA sériques
prédictifs de la réponse au traitement néoadjuvant dans
les cancers du rectum localement avancés
Contexte
Collaboration
La prise en charge des cancers du rectum localement avancés repose sur une radiochimiothérapie (RCT) néoadjuvante suivie d’une exérèse chirurgicale.
Cette stratégie thérapeutique permet d’améliorer le contrôle local de la maladie, le degré de régression tumorale étant par ailleurs un facteur majeur de
pronostic (1). Cependant il existe une grande variabilité interindividuelle de réponse au traitement d’induction et à ce jour aucun biomarqueur spécifique n’a
été validé dans cette situation. Compte-tenu de leur stabilité, leur facilité d’analyse, et de leur présence dans le sang (2), les microARN circulants (miARNcir)
représentent des biomarqueurs potentiels d’intérêt.
Le but de cette étude était d’identifier à partir d’une simple prise de sang, effectuée avant tout traitement, une combinaison de miARNcir prédictifs
de la réponse à la RCT afin de permettre une personnalisation du traitement des patients atteints de cancers du rectum localement avancés.
Ce projet a été lauréat au Concours Mondial de l’Innovation 2014.
Patients et méthodes
Introduction
Résultats
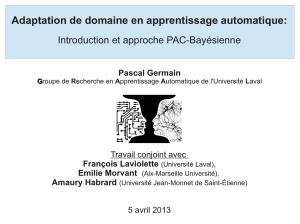
Figure 2 : Expression des miARNcir sur plaques TLDA
Evelyne Crapez1, Laurent Tosolini2, Alexandre Ho-Pun-Cheung1, Gilles Vieira2, Eric Assenat1, Caroline Mollevi1,
Odile Prigneau2, Jean-Pierre Bleuse1, Guillaume Vetter2
1ICM, Institut du Cancer de Montpellier, Montpellier - France ([email protected]ancer.fr)
2Prestizia, Clapiers – France ([email protected]r)
Références
1. Bosset JF, Collette L, Calais G, Mineur L, Maingon P, Radosevic-Jelic L, Daban A, Bardet E, Beny
A, Ollier JC, et al. Chemotherapy with preoperative radiotherapy in rectal cancer. N Engl J Med.
(2006) 355:1114-1123.
2. Mitchell PS, Parkin RK, Kroh EM, Fritz BR, Wyman SK, Pogosova-Agadjanyan EL, Peterson A,
Noteboom J, O'Briant KC, Allen A, et al. Proc Natl Acad Sci USA (2008)105(30):10513-8.
3. Dworak O, Keilholz L, Hoffmann A. Pathological features of rectal cancer after preoperative
radiochemotherapy. Int J Colorectal Dis. (1997) 12(1):19-23.
4. Ho-Pun-Cheung A, Assenat E, Bascoul-Mollevi C, Bibeau F, Boissiere-Michot F, Thezenas S,
Cellier D, Azria D, Rouanet P, Senesse P, et al. A large-scale candidate gene approach identifies
SNPs in SOD2 and IL13 as predictive markers of response to preoperative chemoradiation in
rectal cancer. Pharmacogenomics J. (2011) 11:437-443.
5. PCT/EP2015/070268: Method for predicting the clinical progression of colorectal cancer.
Soixante-neuf patients présentant des tumeurs du rectum T3-T4 et/ou N+
traités de manière homogène par radiochimiothérapie adjuvante (45-50 Gy,
5FU+/-oxaliplatine)suivied’unechirurgiedansles6à8semainesontété
inclus dans l’étude (Table 1). La réponse au traitement néoadjuvant a été
évaluée sur la pièce de résection selon la classification de Dworak (3) en 5
groupes. Les patients montrant des régressions histologiques de grade 4 et
3 ont été classés comme répondeurs. Les régressions de grade 0, 1 et 2
ont été associées aux non-répondeurs.
Figure 1 : Stratégie d’analyse
Pré-traitement des données
Analyse des courbes d’amplification/Contrôle Qualité (CQ: GES V1.0.3)
Normalisation
miRNA de référence sélectionnés par GeNorm
Analyse de l’expression différentielle
SAMR (Significance Analysis of Microarrays R)
Validation individuelle des miRNAcir par RT-qPCR
Valeur Q seuil (<0,05)
Analyse par courbes ROC
Régression logistique multivariée
Classificateur miARNcir
Parmi les 754 miARN analysés, 86 (Plaque A) et 53 (Plaque B) avaient des
profils d’amplification répondant aux CQ (Figure 2). Trois miARNcir
sélectionnés par GeNorm étaient utilisés pour la normalisation (mir-126,
mir-191 et mir-146a).
Les caractéristiques clinicobiologiques (âge, sexe, stade préthérapeutique
de la tumeur) n’étaient pas corrélées à la réponse au traitement d’induction.
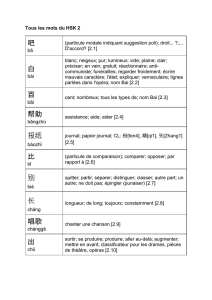
La signature brevetée (5) est composée de 8 miARNcir (Figure 3).
Figure 3 : Caractéristiques du classificateur
Valeur Prédictive Positive = 79%
Valeur Prédictive Négative = 82%
miARNcir Pr(>|z|)
hsa_miR_1 0.038958
hsa_miR_2 0.036594
hsa_miR_3 0.030128
hsa_miR_4 0.022606
hsa_miR_5 0.007036
hsa_miR_6 0.00243
hsa_miR_7 0.001534
hsa_miR_8 0.000948
Table 1 : Caractéristiques des patients
n
%
Sexe
Féminin 20 29
Masculin 49 71
Age
Médiane 62
Min-Max 39-86
uT
2811,6
356 81,2
457,2
uN
N+ 53 76,8
N- 16 23,2
Histologie
Adénocarcinome bien différencié 26 37,7
Adénocarcinome moyennement différencié 35 50,7
Adénocarcinome indifférencié 710,2
Manquant 11,4
Réponse Dworak
022,9
115 21,7
218 26,1
322 31,9
412 17,4
miARNcir miARNcir
1
/
1
100%