BTS ESF 1ère année
Devoir Surveillé L’entretien de la maison
Exercice 1 :
Comment utiliser les déboucheurs de canalisation en toute sécurité ?
DOC2
U
: Le Destop
▪Les solutions commerciales de
la marque DESTOP, vendues
pour déboucher les canalisa-
tions, contiennent essentielle-
ment de l’hydroxyde de sodium.
DOC1
U
: Fiche de sécurité
UDOC3 U: Acide et base au sens de
Bronsted
▪Un acide (au sens de Bronsted) est une es-
pèce chimique (ion, molécule) susceptible de
céder un proton H+ : AH = A- + H+
L’ion hydronium est un acide puisqu’il est ca-
pable de céder un proton:
H3O+ = H2O + H+
▪Une base (au sens de Bronsted) est une es-
pèce chimique (ion, molécule) capable de cap-
ter un proton H+ : A- + H+ = AH
L’ion hydroxyde est une base puisqu’il est
capable de capter un proton:
OH- + H+ = H2O
DOC4 U: Un couple acide/base
▪Un couple Acide/Base (AH/A-) est constitué
par deux espèces qui peuvent échanger un pro-
ton
D’après l’équation H3O+ = H2O + H+ , les
espèces H3O+ et H2O échangent un proton: elles
forment un couple H3O+ / H2O
D’après l’équation OH- + H+ = H2O , les
espèces HO- et H2O échangent un proton: elles
forment un couple H2O / HO-
DOC5 U: Les réactions acide-base en solution aqueuse
▪Lors d’une réaction acide-base, un acide d’un couple donne un proton à une base d’un autre
couple.
Autrement dit une réaction acide-base est une réaction de transfert de proton H+, entre une espèce
donneur de proton (= acide) est une espèce receveur de proton (= base)
AH + B- = A- + BH

1. Donner l'équation de dissolution de l'hydroxyde de sodium dans l'eau.
2. Quel est le nom de l'ion actif dans un déboucheur de canalisations ?
3. Ce produit actif est-il acide ou basique ?
4. Que doit-on faire pour se protéger lors de son utilisation ?
Etude de la solution
►La solution de Destop étant trop concentrée pour être directement utilisée lors d'un
dosage, elle doit donc être diluée 100 fois.
5. Rédiger le protocole qui permet de réaliser la dilution à l’aide du matériel suivant :
-fioles jaugées de 50,0 mL, 100,0 mL, 250,0 mL
-pipettes jaugées de 1,0 mL, 5,0 mL, 10,0 mL et matériel pour pipeter
- béchers
6. Quelle relation peut-on écrire entre C (concentration de la solution commerciale) et CB
(concentration de la solution diluée)?
Dosage de la solution diluée
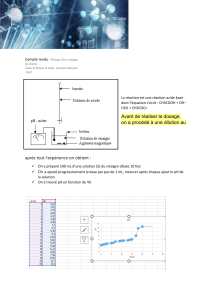
►Afin de déterminer la concentration en hy-
droxyde de sodium dans le Destop, on fait réagir la
solution diluée préparée précédemment, avec de
l’acide chlorhydrique (H3O+ ; Cl-).
On dit que l’on réalise un dosage du Destop
Au cours de la réaction, les ions H3O+ de l’acide
chlorhydrique versés par la burette, réagissent
avec les ions HO- de la solution de Destop.
On dit que l’on est « à l’équivalence du dosage», lorsque l’on a versé suffisam-
ment d’ions H3O+ pour réagir avec tous les ions OH- présents initialement dans le
bécher
7.Donner l'équation de la réaction de dosage ainsi que les couples acido-basiques en jeu.
8. Le pH de la solution dans le bécher est-il inférieur, supérieur ou égal à 7 :
a. Initialement, avant d’avoir versé l’acide chlorhydrique ?
b. Au moment de l’équivalence du dosage ?
c. Après avoir dépassé l’équivalence du dosage ?

►Le BBT est un indicateur coloré : c’est une substance qui change de couleur suivant le
pH de la solution dans laquelle il se trouve.
9. Si on rajoute quelques gouttes de BBT dans le bécher contenant le Destop dilué, quels
seront les changements de couleurs observées au cours du dosage ?
►Le volume versé d'acide chlorhydrique à l'équivalence est VA(eq) = 20,2 mL
Analyse des résultats
►On peut montrer que l’on a la relation :
B
A(eq)A
B
V
C×V
C=
10. Calculer la concentration CB (mol.L-1) de la solution diluée de Destop.
11. En déduire la concentration C (mol.L-1) de la solution concentrée de Destop en
hydroxyde de sodium
12. Calculer la concentration massique Cm (g.L-1) du Destop en hydroxyde de sodium, sa-
chant que l’on a la relation : Cm = C x M avec M(NaOH) = 40g.mol-1
13. Donner la masse d’hydroxyde de sodium dissoute dans 1 L de Destop
14. Sachant que la densité du Destop est d = 1,11 (1 L de Destop a une masse de 1100 g),
calculer le pourcentage en masse de l’hydroxyde de sodium dans le déboucheur.
Exercice 2 - TP:
Le vinaigre de vin blanc
►Les DOCS 3, 4 et 5 de l'exercice 1 peuvent être utilisés dans cet exercice ainsi
que la partie analyse des résultats.
►Le vinaigre de vin blanc est un très bon détartrant ; très économique à
l’achat, il remplace efficacement tous les autres détartrants du commerce.
L’acidité du vinaigre est due à l’acide éthanoïque (appelé également
acide acétique) de formule CH3CO2H.
On se propose de doser l’acide éthanoïque contenu dans le vinaigre de
vin blanc
►Le vinaigre commercial est trop concentré pour être dosé directement, il doit donc être dilué
10 fois.
►Afin de déterminer la concentration en acide éthanoïque dans le vinaigre blanc, on fait
réagir la solution diluée préparée précédemment, avec de la soude (Na+ ; OH-).

-Remplir une burette graduée avec de la soude (Na+ ; OH-) de concentration molaire CB =
1,0.10 -1 mol.L-1. Ajuster son zéro.
-Verser VA = 10,0 mL de vinaigre dilué dans le bécher ; rajouter quelques gouttes de
phénolphtaléine.
-Mettre le turbulent dans le bécher. Placer le bécher sur l’agitateur magnétique.
-Verser la soude dans le bécher jusqu’au changement de couleur de l’indicateur coloré.
→Noter le volume de soude VB(eq) versé à l’équivalence
1. Réaliser les expériences ci-dessous à l'aide du matériel disponible :
a. Diluer le vinaigre
b. Faire le dosage :
2. Calculer la concentration massique Cm (g.L-1) du vinaigre en acide éthanoïque, sachant
que M(C) = 12g.mol-1 ; M(H) = 1,0g.mol-1 et M(O) = 16g.mol-1
3. Sachant que la densité du vinaigre est d=1,02, calculer le pourcentage en masse
d’acide éthanoïque dans le vinaigre.
4. Ce pourcentage en masse correspond-il au degré du vinaigre indiqué sur l’étiquette
de la bouteille ?
1
/
4
100%