Inge
´nierie du tissu osseux oro-maxillofacial
par combinaison de biomate
´riaux,
cellules souches, the
´rapie ge
´nique
Oro-maxillofacial bone tissue engineering combining
biomaterials, stem cells, and gene therapy
L. Myon
a,b,c
, J. Ferri
a,b,c,d
, F. Chai
a,b
, N. Blanchemain
a,b
, G. Raoul
a,b,c,
*
,d
a
Universite
´Lille Nord de France, UDSL, 59000 Lille, France
b
Unite
´Inserm U1008, me
´dicaments et biomate
´riaux a
`libe
´ration contro
ˆle
´e, 59000 Lille, France
c
De
´partement universitaire de chirurgie maxillofaciale et stomatologie, ho
ˆpital Roger-
Salengro, rue du Professeur-Emile-Laine, CHU de Lille, 59000 Lille, France
d
Association internationale de me
´decine orale et maxillofaciale (AIMOM), 59000 Lille, France
Disponible en ligne sur
www.sciencedirect.com
Summary
Improvements have been made in regenerative medicine, due to the
development of tissue engineering and cellular therapy. Bone rege-
neration is an ambitious project, leading to many applications invol-
ving skull, maxillofacial, and orthopaedic surgery. Scaffolds, stem
cells, and signals support bone tissue engineering. The scaffold
physical and chemical properties promote cell invasion, guide their
differentiation, and enable signal transmission. Scaffold may be
inorganic or organic. Their conception was improved by the use of
new techniques: self-assembled nanofibres, electrospinning, solution-
phase separation, micropatterned hydrogels, bioprinting, and rapid
prototyping. Cellular biology processes allow us to choose between
embryonic stem cells or adult stem cells for regenerative medicine.
Finally, communication between cells and their environment is essen-
tial; they use various signals to do so. The study of signals and their
transmission led to the discovery and the use of Bone Morphogenetic
Protein (BMP). The development of cellular therapy led to the emer-
gence of a specific field: gene therapy. It relies on viral vectors, which
include: retroviruses, adenoviruses and adeno-associated vectors
(AAV). Non-viral vectors include plasmids and lipoplex. Some
BMP genes have successfully been transfected. The ability to control
transfected cells and the capacity to combine and transfect many genes
involved in osseous healing will improve gene therapy.
ß2011 Elsevier Masson SAS. All rights reserved.
Keywords: Tissue engineering, Gene therapy, Bone substitutes,
Tissue scaffolds
Re
´sume
´
La me
´decine re
´ge
´ne
´rative a progresse
´gra
ˆce a
`l’essor de l’inge
´nierie
tissulaire et de la the
´rapie cellulaire. La re
´ge
´ne
´ration du tissu osseux
est un projet ambitieux, aux applications multiples dans les sphe
`res
oro-maxillofaciale et orthope
´dique. L’inge
´nierie tissulaire osseuse
(ITO) repose sur la combinaison de trois e
´le
´ments : un support, des
cellules et des signaux. Le support posse
`de des proprie
´te
´s physico-
chimiques qui favorisent sa colonisation par les cellules, guident leur
diffe
´renciation, et autorisent la transmission de signaux. Ces supports
peuvent e
ˆtre de type inorganique ou organique. Leur conception a
progresse
´gra
ˆce a
`de nouvelles technologies (nanofibres auto-assem-
ble
´es, e
´lectrospinning, se
´paration de phase, hydrogels, bioprinting et
prototypage rapide). Associe
´es au support, les cellules ont be
´ne
´ficie
´du
ge
´nie cellulaire avec le choix entre cellules souches (embryonnaires ou
adultes) et matures. Les signaux et leurs transmissions entre les
cellules et leur environnement sont essentiels ; leur e
´tude a permis
la de
´couverte et l’utilisation des Bone Morphogenetic Protein (BMP).
Le de
´veloppement de la the
´rapie cellulaire a conduit a
`l’e
´mergence
d’une discipline particulie
`re, la the
´rapie ge
´nique. Elle fait appel a
`des
vecteurs viraux qui comprennent les re
´trovirus, les ade
´novirus et les
adeno-associated vectors (AAV). Les vecteurs non viraux comprennent
les plasmides, les lipoplex. Des essais impliquant la transfection de
se
´quences codantes pour une BMP ont e
´te
´effectue
´s. Les perspectives
d’ame
´lioration de ces techniques passent par la maı
ˆtrise accrue des
cellules transfecte
´es et par la combinaison de plusieurs se
´quences
implique
´es dans la cicatrisation osseuse.
ß2011 Elsevier Masson SAS. Tous droits re
´serve
´s.
Mots cle
´s:Inge
´nierie tissulaire, The
´rapie ge
´nique, Substituts osseux,
Supports tissulaires
*Auteur correspondant.
e-mail : [email protected] (G. Raoul).
Disponible en ligne
27 juillet 2011
47
e
congre
`s SFSCMF
201
0035-1768/$ - see front matter ß2011 Elsevier Masson SAS. Tous droits re
´serve
´s.
10.1016/j.stomax.2011.06.002 Rev Stomatol Chir Maxillofac 2011;112:201-211

Introduction
En 2011, les pertes de substances osseuses repre
´sentent tou-
jours un de
´fi technique, mate
´riel et e
´conomique. Les techni-
ques actuelles de re
´paration privile
´gient l’apport de tissu
osseux autologue, sous forme de greffes osseuses non vas-
cularise
´es [1,2] ou de lambeaux libres micro-anastomose
´s[3],
car l’utilisation de ces greffons autologues permet de re
´duire
les phe
´nome
`nes de rejet immunitaire.
Ces techniques permettent ainsi l’apport conjoint d’un sup-
port (ou matrice) et de cellules osseuses, fonctionnelles et
actives, ainsi qu’une e
´ventuelle supple
´ance vasculaire en
fonction de la technique chirurgicale et du volume greffe
´.
Il existe, cependant, plusieurs restrictions a
`l’utilisation de ces
techniques : les re
´serves osseuses mobilisables sont limite
´es
et leur pre
´le
`vement n’est pas de
´nue
´d’une certaine morbidite
´
[4]. C’est pourquoi l’allogreffe osseuse a e
´te
´propose
´e, mais
elle est soumise au risque inhe
´rent de transmission de patho-
logies infectieuses.
Concernant les besoins en os de nos patients, les implications
e
´conomiques ne sont pas ne
´gligeables puisqu’aux E
´tats-Unis,
le couˆt des proce
´dures chirurgicales lie
´es a
`la perte de tissu
osseux au niveau de la cavite
´buccale a e
´te
´estime
´a
`presque
six milliards de dollars par an [5]. Le nombre de 600 000 gref-
fes osseuses annuelles aux E
´tats-Unis est rapporte
´[6], ce qui
est tout a
`fait conside
´rable. L’inge
´nierie tissulaire osseuse
apporte donc un espoir rationnel de simplification des tech-
niques de greffe ainsi que leur de
´mocratisation.
De
´finitions
La me
´decine re
´ge
´ne
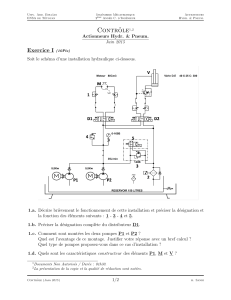
´rative (fig. 1) est une spe
´cialite
´qui permet
d’envisager de nombreuses perspectives et me
´thodes de
reconstruction du tissu osseux. Elle offre des alternatives
aux greffes osseuses.
Plan du chapitre
I. Introduction
II. De
´finitions
III. L’inge
´nierie tissulaire osseuse
III.1. Le support ou matrice (scaffold)
III.1.1. Ge
´ne
´ralite
´s sur les supports
III.1.2. Les supports inorganiques
III.1.3. Les supports organiques
III.1.4. Perspectives d’ame
´lioration des supports
III.2. Les cellules
III.3. Les signaux
III.3.1. Ge
´ne
´ralite
´s sur les signaux
III.3.2. Les biomole
´cules
III.3.2.1. Utilisation des biomole
´cules
III.3.2.2. Indications et applications des
biomole
´cules
IV. La the
´rapie ge
´nique
IV.1. Les vecteurs viraux
IV.2. Les vecteurs non viraux
IV.3. Applications
V. Conclusions
On lui distingue deux composantes : l’inge
´nierie tissulaire et la
the
´rapie cellulaire.
L’inge
´nierie tissulaire utilise les principes des sciences de la vie
et de l’inge
´nierie afin de de
´velopper des substituts biologi-
ques pour restaurer, maintenir ou ame
´liorer la fonction des
tissus. Langer et Vacanti [7] ont ainsi de
´fini l’inge
´nierie tissu-
laire en 1993. L’inge
´nierie tissulaire a e
´te
´de
´finie par Riha [8]
en 2005 en conside
´rant, d’une part, ses bases scientifiques et,
d’autre part, ses applications.
Les bases scientifiques de l’inge
´nierie tissulaire sont la coa-
lescence de trois e
´le
´ments : un support ou matrice ou scaffold
(e
´chafaudage), des cellules, et des signaux (par l’interme
´diaire
d’un biore
´acteur
1
) dont le but est de cre
´er un tissu biologi-
quement actif.
Les applications de l’inge
´nierie tissulaire peuvent e
ˆtre consi-
de
´re
´es comme la fabrication d’un tissu ne
´oforme
´et fonction-
nel qui peut e
ˆtre utilise
´in vivo a
`des fins the
´rapeutiques ou in
vitro pour la recherche (fig. 2).
La the
´rapie cellulaire peut e
ˆtre de
´finie comme : « l’adminis-
tration de cellules autologues, alloge
´niques, voire xe
´noge
´ni-
ques, a
`l’homme, dans le but de pre
´venir, de traiter ou
d’atte
´nuer une maladie » [9,10]. Ces cellules ont subi des
modifications de leurs caracte
´ristiques biologiques a
`l’issue de
leur manipulation, dans le but d’obtenir par un effet me
´ta-
bolique, pharmacologique ou immunologique, un effet the
´-
rapeutique, diagnostique ou pre
´ventif. Ces manipulations
peuvent e
ˆtre mene
´es ex vivo ou in vivo.
La the
´rapie cellulaire couvre e
´galement les cellules ge
´ne
´ti-
quement modifie
´es, exprimant des proprie
´te
´s fonctionnelles,
non ante
´rieurement exprime
´es.
Au sein de la the
´rapie cellulaire, nous trouvons donc la the
´rapie
ge
´nique. Les produits de the
´rapie ge
´nique sont de
´finis comme
des produits obtenus a
`l’issue d’un proce
´de
´de fabrication, dans
le but de re
´aliser le transfert in vivo ou ex vivo d’un ge
`ne, dans
des cellules humaines ou animales, et son expression in vivo
dans un but prophylactique, the
´rapeutique ou diagnostique.
La the
´rapie cellulaire repose sur le principe d’ensemencement
de cellules (souches ou non, transforme
´es ou non par the
´rapie
ge
´nique), encapsule
´es ou non, dans un organe le
´se
´afin de
restaurer ses fonctions ou de pre
´venir l’apparition d’une
L. Myon et al. Rev Stomatol Chir Maxillofac 2011;112:201-211
1
Un biore
´acteur (dans le domaine du Tissu Engineering) est un
syste
`me qui permet de subvenir aux besoins des cellules et des tissus;
de guider leur de
´veloppement, dans un environnement tridimen-
sionnel. Il s’agit d’une boite de pe
´tri ame
´liore
´e permettant la culture
et la croissance des cellules dans sa chambre.
202

pathologie. La the
´rapie ge
´nique est donc une des branches de
la the
´rapie cellulaire.
Nous allons donc voir l’inge
´nerie tissulaire, d’une part, et la
the
´rapie ge
´nique, d’autre part, qui est la branche de la the
´-
rapie cellulaire qui nous inte
´resse.
L’inge
´nierie tissulaire osseuse
L’inge
´nierie tissulaire repose sur le biomime
´tisme pour abou-
tir a
`la re
´ge
´ne
´ration tissulaire.
Cette discipline tire parti des avance
´es technologiques des
domaines qui la composent. Ainsi, l’essor des biomate
´riaux,
les progre
`s de la biologie cellulaire, l’ame
´lioration du ge
´nie
des proce
´de
´s contribuent aux progre
`sre
´cemment re
´alise
´s.
On distingue trois composantes ne
´cessaires aux proce
´de
´s
d’inge
´nierie tissulaire : le scaffold, les cellules et les signaux.
Le support ou matrice (scaffold)
Ge
´ne
´ralite
´s sur les supports
Le support est un support physique, colonisable par des
cellules. Il doit permettre de diriger la croissance, la diffe
´ren-
ciation et l’organisation des cellules qui y adhe
`rent. Il autorise
la transmission de signaux chimiques et physiques. Il doit
interagir avec les syste
`mes biologiques. Ainsi, le scaffold doit
guider l’adhe
´sion, puis permettre la diffe
´renciation des cel-
lules qui le colonisent. Le support ide
´al en inge
´nierie tissulaire
osseuse doit posse
´der les proprie
´te
´s suivantes : oste
´oconduc-
tivite
´, oste
´o-inte
´gration et oste
´ogene
`se, sans oublier ses
proprie
´te
´s biome
´caniques.
L’inte
´gration de mole
´cules solubles ou insolubles [11–13] aux
supports (ou scaffold)permetd’ame
´liorer la fonctionnalisation
de ces derniers et de favoriser la croissance cellulaire. Toute la
proble
´matique d’inte
´gration de mole
´cules bioactives au scaf-
fold est de ne pas de
´naturer ou modifier les proprie
´te
´sbiome
´-
caniques (re
´sistance) et biochimiques (oste
´o-induction ;
re
´sorption) du scaffold lors de l’addition ou de l’inte
´gration
de ces mole
´cules bioactives.
Le scaffold doit mimer les proprie
´te
´s (physiques et biologi-
ques) du tissu remplace
´. C’est un mate
´riel re
´sorbable, dans
l’ide
´al, adapte
´au rythme de re
´paration tissulaire. La maıˆtrise
des proprie
´te
´s du support au cours du temps (vitesse de
re
´sorption, les substances libe
´re
´es lors de sa de
´gradation,
leurs influences sur le milieu environnant) sont a
`prendre
en compte. Son architecture tridimensionnelle permet aux
cellules de secre
´ter la matrice extracellulaire, une fois colo-
nise
´e, dans l’espoir d’aboutir a
`la re
´ge
´ne
´ration d’un tissu ou
d’un organe.
La nature des biomate
´riaux se
´lectionne
´sde
´pend de leur
utilisation et a fait l’objet d’un expose
´spe
´cifique dans ce
nume
´ro de la Revue de Stomatologie [14].
Les supports osseux doivent pre
´senter une certaine porosite
´
afin de permettre leur colonisation, le transport des nutri-
ments et des signaux. Leurs proprie
´te
´sdere
´sistance physique
doivent e
ˆtre e
´leve
´es malgre
´cette structure poreuse, en
Inge
´nierie du tissu osseux oro-maxillofacial par combinaison de biomate
´riaux
[(Figure_1)TD$FIG]
Figure 1. Sche
´ma re
´capitulatif des diffe
´rentes composantes d’inge
´nierie
tissulaire osseuse et dentaire.
[(Figure_2)TD$FIG]
Figure 2. L’e
´tape 1 comprend la culture des cellules souches et la
re
´alisation d’une matrice se
´pare
´ment. L’e
´tape 2 permet la mise en
culture de ces deux composants dans un biore
´acteur. Ce dernier permet
la transmission de signaux biologiques et physiques au syste
`me
pre
´ce
´demment cre
´e
´. Enfin, l’e
´tape 3 repre
´sente un des objectifs
d’application concre
`te de l’inge
´nierie tissulaire osseuse dans le
traitement des fractures.
203

particulier lorsque l’on projette de remplacer une interruption
mandibulaire.
Les supports e
´tudie
´s et utilise
´s en inge
´nierie tissulaire osseuse
sont organiques ou inorganiques.
Les supports inorganiques
Les supports inorganiques les plus fre
´quemment utilise
´s sont
expose
´s ci-apre
`s:
bioce
´ramique phosphocalcique et les bio-verres : les
phosphates tricalciques (b-TCP), hydroxyapatite synthe
´tique.
Ils posse
`dent d’excellentes proprie
´te
´s oste
´oconductives et
d’adhe
´sion avec les tissus pe
´riphe
´riques. Leurs proprie
´te
´s
me
´caniques et leurs faibles re
´sistances aux fractures limitent
leur utilisation en charge [6]. Les phosphates tricalciques
posse
`dent une vitesse de re
´sorption supe
´rieure a
`
l’hydroxyapatite ;
polyme
`res organiques ou synthe
´tiques :
organique : collage
`ne,
synthe
´tique : polyester, poly (lactic acid) (PLA), poly
(glycolic acid) (PLGA), polycaprolactone (PCL).
Leur utilisation permet la re
´alisation de supports tridimen-
sionnels re
´fle
´chis et varie
´s. Des re
´actions d’hypersensibilite
´
aux polyme
`res organiques ont e
´te
´rapporte
´es [15]. Les pro-
duits de de
´gradation des polyme
`res synthe
´tiques peuvent
engendrer des modifications physicochimiques de l’environ-
nement (acidification).
Les supports organiques
Les supports organiques sont repre
´sente
´s par :
matrice osseuse de
´mine
´ralise
´e. Il s’agit d’une allogreffe
osseuse dont seules les prote
´ines non collage
´niques et
collage
´niques de type I ont e
´te
´conserve
´es. On retrouve de
nombreux facteurs de croissance parmi les prote
´ines non
collage
´niques dont les Bone Morphogenetic Protein (BMP) [6].
Le taux de BMP pre
´sent dans les pre
´parations est variable,
influenc¸ant les proprie
´te
´s d’oste
´o-induction et d’oste
´ocon-
duction [6]. Il existe un risque de transmission de pathologies
infectieuses inhe
´rent aux allogreffes.
Perspectives d’ame
´lioration des supports
Les perspectives d’ame
´lioration des supports passent, entre
autres par l’utilisation des micro- ou nanotechnologies. Le
biomime
´tisme micro- ou nanostructural de l’environnement
extracellulaire permet d’ame
´liorer les supports. Elles auto-
risent la re
´alisation de supports « bioactifs » qui favorisent
l’adhe
´sion et la diffe
´renciation cellulaire [11].
Ces techniques permettent d’agencer la re
´partition cellulaire
sur le support, d’inte
´grer de nouveaux traitements de surface,
d’augmenter l’adhe
´sion des cellules au support par le biais des
mole
´cules de liaison intercellulaire (inte
´grines) [11].Onpeut
aussi envisager la libe
´ration de mole
´cules (signaux, facteurs de
croissance) au sein du support, de manie
`re plus ou moins
prolonge
´e.
Plusieurs proce
´de
´s sont ainsi envisage
´s:
nanofibres auto-assemble
´es. Le principe est celui de
l’assemblage de particules composant initialement un
syste
`me de
´sordonne
´en une structure organise
´e, du simple
fait des interactions des composants entre eux, sans
intervention exte
´rieure. Cela est permis par l’utilisation de
se
´quences peptidiques. Ces se
´quences posse
`dent des pro-
prie
´te
´s hydrophobes ou hydrophiles, de
´finies par des
se
´quences d’acides amine
´s. Leurs interactions permettent
la cre
´ation de structures myce
´liennes de formes varie
´es, mais
aussi des structures tridimensionnelles.
La connaissance des proprie
´te
´s des se
´quences peptidiques et
de leurs interactions permet la re
´alisation de structures
ge
´ome
´triques [16]. Certaines se
´quences peptidiques, (RAD16-
I) re
´alisent des assemblages biomime
´tiques et reproduisent
des re
´seaux de nanofibres similaires a
`du collage
`ne de type I
[6] et posse
`dent alors des proprie
´te
´s oste
´oge
´niques vis-a
`-vis
de BMSCs (in vitro), telles que les nanofibres natives de
collage
`ne.
Il est, de plus, possible d’inte
´grer des se
´quences peptidiques
connues pour favoriser l’adhe
´sion cellulaire et la diffe
´rencia-
tion [16]. Conjugue
´es a
`des hydrogels, ces nanofibres auto-
assemble
´es sont facilement sculptables et admettent
l’adjonction de cellules selon certains patrons ;
l’e
´lectrospinning. On induit un potentiel e
´lectrostatique
e
´leve
´entre une e
´lectrode d’e
´lectrospinning et une plaque de
recueil. Ce potentiel induit une accumulation de charges a
`la
surface de la solution de polyme
`res (solvants + polyme
`res)
situe
´e sur l’e
´lectrode et engendre des forces de re
´pulsion
e
´lectrostatiques. Lorsque ces forces de re
´pulsion sont assez
e
´leve
´es, elles engendrent le transfert de la solution sur la
plaque de recueil. Une fois le solvant e
´limine
´ou e
´vapore
´,on
recueille les nanofibres forme
´es sur la plaque.
L’orientation de ces dernie
`res est perfectible et l’utilisation de
roues de recueil permet leur alignement.
Cette technique permet la cre
´ation de nanostructures
organiques et synthe
´tiques. L’utilisation de mate
´riaux
naturels a e
´te
´re
´alise
´e avec succe
`s (collage
`ne, chitine,
laminine) [16]. On peut aussi combiner la re
´alisation de
nanofibrilles de collage
`ne ou de soie et l’incorporation de
cristaux phosphocalciques [6] ;
la se
´paration de phase. Elle utilise les proprie
´te
´sde
se
´paration de phase, en faisant varier la tempe
´rature et la
concentration de la solution (solvant + polyme
`re). Apre
`s
se
´paration des phases, extraction du solvant et refroidisse-
ment, il est possible d’obtenir des nanofibres. Plusieurs
solutions comprenant des polyme
`res de nature diffe
´rente
mais une me
ˆme tempe
´rature de se
´paration de phase peuvent
e
ˆtre utilise
´s simultane
´ment. Cette technique autorise la
re
´alisation de nanofibres organiques et synthe
´tiques [16].
L’utilisation de nanocomposites synthe
´tiques est envisage
´e
afin de d’ame
´liorer les proprie
´te
´sme
´caniques du support et sa
tole
´rance. L’adjonction de PLA a
`un support nanocomposite
organique augmente la re
´sistance du support. Le remplace-
L. Myon et al. Rev Stomatol Chir Maxillofac 2011;112:201-211
204

ment complet du collage
`ne par du PCL aboutit au me
ˆme
effet [6] ;
les hydrogels. Ils reproduisent les aspects chimiques et
me
´caniques de la matrice extracellulaire.
Ils sont extre
ˆmement maniables et permettent l’e
´laboration de
ve
´ritables patrons cellulaires. Ils autorisent ainsi une reproduc-
tion plus fide
`le de la distribution cellulaire dans le tissu cible.
Des constructions plus e
´labore
´es me
ˆlant diffe
´rents types
cellulaires au sein d’un me
ˆme support sont re
´alisables. Il est
possible d’y inte
´grer des signaux d’adhe
´sion et des facteurs de
croissance ou de diffe
´renciation. On peut ainsi envisager
l’inte
´gration d’une population de cellules souches et les signaux
ne
´cessaires a
`leur diffe
´renciation au sein du gel [17]. Ils peuvent
e
ˆtre re
´alise
´sa
`partir de polyme
`res synthe
´tiques ou naturelles.
L’utilisation d’hydrogels photopolyme
´risables permet d’e
´ta-
blir des structures tridimensionnelles inte
´ressantes, par le
biais de photomasques. Le principe consiste a
`placer un
photomasque conc¸u selon un plan pre
´cis au dessus d’une
solution initiale non polyme
´rise
´e, puis de l’exposer aux UV. Le
photomasque est opaque, des zones fene
ˆtre
´es sont ame
´na-
ge
´es pour laisser passer les UV. Le motif re
´alise
´correspond
aux dessins des fene
ˆtres [11,18] ;
le bioprinting. Il s’agit de l’application me
´dicale des
proce
´de
´sderapid-prototyping (RP). Le RP consiste en la
re
´alisation de structures ; par de
´pose de couches successives
ou feuillets, selon un sche
´ma pre
´-de
´termine
´et assiste
´par
ordinateur. On envisage la re
´alisation d’organes selon ce
principe (reins, vaisseaux) (fig. 3).
Ce proce
´de
´requiert l’utilisation d’une bio-imprimante,
machine capable d’imprimer des motifs au moyen d’une
« encre » contenant des cellules vivantes.
L’encre est cre
´e
´ea
`partir de cellules ayant subi des traitements
physiques (centrifugation), qui s’organisent sous forme de
« balles ». Cette encre biologique est compose
´e de « balles »
au contenu cellulaire. Cette encre passe au sein d’une canule
dans la bio-imprimante qui la projette sur un support.
On re
´alise alors un sche
´ma ge
´ome
´trique de base sur le
support, a
`chaque couche. Un gel de matrice extracellulaire
est applique
´entre chaque couche. La re
´pe
´tition de cette e
´tape
aboutit a
`la constitution de figures ge
´ome
´triques tridimen-
sionnelles.
Ainsi, l’impression d’une structure annulaire permet d’obtenir
un cylindre et, a
`une autre e
´chelle, un vaisseau. On peut
combiner l’utilisation de diffe
´rentes encres et donc de cellules
de diffe
´rente nature (pour reproduire les diffe
´rentes tuniques
d’un vaisseau) [19,20] ;
le prototypage des matrices. La modernisation et la
re
´duction des couˆts et de
´lais permettent de
´sormais d’obtenir
des biomate
´riaux sur mesure.
Cette e
´tape permet de re
´pondre directement a
`la forme
tridimensionnelle du de
´fect osseux et de de
´terminer sa
microstructure, gardant en arrie
`re pense
´e la colonisation par
les cellules oste
´oproge
´nitrices, mais aussi la ne
´ovascularisa-
tion [21]. De plus, la forme adapte
´e permet une fixation
simplifie
´e et un rendu cosme
´tique ine
´galable (fig. 4).Le
dernier avantage e
´tant de pouvoir restaurer la biome
´canique
de l’organe remplace
´et d’ajouter le signal biome
´canique aux
cellules en contact et favoriser d’un point de vue the
´orique
l’oste
´o-inte
´gration et l’oste
´o-induction.
Une autre voie de recherche est la re
´alisation de supports pre
´-
vascularise
´s, ame
´liorant ainsi la diffusion des nutriments et qui
permettraient d’envisager des re
´ge
´ne
´rations en terrain irradie
´.
Pour ce faire, des techniques de construction de support en
plusieurs couches ont e
´te
´de
´montre
´es, permettant d’incorporer
diffe
´rents types cellulaires (endothe
´liales et osseuses) [11,18].
L’ame
´lioration des proprie
´te
´s physiques des mate
´riaux
utilise
´s, se rapprochant ainsi des conditions in vivo et
permettant la restitution des fonctions.
L’e
´tude des proprie
´te
´sdere
´sorption des mate
´riaux (temps de
re
´sorption, modifications des proprie
´te
´s physicochimiques du
milieu) est un des objectifs.
Les cellules
Le proce
´de
´standard d’inge
´nierie tissulaire comprend l’e
´labo-
ration d’un tissu tridimensionnel biologiquement actif in vitro
avant sa re
´implantation in vivo.
Inge
´nierie du tissu osseux oro-maxillofacial par combinaison de biomate
´riaux
[(Figure_3)TD$FIG]
Figure 3. Le bioprinting envisage la cre
´ation d’organes fonctionnels par
de
´pose de couches successives. Ainsi, on de
´bute par l’application d’encre
biologique sur chaque feuillet de la structure. Le dessin des motifs est
assiste
´par ordinateur. Les diffe
´rents feuillets sont empile
´s. Les gouttes
forment une structure continue par coalescence. Cette succession
d’empilement permet la re
´alisation de structures tridimensionnelles,
telles que des structures vasculaires.
205
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
1
/
11
100%