le diverticule géant de l`oreillette droite fissuré dans la plèvre

Une cause exceptionnelle de dyspnée:
le diverticule géant de l’oreillette droite
fissuré dans la plèvre
M. Fikri, M. Snaiki, A. Maroudi, S.
Bouklata, FZ. Gueddari, F. Imani
Service de Radiologie Centrale. Hôpital
Avicenne. Rabat. Maroc.

INTRODUCTION
Le diverticule de l’oreillette droite (OD)
est une anomalie extrêmement rare.
Il est défini comme une structure
sacculaire, ayant pour origine la paroi
auriculaire libre, avec une taille variable
souvent importante, communiquant avec
l’OD par un large collet (1, 2).

OBSERVATION
Patiente âgée de 28 ans, sans
antécédents pathologiques
notables
L’histoire de la maladie remonte à
2 mois par l’installation d’une
dyspnée stade II, d’aggravation
progressive. Il s’y associe des
épigastralgies avec épisodes de
lipothymie.
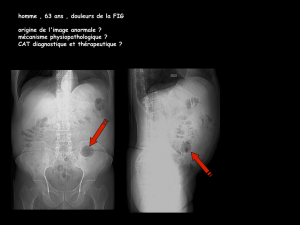
La radiographie thoracique
montre :
– Une cardiomégalie, avec débord
droit.
– Un épanchement pleural
homolatéral.

OBSERVATION
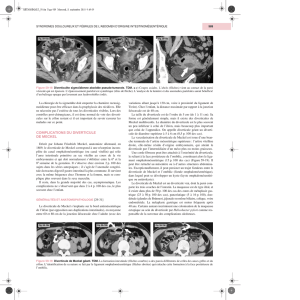
Le scanner thoracique réalisé avant et
après injection de produit de contraste
met en évidence :
– Une importante ectasie de l’oreillette
droite avec présence d’une formation
arrondie adjacente dont le
rehaussement est synchrone de celle-
ci.
– Des petits thrombi dans l’OD, sous
forme de formations hypodense,
pariétales non rehaussées après
contraste.
– Un épanchement pleural de grande
abondance, spontanément hyperdense.
– Sur les coupes basses : un trouble de
perfusion hépatique avec un aspect en
motte rappelant celui d’un Budd-Chiari.

OBSERVATION
L’échocardiographie trans-
thoracique :
– Confirme la dilatation de l’OD
– Met en évidence une poche
liquidienne communiquant avec
l’OD à travers un pertuis.
– Le doppler couleur montre le
remplissage de la poche travers
ce pertuis.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
1
/
16
100%