Chapitre I: rappels

Biochimie-réactions cellulaires
L2 Biologie-parcours BC et BCB-S3
Responsables de l’UE: James Sturgis (AMU)-Marie-Jeanne Papandréou (P1)
Organisation de l’UE: 3 parties
- COURS 28h
1ère partie: Protéines et stratégies d’études 10h; Isabelle Crenon
2ème partie: Enzymologie 12h; Marie-Jeanne Papandréou
3ème partie: Métabolisme 6h; José Luis
- TD 16h
3 TD Protéines/méthodologie; Isabelle Crenon et Myriam Brugna
3 TD Enzymologie; Myriam Brugna et Corinne Kreuzer
1 TD Métabolisme; Ludovic Leloup
1 partiel
- TP 2 jours
MCC: NF = 0,35*Partiel + 0,3*TP + 0,35*ET

1ère partie: Propriétés et stratégie d’étude des protéines
Introduction.
Chapitre I: Rappels
1.1. Les acides aminés
1.2. Structure covalente des protéines
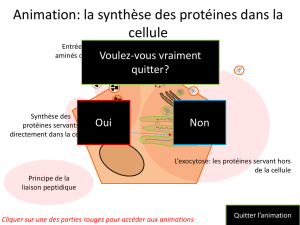
1.3. Biosynthèse des protéines
Chapitre II: Stratégies pour l’étude des protéines
2.1. Isolement d’une protéine
2.2. Composition chimique d’une protéine
Chapitre III: Structure spatiale des protéines
3.1. Conformation des protéines
3.2. Différentes liaisons covalente et non covalentes
3.3. Les 4 niveaux d’organisation structurale
3.4. Les structures secondaires
3.5. Les structures super secondaires
3.6. Structure tertiaire et notion de domaine
3.7. La structure quaternaire
Isabelle Crenon
10 heures de cours - 6 heures de travaux dirigés –

Introduction
Protéine: vient de « prôtos » = qui occupe le premier rang
rôle prépondérant dans la plupart des processus biologiques
vaste domaine des fonctions biologiques
Architecture cellulaire et tissulaire
Des protéines de structure assurent
soutien mécanique et forme des
cellules, donc des tissus et des
organismes
Métabolisme
-Les enzymes catalysent
l’essentiel des réactions chimiques
du vivant
-Des protéines comme source
d’énergie ou réserve d’acides
aminés
Communication intra
et extra cellulaire
-Hormones
-Récepteurs
Attaque et défense
et de l’organisme
-Toxine
-Immunoglobulines
-Facteurs de coagulation
Motricité
Des protéines effectuent un
travail mécanique tel
mouvement des flagelles,
contraction des muscles ou
migration des chromosomes
Transport et stockage
-Des protéines fixent,
transportent ou stockent
d’autres molécules: O2 et
hémoglobine ou myoglobine;
Fer et ferritine ou
transferrine
-Transfert des électrons
Expression des gènes
-Des protéines sont mobilisées
pour décoder l’information
génétique transcription, traduction
-Des protéines régulent
l’expression génétique

Introduction
Protéine: polymères d’acides aminés (20 acides aminés constitutifs)
Nombre et ordre d’enchaînement (séquence) déterminés génétiquement
conformation et fonction de la protéine
Structure primaire : séquence des acides aminés liés par covalence
3 autres niveaux structuraux
Structure secondaire
Conformation répétitive
localisée
Structure tertiaire
Repliement d’une chaîne
peptidique dans l’espace
Structure quaternaire
Arrangement spatial d’une
protéine multimérique
Organisation des éléments
structuraux secondaires
entre eux.
Association des sous-unités d’une
protéine complexe (au moins
dimèrique):
homo- ou hétéro-oligomère
Motifs structuraux de base:
hélice alpha, feuillet bêta,
tours et coudes…

Introduction
Les protéines peuvent être classées sur la base de
¾leur solubilité dans des solutions salines (usage limité en biochimie clinique)
Albumines, globulines, histones
¾leur forme
Protéines fibreuses, rayons axiaux >10
Protéines globulaires, compactes, rayons axiaux <10
¾leur fonction biologique
Enzymes, protéines de stockage, protéines de régulation,
protéines structurales
¾leur structure 3D
Protéines avec motif de fixation à l’ADN
¾leur mobilité électrophorétique ou leur coefficient de sédimentation
Lipoprotéines plasmatiques
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
 45
45
 46
46
 47
47
1
/
47
100%