Questions

Bio II - Ex. II

Question I
!
1!
Exos 1. Adaptation rapide des bactéries aux changements d’environnement.
Expérience : Cooper et Lenski ont testé la capacité d’une souche E. coli à s’adapter à un
nouvel environnement. L’environnement habituel est un milieu de culture riche, Luria broth
(LB), le nouvel environnement est un milieu de culture pauvre, Davis minimal (DM25,
glucose = 25 µg/mL). Ils ont établi 12 populations, chacune dérivant d’une cellule unique
d’une souche asexuée d’E. coli. Ils ont suivi ces populations pendant 20’000 générations
(3’000 jours) dans du DM25. Pour maintenir un apport nutritif régulier, 0.1 mL de culture
bactérienne est transféré chaque jour dans un tube contenant 9.9 mL de milieu DM25 frais
(dilutions 1/100 en série, Figure 1.1).
Figure 1.1 : dilution 1/100 quotidienne
Le milieu DM25 contient toutes les ressources nécessaires à la croissance, la seule source de
carbone (le glucose) est limitée. Des échantillons des cultures sont prélevés périodiquement,
chaque 5'000 générations, et la croissance en DM25 des bactéries « évoluées » est comparée
à la croissance dans ce même milieu de la souche E. coli initiale (maintenue congelée à
-80 °C pour qu’elle n’évolue pas pendant les 8 années de l’expérience).
Résultats :
La figure 1.2 montre la moyenne des taux relatifs de croissance des souches « évoluées »
(n=12) par rapport à la souche initiale (« Fitness relative to ancestor ») en fonction du nombre
de générations en culture.
Figure 1. 2 :
Questions :
1) Sachant que la masse d’une bactérie E. coli équivaut à 7x10-16 kg et que le temps de
génération (doublement) est de 20 min. en conditions optimales (LB normal), estimez
le poids de la descendance d’une bactérie après 3 jours de culture ? Justifiez la
nécessité de faire des dilutions en séries.
!
1!
Exos 1. Adaptation rapide des bactéries aux changements d’environnement.
Expérience : Cooper et Lenski ont testé la capacité d’une souche E. coli à s’adapter à un
nouvel environnement. L’environnement habituel est un milieu de culture riche, Luria broth
(LB), le nouvel environnement est un milieu de culture pauvre, Davis minimal (DM25,
glucose = 25 µg/mL). Ils ont établi 12 populations, chacune dérivant d’une cellule unique
d’une souche asexuée d’E. coli. Ils ont suivi ces populations pendant 20’000 générations
(3’000 jours) dans du DM25. Pour maintenir un apport nutritif régulier, 0.1 mL de culture
bactérienne est transféré chaque jour dans un tube contenant 9.9 mL de milieu DM25 frais
(dilutions 1/100 en série, Figure 1.1).
Figure 1.1 : dilution 1/100 quotidienne
Le milieu DM25 contient toutes les ressources nécessaires à la croissance, la seule source de
carbone (le glucose) est limitée. Des échantillons des cultures sont prélevés périodiquement,
chaque 5'000 générations, et la croissance en DM25 des bactéries « évoluées » est comparée
à la croissance dans ce même milieu de la souche E. coli initiale (maintenue congelée à
-80 °C pour qu’elle n’évolue pas pendant les 8 années de l’expérience).
Résultats :
La figure 1.2 montre la moyenne des taux relatifs de croissance des souches « évoluées »
(n=12) par rapport à la souche initiale (« Fitness relative to ancestor ») en fonction du nombre
de générations en culture.
Figure 1. 2 :
Questions :
1) Sachant que la masse d’une bactérie E. coli équivaut à 7x10-16 kg et que le temps de
génération (doublement) est de 20 min. en conditions optimales (LB normal), estimez
le poids de la descendance d’une bactérie après 3 jours de culture ? Justifiez la
nécessité de faire des dilutions en séries.
!
2!
2) Sachant qu’il a fallu 3'000 jours pour obtenir 20'000 doublement dans le milieu DM25,
quel est le temps de génération (doublement) dans ce milieu ?
3) Interprétez/ commentez la courbe de la figure 1.2.
4) Suggérez les fonctions possibles des gènes dont la séquence codante ou l’expression a
été altérée dans les populations adaptées au milieu minimal (DM25).
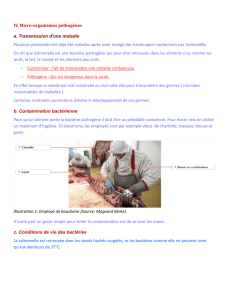
Exos 2 : Analyse génétique chez Neurospora crassa
Neurospora est un champignon microscopique haploïde dont les principales étapes du cycle
de développement sont présentées de façon simplifiée sur la figure 2.1 :
On connaît chez ce champignon deux souches qui se distinguent par leur capacité à croître
sur un milieu "minimum" sans méthionine (un acide aminé) :
· la souche sauvage [M+] peut se développer en l'absence de méthionine,
· la souche mutante [M-] a besoin de méthionine pour se développer.
On admet que ce phénotype est déterminé par l'expression d'un couple d'allèles notés M+ et
M- au locus M.

!"#$%&'()(
Ce#que#l’on#veut:##
*$%+#,(-#(.&/0$(0#(-1(0#$2#'01'2#(03"'#(412567/#(1.78$(9(:&"7$(0#(2"-5"7#(;+/-/#"(<=>?#
Ce#que#l’on#sait:#
@1$$#(03"'#(412567/#(!"#$%&'(A(BC)DE)F(GH(
I#+.$(0#(0&"4-#+#'5(A(JD(+/'(;+/-/#"(<=>(
#
Réponses#:(
K&+4/#'(0#(0&"4-#+#'5(.17(L#"7#(M(9(C(JD(+/'(A(FD(+/'(
! 9(0&"4-#+#'5$(.17(L#"7#(C(JN(L#"7#$(C(9(:&"7$(A(J)F(0&"4-#+#'5$(.&"7(9(:&"7$(0#(
2"-5"7#?((
(
@1$$#O(A(B()DE)F(GH(C(J;J)F>(A(B?9(C()DNP(GH((
())*%+',-.%/0#12#234##5#36#478#

!"#$%&'()(*$"+,#-(
Ce#que#l’on#veut:##
!"#.(#$,(.#(,#/0$(1#(23'345%&'(*1&"6.#/#',-(15'$(7#(/+.+#"(8(
Ce#que#l’on#sait9(:;<<<(=&"4$(0&"4(5>&+4(?<;<<<(1&"6.#/#',(*@A?B-(
(
Réponse#
C54(=&"49(?<D<<<(1&"6.#/#',$(E(:D<<<(=&"4$(F(GHG(1&"6.#/#',$(054(=&"4(
C54(/+'",#9(?I·60$minutes$=$)II<(/+'",#$(
)II<(J/+'E=&"4K(E(GHG(1&"6.#/#',(J=&"4KF(?)L(/+'(#$,(.#(,#/0$(1#(1&"6.#/#',(0&"4(7#(
/+.+#"(*@A?B-H(
(
Conclusion#
M#(,#/0$(1#(23'345%&'(15'$(.#(/+.+#"(05">4#(*N?<<(/+'",#$-(#$,()<(O&+$(0."$(.&'2(P"#(
.#((,#/0$(1#(23'345%&'(15'$(.#(/+.+#"(4+7Q#(*N?<(/+'",#$-H(
M#$(1+."%&'$(P"&%1+#''#$()E)<<($&',(5004&04+3#$(9(.5(0&0".5%&'(657,34+#''#(
5"2/#',#(1;"'(O57,#"4(1;#'>+4&'()<<(*?G.G(F(RS-(054(=&"4H(

!"#$%&'()(*$"+,#-(
Ce#que#l’on#veut.((
)',#/0/1,#23(4&55#',#2(67(4&"/8#(9#(67(:;"/#(<=>=(
(
(
(
(
(
(
(
(
(
(
?'(&8$#/@#("'#(7516+&/7%&'(0/&;/#$$+@#(9#(67(47074+,1(9#$(874,1/+#$(A(0&"$$#/(97'$(
6#(5+6+#"(BC>D(.(/744&"/4+$$#5#',(9"(,#50$(9#(;1'1/7%&'(7"(4&"/$(9#(6E#F01/+#'4#=(
GE7516+&/7%&'(#$,(9E78&/9(/70+9#(0"+$(06"$(6#',#=(G#$(874,1/+#$(&',(744"5"61(9#$(
5",7%&'$(7516+&/7',(67(4/&+$$7'4#(97'$(4#(5+6+#"(H(4#$(5",7%&'$(&',(1,1(
$16#4%&''1#$(7"(4&"/$(9"(,#50$=(
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
1
/
18
100%