Dystrophies musculaires de Duchenne et de Becker

Dystrophies
musculaires de
Duchenne et de
Becker
JUIN 2008
AVANCÉES DE LA RECHERCHE 2007-2008

AVANCÉES DE LA RECHERCHE 2007-2008
Dystrophies musculaires de Duchenne et de Becker
AFM>Myoinfo - 2 - AV08_DBMD.doc
Sommaire
Faits marquants de la recherche .......................................................................................4
Mieux traiter la dystrophie musculaire de Duchenne par le saut d'exon .......................4
Succès d'un essai de tolérance du PRO051 (Prosensa) chez 4 garçons DMD ......4
Démarrage d'un essai anglais (Pr. Muntoni) de phase I avec des morpholinos......5
Le point sur les avancées du saut d'exon par AAV-U7 ...........................................5
Mieux traiter les dystrophies musculaire de Duchenne et de Becker par le PTC124 .....7
Succès d'un essai de phase II et lancement d'un essai international de phase IIb .7
Participer à l'essai PTC124 en pratique ..................................................................8
Mieux traiter les dystrophies musculaires de Duchenne et de Becker par thérapie
génique...........................................................................................................................9
Le point sur deux essais de thérapie génique.........................................................9
Mieux traiter les dystrophies musculaires de Duchenne et de Becker par thérapie
cellulaire.......................................................................................................................10
Succès d'un essai Italien de tolérance d'une autogreffe de cellules souches
musculaires adultes CD133+ ................................................................................10
La greffe de mésangioblastes améliore la fonction musculaire chez les chiens
GRMD ...................................................................................................................11
Suspension de l'essai québécois de phase II d'autogreffe de myoblastes............11
Mieux traiter les dystrophies musculaires de Duchenne et de Becker par les
médicaments................................................................................................................11
Le périndopril permet aux enfants atteints de DMD de vivre plus longtemps........12
Idébénone et DMD : le point sur les résultats de l'essai Santhera ........................12
Résultats en demi teinte du premier essai clinique de phase I avec un inhibiteur de
la myostatine dans plusieurs formes de dystrophie musculaire ............................13
Autres publications ..........................................................................................................13
Mieux connaître pour mieux soigner les dystrophies musculaires de Duchenne et de
Becker ...........................................................................................................................13
Myoglobinurie et corticothérapie au long cours dans la myopathie de Duchenne :
une complication rare à connaître.........................................................................13
Sous-estimation des difficultés psychologiques et cognitives dans la myopathie de
Becker : à propos d’une enquête australienne......................................................14
Risque cardiaque chez les femmes transmettrices de dystrophinopathie : pas si
grave que cela ?....................................................................................................14
Mieux diagnostiquer la dystrophie musculaire de Duchenne.......................................15
Dépistage néonatal et maladie de Duchenne : il est urgent d’attendre .................15
Mieux soigner la dystrophie musculaire de Duchenne .................................................15
Résultats décevants de l'étude pilote avec de l'oxatomide ...................................15
La place des corticoïdes dans l’arsenal thérapeutique de la myopathie de
Duchenne : une nouvelle revue Cochrane fait le point..........................................16
Confirmation des effets bénéfiques à long terme du Déflazacort dans un groupe
de jeunes patients canadiens................................................................................16
*
* *

AVANCÉES DE LA RECHERCHE 2007-2008
Dystrophies musculaires de Duchenne et de Becker
AV08_DBMD.doc - 3 - Myoinfo>AFM
La dystrophie musculaire de Duchenne (DMD) et la dystrophie musculaire de
Becker (DMB) sont dues à des altérations du gène DYS qui code une protéine des
fibres musculaires, la dystrophine. L'anomalie moléculaire du gène DYS aboutit à
un déficit total (DMD) ou partiel (DMB) en dystrophine ou à une dystrophine de taille
anormale (DMB)
La dystrophie musculaire de Duchenne est la plus répandue des myopathies de
l'enfant : elle concerne 1 garçon sur 3 500 à la naissance. C’est une maladie qui
touche l'ensemble des muscles de l'organisme (muscles squelettiques, muscle
cardiaque et muscles lisses).
La dystrophie musculaire de Becker est dix fois moins fréquente que la dystrophie
musculaire de Duchenne. Ses manifestations sont moins marquées et moins
évolutives que celles de la dystrophie musculaire de Duchenne.
f
ibre
m
uscu
l
a
ir
e
motoneurone
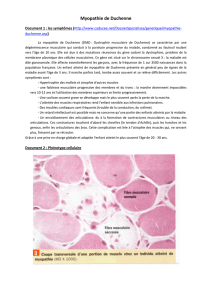
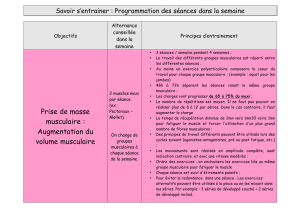
La dystrophine est localisée sous la membrane cellulaire (sarcolemme) de la fibre
musculaire. Elle est associée à un complexe de protéines (DAG : glycoprotéines
associées à la dystrophine) qui relient à travers la membrane cellulaire, l'intérieur de
la fibre musculaire (cytosquelette) à l'extérieur (matrice extracellulaire).
L’absence de dystrophine déstabilise cette interaction et par conséquent fragilise la
membrane de la fibre musculaire. La membrane musculaire fragilisée ne résisterait
plus aux contraintes imposées lors de la contraction, et la fibre musculaire serait
détruite, libérant des enzymes musculaires (CPK) dans le sang.
dystrophine
© AFM - M. Gilles
© AFM - M. Gilles

AVANCÉES DE LA RECHERCHE 2007-2008
Dystrophies musculaires de Duchenne et de Becker
AFM>Myoinfo - 4 - AV08_DBMD.doc
Faits marquants de la recherche
MIEUX TRAITER LA DYSTROPHIE MUSCULAIRE DE DUCHENNE PAR LE
SAUT D'EXON
SUCCES D'UN ESSAI DE TOLERANCE DU PRO051 (PROSENSA) CHEZ 4 GARÇONS
ATTEINTS DE DMD
Un essai clinique de phase I (faisabilité et tolérance) s’appuyant sur la technique du saut d’exon a
été mené avec succès aux Pays-Bas chez des enfants atteints de la myopathie de Duchenne. Cet
essai a utilisé des oligonucléotides anti-sens ciblant l'exon 51 : PRO051 mis au point par la société
de biotechnologie Prosensa.
48 49 52
51
48 49 52
51
X
Pas de
dystrophine
La DMD résulte de mutations dans le gène de la dystrophine.
Dans 65% des cas, il s’agit de délétions d’un ou plusieurs
exons provoquant un décalage du cadre de lecture : la
dystrophine n’est pas synthétisée.
48 49 52
51
48 49 52
Dystrophine raccourcie mais
fonctionnelle (quasi-dystrophine)
saut de l'exon 51 provoqué
par les oligonucléotides
anti-sens ciblés
Le saut d’exon a pour objectif de rattraper un cadre de lecture fonctionnel en
éliminant un ou plusieurs exons de l’ARN muté. Certes, la dystrophine produite
est plus courte (quasi-dystrophine), mais elle est fonctionnelle.
Pour induire un saut d’exon, les chercheurs interviennent au niveau de la
réaction d’épissage de l’ARN à l’aide de petits ARN artificiels anti-sens
(oligonucléotides anti-sens) spécifiques des exons qu’ils cherchent à exclure.
Ces oligonucléotides anti-sens sont soit des molécules synthétiques (comme le
PRO51 ou les morpholinos), soit produits par un minigène (U7 ou U1) qui est
apporté dans la cellule par un vecteur viral AAV.

AVANCÉES DE LA RECHERCHE 2007-2008
Dystrophies musculaires de Duchenne et de Becker
AV08_DBMD.doc - 5 - Myoinfo>AFM
Lors de cet essai, mené par l'équipe néerlandaise de Judith van Deutekom et Gertjan van Ommen,
au Centre Médical de l’Université de Leiden, 4 enfants âgés de 10 à 13 ans ont reçu dans une
partie d’un muscle de la jambe une injection unique d’un traitement à base de PRO051. Quatre
semaines après cette injection, une biopsie réalisée sur ces patients a permis de constater la
présence de la dystrophine, avec un niveau d’expression significatif. Aucun effet secondaire n’a
été enregistré et la force musculaire n’a pas été altérée par cette injection.
Un essai de phase I/II a débuté pour tester la sécurité et apporter des indications d’efficacité du
traitement par PRO051 administré non plus intramusculaire (localisé) mais par voie sous-cutanée,
qui devrait permettre d’atteindre l’ensemble de la musculature squelettique et cardiaque. Cet essai
sera mené dans trois centres à Leiden (Pays-Bas), Gotteborg (Suède) et Leuven/Louvain
(Belgique).
Local Dystrophin Restoration with Antisense Oligonucleotide PRO051.
Van Deutekom et coll. N Engl J Med. 2007, 357(26) : 2677-86 (Décembre 2007).
DEMARRAGE D'UN ESSAI ANGLAIS DE PHASE I AVEC DES MORPHOLINOS
L’essai thérapeutique de phase I, mené par Francesco Muntoni au Hammersmith Hospital de
Londres, en collaboration avec le consortium britannique MDEX et la société américaine AVI
Biopharma Incorporation, évalue la tolérance d’une injection de morpholinos (molécules
synthétiques entraînant un saut d’exon) chez 9 garçons atteint de dystrophie musculaire de
Duchenne, âgés de 12 à 16 ans.
En pratique, les malades sont séparés en trois groupes, chaque groupe recevant, au niveau d’un
petit muscle du pied, une dose croissante de morpholinos. Au bout de 14, puis de 28 jours, les
médecins pratiqueront une biopsie dans la zone traitée afin d’y rechercher tout d’abord les ARN
messagers de la dystrophine puis, éventuellement, la protéine.
L’injection des morpholinos se fait actuellement en intramusculaire mais les médecins comptent
passer rapidement à une administration systémique. Leurs recherches précliniques sur un
traitement par voie systémique chez des souris mdx ont montré qu’une injection en sous-cutanée
ou en intraveineux avaient la même efficacité. Par contre, la dose de morpholinos est plus efficace
quand elle est injectée en 4 fois sur une semaine plutôt qu’en une seule fois. Ces données
précliniques seront probablement prises en compte dans la poursuite de l’essai dont les premiers
résultats sont attendus avec impatience.
Communication de Georges Dickson
Myology 2008 (Mai 2008).
LE POINT SUR LES AVANCEES DU SAUT D'EXON PAR AAV-U7
En 2004, Luis Garcia et son équipe du Généthon avaient réussi, grâce à la technique du saut
d’exon, à rétablir la production d’une dystrophine fonctionnelle chez la souris mdx (modèle de la
dystrophie musculaire de Duchenne), avec une restauration de la force musculaire. Les
chercheurs avaient injecté par voie intra-artérielle ou intramusculaire un vecteur AAV (adeno
associated virus) couplé au gène U7. Le rôle du gène U7 est de produire un petit ARN antisens qui
va masquer l’exon défectueux et rétablir ainsi la production d’une dystrophine incomplète mais
fonctionnelle, appelée quasi-dystrophine. L'avantage de cette stratégie est de faire exprimer par
l'organisme lui-même l'outil thérapeutique, en l'occurrence l'oligonucléotide anti-sens, et cela
pendant plusieurs années.
Depuis les chercheurs ont appliqué cette technique au chien GRMD, un modèle animal beaucoup
plus proche de la maladie humaine. Ils ont d’abord démontré l’efficacité de leur approche sur un
seul membre de l'animal. La quasi-dystrophine produite est fonctionnelle puisque les fibres
musculaires sont résistantes aux contractions et que la force du membre traité est améliorée par
rapport à celle du membre non traité.
Aujourd’hui, l’équipe de Louis Garcia, maintenant implantée à l’Institut de Myologie, a développé
une nouvelle approche pour traiter un chien en entier, en collaboration avec Stéphane Blot (École
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
1
/
16
100%