DOSSIER
20
La Lettre du Gynécologue - n° 266 - novembre 2001
PRINCIPE DE L’EXAMEN
Pour le clinicien, la tomographie par émission de positons, ou
TEP, au FDG s’apparente étroitement à la scintigraphie. Les
images obtenues sont des images fonctionnelles du corps
entier qui reflètent l’accumulation intracellulaire d’un ana-
logue radioactif du glucose (figures 1-5). Par rapport à la scin-
tigraphie traditionnelle, il remarquera un gain dans la résolu-
tion des images, des anomalies infracentimétriques pouvant
être détectées.
Le [18F]-FDG et sa fixation dans la cellule cancéreuse
Une des caractéristiques de la cellule maligne est le fonction-
nement exagéré de sa glycolyse. Ce phénomène est rattaché à
une augmentation de l’activité des principales enzymes contrô-
lant cette voie métabolique (hexokinase, phospho-fructokinase
et pyruvate déshydrogénase). La transformation maligne de
certaines lignées cellulaires s’accompagne d’une augmentation
des capacités de transport membranaire du glucose.
Le [18F]-FDG est un analogue du glucose naturel pour lequel
le groupement hydroxyl en 2 est remplacé en plusieurs étapes
par un atome de fluor radioactif. Tout comme le glucose natu-
rel, le FDG plasmatique franchit la membrane cellulaire par
diffusion facilitée avec l’aide d’un transporteur (GLUT 1,
GLUT 2, GLUT 3). Le FDG est ensuite phosphorylé en FDG-
6-phosphate ([18F]-FDG-6-P) par l’hexokinase, sans métabo-
lisme ultérieur par la glucose-phosphate-isomérase. La
déphosphorylation du [18F]-FDG-6-P est négligeable dans la
plupart des tissus (sauf l’hépatocyte). Ainsi, le [18F]-FDG-6-P
porteur d’une charge négative ne peut diffuser vers l’extérieur
à travers la membrane cellulaire et s’accumule dans la cellule
sans subir de dégradation supplémentaire. La fixation du
[18F]-FDG est indépendante du débit sanguin et elle reflète le
degré de prolifération des cellules tumorales viables, indépen-
damment du type histologique.
Détection in vivo du [18F]-FDG
La concentration tissulaire en fluor-18 reflète donc celle en
[18F]-FDG, permettant de détecter les tissus qui font une forte
consommation de glucose in vivo chez l’homme, grâce à des
coupes tomographiques reconstruites à partir de la détection
externe des photons de 511 keV émis après anihilation des
positons du fluor-18. À part les tissus qui ont une forte
consommation physiologique de glucose (cerveau et, dans une
moindre mesure chez le patient à jeun, myocarde) ou qui
excrètent le FDG (reins, vessie), les tissus présentant un ou
plusieurs foyers d’hyperfixation sont suspects de malignité.
La détection non invasive des photons de 511 keV, émis en
coïncidence à la suite de la désintégration du fluor-18, nécessite
un appareillage différent des gamma-caméras traditionnelles :
– Soit une caméra dédiée dite “TEP” qui, du fait d’une détec-
tion spécialement étudiée, permet d’obtenir des images riches
en information pour un temps total d’acquisition de l’ordre de
l’heure (figure 5). Le centre TEP AP-HP a effectué des exa-
mens de routine sur une telle machine depuis 1999. Deux
autres machines sont actuellement en fonctionnement pour la
routine, l’une à Paris à l’HIA Val-de-Grâce et l’autre à Lille, et
20 machines sont autorisées et seront installées prochainement.
– Soit une caméra “mixte” dite “TEDC” (1), encore capable
d’effectuer des examens scintigraphiques traditionnels, mais
aussi de détecter le [18F]-FDG, au prix d’une moindre quantité
d’informations contenues dans les images et d’un temps d’exa-
men nettement plus long : 1 h 30 environ au total sur la machine
TEDC à 3 têtes disposons (figures 1-4). Sept machines TEDC
sont actuellement installées ou autorisées en France.
La superposition des images de TEP au [18F]-FDG à celles de la
TDM se développe rapidement ; quelques travaux montrent éga-
lement l’intérêt de la fusion des images TEP avec celles qui sont
issues de la mammographie ou de l’IRM. Elle permet d’améliorer
la précision de la localisation des lésions et de caractériser
l’organe envahi, en combinant les approches anatomiques et fonc-
tionnelles. Des machines associant TEP et TDM, les seules qui
méritent le nom actuellement répandu à tort de “PET scan”, sont
disponibles sur le marché depuis moins d’un an et le centre TEP
AP-HP espère pouvoir en faire bénéficier bientôt les malades.
INDICATIONS DE L’EXAMEN
Les indications documentées en cancérologie sont nombreuses
et diverses. Certaines sont incluses dans l’autorisation de mise
sur le marché (AMM) du FDG en France dont a bénéficié, en
novembre 1998, la préparation commerciale Flucis®, ce qui
n’est pas actuellement le cas du cancer de l’ovaire.
La TEP au [18F]-fluoro-2-désoxyglucose
dans le cancer de l’ovaire
●J.N. Talbot*, K. Kerrou*, D. Grahek*, N. Younsi*, V. De Beco*, C. Colombet-Lamau*, Y. Petegnief*, F. Montravers*
* Service de médecine nucléaire et centre TEP AP-HP, hôpital Tenon, 4, rue de
la Chine, 75020 Paris.

21
La Lettre du Gynécologue - n° 266 - novembre 2001
Pour tout cancer, y compris, donc, pour celui de l’ovaire,
l’examen au [18F]-FDG a potentiellement une place dans le
dépistage systématique, le diagnostic de malignité devant une
tumeur détectée par la clinique, l’imagerie et/ou l’endoscopie
mais sans preuve histologique à la biopsie, dans le diagnostic
de l’extension métastatique lorsque le cancer est démontré,
dans celui de l’efficacité ou de l’inefficacité des mesures thé-
rapeutiques, en particulier dès les premiers cycles d’une chi-
miothérapie, dans le diagnostic et l’extension de la récidive,
soit en cas de récidive occulte (augmentation du CA 125 sans
localisation par les examens conventionnels d’imagerie), soit
en cas de récidive connue pouvant bénéficier d’une thérapeu-
tique ciblée.
Réalisation pratique de l’examen
Selon nous, la décision d’indiquer l’examen (actuellement,
donc, hors AMM) doit reposer sur le choix thérapeutique que
son résultat permettra. Non seulement le clinicien doit se trouver
RL
RL
Thorax-
abdomen
Abdomen-
pelvis
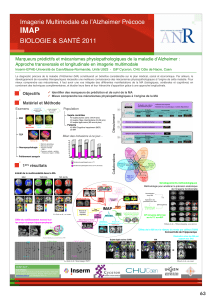
Figure 1. Récidive occulte d’un cancer de l’ovaire : augmentation de la
concentration sérique de CA 125 et imagerie conventionnelle négative.
L’examen TEDC révèle une carcinose péritonéale confirmée histologi-
quement.
R
Corps
entier
3D
Thorax-abdomen
3D
Abdomen-pelvis
L
Figure 3. Augmentation progressive du CA 125 chez une patiente ayant
des antécédents de cancer de l’ovaire. La seule anomalie visualisée en
TDM est un épanchement pelvien (flèche blanche). L’examen TEDC
révèle plusieurs foyers de récidive métastatique (flèches rouges) confir-
més histologiquement.
Figure 2. Récidive occulte d’un cancer de l’ovaire : augmentation de la
concentration sérique de CA 125 et imagerie conventionnelle négative.
L’examen TEDC révèle un nodule pelvien néoplasique isolé de 20 x 15 x
10 mm, confirmé histologiquement.
transverse sagittal coronal
Figure 5. Récidive de cancer de l’ovaire. Bilan d’extension de la réci-
dive réalisé grâce à la caméra TEP dédiée. On découvre un foyer méta-
statique dans la partie supérieure du thorax gauche.
Décembre 1997 Août 1998
Thorax Thorax
Abdomen Abdomen
Figure 4. Récidive occulte de cancer de l’ovaire. L’examen TEDC révèle
deux foyers de récidive néoplasique, ce qui fait choisir un traitement
par chimiothérapie. Celle-ci permet d’obtenir une rémission complète,
illustrée par la normalisation de l’examen TEDC au bout de 8 mois
(images de droite), confirmée 24 mois plus tard par la normalité de la
concentration sérique de CA 125 et des examens d’imagerie conven-
tionnelle.

devant un problème ou un doute diagnostique, mais il doit avoir
prévu son attitude thérapeutique selon que la TEP au FDG ne
montre pas de foyer pathologique, ou bien qu’elle témoigne
d’un seul foyer pathologique ou de foyers étendus et dispersés.
Il convient donc que l’indication soit bien pesée, a fortiori en
cas de diabète, qui rend l’examen moins sensible.
La prise de rendez-vous est comparable à celle de toute scin-
tigraphie. Il convient de s’assurer de l’absence de grossesse
en cours. En cas d’allaitement, on conseille généralement de
le suspendre pendant 12 heures au maximum, bien que des
données récentes indiquent que la dose de rayonnement déli-
vrée au nourrisson est si faible que l’allaitement pourrait être
poursuivi sans modification (2). La patiente doit être à jeun
depuis au moins 6 heures, tout en conservant un bon apport
hydrique (pas de boissons sucrées) ; bien entendu, elle ne
doit pas être perfusée avec une solution contenant du glu-
cose, celui-ci entrant en compétition avec son analogue
radioactif. Il ne faut pas qu’elle effectue d’effort musculaire
intense (sport) dans la journée qui précède l’examen, car les
muscles activés fixent le FDG. Lors de son arrivée dans le
service, elle est allongée et mise au repos musculaire ; 15 à
20 minutes plus tard, on met en place une perfusion intravei-
neuse de 0,5 litre de sérum physiologique par laquelle on
injecte du Spasfon®, en l’absence de réaction secondaire
connue de la patiente à ce produit, afin de diminuer le tonus
de la fibre musculaire lisse intestinale. On injecte ensuite le
[18F]-FDG. La patiente reste allongée sans lire ni parler, tou-
jours afin d’éviter l’incorporation du FDG dans les muscles.
Une heure après, la fixation du [18F]-FDG a atteint son pla-
teau, et on réalise l’examen : la patiente est invitée à vider sa
vessie et elle est positionnée pour son examen dans la
machine TEP ou TEDC. Elle peut ensuite repartir par ses
propres moyens, et même conduire : le [18F]-FDG ne donne
ni malaise, nausée ou somnolence, ni aucun autre effet
secondaire (3).
Les images sont reconstruites grâce à une station de travail
informatique, imprimées, interprétées par le médecin
nucléaire, et l’examen est adressé au prescripteur. Les images
issues de la caméra TEP dédiée sont reconstruites et analysées
avec et sans la correction de l’atténuation, qui est inhomogène
au sein des tissus traversés par les photons.
PERFORMANCES CLINIQUES DE L’EXAMEN AU FDG
Caractérisation d’une masse tumorale annexielle et
bilan d’extension
La caractérisation d’une masse tumorale annexielle comme
étant maligne et son bilan d’extension sont possibles lors du
même examen TEP au FDG, comme l’a montré Hubner (4)
dès 1993. Son étude démontre également les meilleures sensi-
bilité et spécificité de l’examen par rapport à la TDM et aussi
sa capacité à déceler d’autres tumeurs malignes à localisation
gynécologique : métastases d’un cancer de l’œsophage, can-
cer de la vulve, du vagin et, plus souvent, de l’utérus. Des
études sont venues confirmer celle de Hubner (5-8). Parmi les
causes de faux positifs, on retrouve la salpingite, comme toute
infection aiguë, certains cystadénomes et kystes du corps
jaune et certaines lésions d’endométriose ; parmi celles de
faux négatifs, les cancers de faible malignité et l’adénocarci-
nome mucineux (6). La sensibilité de la TEP apparaît comme
particulièrement faible dans l’étude de Grab (7/12 = 58 %)
(7), ce qui s’explique par l’inclusion de carcinomes de stade I,
dont deux sur trois ont été décelés, et surtout de tumeurs
limites (borderline), que l’auteur considère comme malignes,
et dont une sur cinq a été décelée. La modalité concurrente
paraît être l’IRM, qui obtient une exactitude légèrement supé-
rieure dans l’étude de Grab (77 % en TEP contre 84 % en
TDM) (7) comme dans les résultats préliminaires de Kubik-
Huch sur sept patientes (8).
En regroupant les résultats de ces quatre études, on constate
une intéressante valeur prédictive négative de 96 sur 106
(91 %), qui peut permettre, dans certains cas particuliers, une
simple surveillance en cas d’examen négatif. Même si la
valeur prédictive positive au niveau de la tumeur elle-même
est moins bonne (42/70 = 60 %), il ressort de notre expérience
qu’un examen positif, surtout s’il montre une dissémination
des foyers de fixation du FDG, est un élément important pour
le choix de la stratégie chirurgicale.
Recherche et localisation des récidives, évaluation de
leur traitement
La TEP au FDG est utile dans le bilan tumoral résiduel post-
thérapeutique, étant donné la faible sensibilité de l’imagerie
traditionnelle (TDM, IRM et échographie), du fait, en particu-
lier, des remaniements postchirurgicaux au niveau du pelvis et
de l’abdomen. L’examen clinique est souvent peu contributif
et l’élévation de la concentration sanguine de CA 125 incons-
tante. La TEP au FDG, par sa valeur prédictive positive éle-
vée, devrait s’avérer utile avant la laparotomie exploratrice
post-thérapeutique, soit en évitant les gestes opératoires
inutiles chez les patientes se présentant à un stade avancé
(figure 3), soit en guidant le chirurgien dans les autres cas. La
figure 4 illustre l’intérêt de l’examen pour contrôler de façon
non invasive l’efficacité de la chimiothérapie d’une récidive
multifocale.
Elle est également utile dans le suivi, lors de toute suspicion
de récidive. Le rôle favorable sur la survie de la chirurgie de
cytoréduction est désormais mis en avant, ce qui implique
une méthode sensible et fiable d’imagerie pour en diminuer
les risques (9). La TEP au FDG permet de détecter une réci-
dive alors que l’imagerie conventionnelle reste négative
(maladie occulte [figures 1-4]) et même avant l’élévation de
la concentration circulante des marqueurs tumoraux (15).
Notre équipe et celle de Lieberman ont rapporté, chez
37 patientes au total, une sensibilité de 100 % pour la détec-
tion de la récidive pelvienne grâce à une caméra hybride
TEDC (18, 19) (figure 2). La détection des récidives méta-
statiques à distance est également très efficace : 30 patientes
sur les 57 de Smith (14) et, dans la courte série de
10 patientes en suspicion de récidive de Kubik-Huch (8), une
métastase isolée du côlon transverse visible uniquement en
TEP. Un cas similaire de détection d’une métastase thora-
cique est illustré par la figure 5.
DOSSIER
22
La Lettre du Gynécologue - n° 266 - novembre 2001

La maladie microscopique reste toutefois une source de faux
négatifs (5 cas négatifs sur 6 examens au FDG dans l’étude de
Karlan [11]), quelle que soit la modalité d’imagerie utilisée
(TEP, IRM ou TDM). La carcinose péritonéale (figure 1), fré-
quemment constituée de granulations très infracentimétriques,
n’est détectée par TEP au FDG que dans 7 cas sur 16 (sensibi-
lité de 44 %) dans l’expérience de Turlakow (20) ; elle a donné
lieu à 2 faux négatifs sur les 5 patientes en récidive de l’étude
de Romer (5). Bohdiewicz, en 1995, constate que le seul avan-
tage, par rapport à la TEP, de l’immunoscintigraphie à l’aide
d’un anticorps anti-ACE marqué à l’indium-111, l’Oncoscint®,
concerne la visualisation de la carcinose dans deux cas contre
zéro (21). L’étude de Baum confirme cependant que les per-
formances de la TEP au FDG sont globalement supérieures à
celles de l’immunoscintigraphie (12) et surtout que, si la détec-
tion de la carcinose péritonéale est possible en immunoscinti-
graphie, elle donne lieu à de nombreux faux positifs respon-
sables d’une mauvaise spécificité. De plus, cet examen n’est
pas utilisable pour déceler les métastases hépatiques (21).
Chez les 14 patientes en récidive étudiées par Baum, la TEP
mettait en évidence 61 lésions contre 19 seulement pour
l’immunoscintigraphie et 11 pour la TDM.
En regroupant les résultats publiés par les équipes utilisant
des machines TEP dédiées (10-17), on aboutit à une sensibi-
lité de 100 sur 115 (87 %) et à une spécificité de 52 sur
57 (91 %).
Notre expérience porte actuellement sur 49 examens TEDC
évaluables, avec comme référence l’histologie ou un suivi de
plus d’un an. La TEDC a une sensibilité de 36 sur 39 (92 %) et
une spécificité de 10 sur 10 (100 %), contre respectivement
19 sur 39 (49 %) et 4 sur 10 (40 %) pour l’imagerie conven-
tionnelle. Dans le cas particulier des récidives occultes, où la
sensibilité de l’imagerie conventionnelle est de zéro par défini-
tion, la sensibilité de la TEDC a été de 17 sur 19 (89 %).
Enfin, une étude américaine a montré que la TEP au FDG per-
mettait, en évitant des laparotomies itératives, de réaliser une
économie moyenne de 8 500 $ par patiente (14).
Impact sur la prise en charge de la patiente
L’impact de l’examen TEP au FDG sur la prise en charge des
patientes suivies pour un cancer de l’ovaire n’avait à notre
connaissance été rapporté que par Nakamoto et al. sous la
forme d’un résumé (22). L’examen avait entraîné une modifi-
cation de l’attitude thérapeutique chez 4 patientes sur 16
adressées pour suspicion de récidive et 1 patiente sur 14 chez
qui l’examen était réalisé à titre systématique. Nous avons
effectué l’étude de l’impact de l’examen en adressant un ques-
tionnaire au clinicien demandeur. L’étude a porté sur les exa-
mens effectués à l’hôpital Tenon durant l’année 2000, soit
grâce à la machine TEP dédiée (dans le cadre d’un protocole
loi Huriet sur le cancer de l’ovaire), soit grâce à la machine
“hybride” TEDC. La fréquence de modification de l’attitude
thérapeutique (tableau) est élevée dans le cancer de l’ovaire
comme dans les autres cancers gynécologiques (sein et utérus),
plus de 60 % contre environ 50 % en général, ce qui reflète un
impact thérapeutique très fort pour un examen diagnostique
unique.
CONCLUSION
Les données de la littérature montrent que les performances
diagnostiques de l’examen au FDG sont comparables dans le
cancer de l’ovaire à celles observées dans les indications déjà
reconnues : cancer du poumon, du côlon, ORL, mélanome et
lymphome. Elles sont très supérieures à celles de l’imagerie
conventionnelle pour le suivi de la maladie. L’exemple des
“récidives occultes”, où l’imagerie conventionnelle est prise en
défaut alors que la sensibilité de l’examen au FDG est de 89 %
dans notre expérience, l’illustre. L’expérience de quelques
équipes, la nôtre en particulier, précise que la détection TEDC
conserve son utilité clinique à l’examen au FDG. L’impact de
l’examen en termes de modification de l’attitude thérapeutique
est considérable (plus de 60 % pour les trois cancers étudiés),
parmi les plus élevés dans les indications cancérologiques de
la TEP. Tout cela doit logiquement conduire à une extension
de l’AMM du FDG qui englobe le cancer de l’ovaire. ■
23
La Lettre du Gynécologue - n° 266 - novembre 2001
Tableau. Impact de l’examen au FDG sur l’attitude thérapeutique.
Expérience de l’hôpital Tenon durant l’année 2000.
Ovaire Total Global Global
gynécologie TEP TEDC
Non 9 23 (37 %) 123 (51 %) 84 (48 %)
Chirurgie 4 8 (13 %) 45 (19 %) 23 (13 %)
remplacée
Chirurgie
indiquée 5 8 (13 %) 29 (12 %) 26 (15 %)
ou modifiée
Radiothérapie 1 4 (7 %) 9 (4 %) 10 (6 %)
indiquée
ou modifiée
ou arrêtée
Arrêt 1 3 (5 %) 7 (3 %) 6 (3 %)
chimiothérapie
Chimiothérapie 3 7 (11 %) 17 (7 %) 10 (6 %)
indiquée
Chimiothérapie 2 10 (16 %) 13 (5 %) 16 (9 %)
modifiée
Total 25 63 243 175
Taux 64 % 63 % 49 % 52 %
de modification
Remerciements
Nous remercions l’équipe des manipulateurs et manipulatrices du service
de médecine nucléaire de l’hôpital Tenon, et tout particulièrement leurs
surveillantes Mmes Marie-Louise et Machacek, pour leur aide quotidienne
et leur intérêt pour la TEP au FDG.
Nous remercions tous nos correspondants cliniciens qui nous ont adressé leurs
patientes et ont participé à l’évaluation de l’impact thérapeutique de l’examen,
en particulier les Prs S. Uzan, V. Izraël, E. Touboul et J.P. Lotz de l’hôpital
Tenon, le Pr A. de Gramont de l’hôpital Saint-Antoine et le Pr F. Lécuru de
l’hôpital Georges-Pompidou, ainsi que toutes leurs équipes médicales.

DOSSIER
24
La Lettre du Gynécologue - n° 266 - novembre 2001
RÉFÉRENCES BIBLIOGRAPHIQUES
1. Kerrou K, Gausachs L, Montravers F et al. La gamma-caméra à détection de
coïncidence. I Principe, compromis, utilisation pour la scintigraphie conven-
tionnelle. RBM 1998 ; 20 : 123-31.
2. Hicks R, Binns D, Stabin M. Pattern of uptake and excretion of 18F-FDG in
the lactating breast. J Nucl Med 2001 ; 42 (8) : 1238-42.
3. Silberstein EB. Prevalence of adverse reaction to positron emitting radio-
pharmaceuticals in nuclear medicine. J Nucl Med 1998 ; 39 : 2190-2.
4. Hubner KF, McDonald TW, Niethammer JG et al. Assessment of primary
and metastatic ovarian cancer by positron emission tomography (PET) using 2-
[18F]deoxyglucose (2-[18F]FDG). Gynecol Oncol 1993 ; 51 : 197-204.
5. Romer W, Avril N, Dose J et al. Metabolic characterization of ovarian
tumors with positron-emission tomography and 18F-fluorodeoxyglucose. Rofo
Fortschr Geb Rontgenstr Neuen Bildgeb Verfahr 1997 ; 166 (1) : 62-8.
6. Zimny M, Schroder W, Wolters S et al. 18F-fluorodeoxyglucose PET in ova-
rian carcinoma : methodology and preliminary results. Nuklearmedizin 1997 ;
36 (7) : 228-33.
7. Grab D, Flock F, Stohr I et al. Classification of asymptomatic adnexal
masses by ultrasound, magnetic resonance imaging, and positron emission
tomography. Gynecol Oncol 2000 ; 77 (3) : 454-9.
8. Kubik-Huch RA, Dorffler W, von Schulthess GK et al. Value of (18F)-FDG
positron emission tomography, computed tomography, and magnetic resonance
imaging in diagnosing primary and recurrent ovarian carcinoma. Eur Radiol
2000 ; 10 (5) : 761-7.
9. Chen LM, Karlan BY. Recurrent ovarian carcinoma : is there a place for
surgery ? Semin Surg Oncol 2000 ; 19 (1) : 62-8.
10. Casey MJ, Gupta NC, Muths CK. Experience with positron emission tomogra-
phy (PET) scans in patients with ovarian cancer. Gynecol Oncol 1994 ; 53 : 331-8.
11. Karlan BY, Hawkins R, Hoh C et al. Whole-body positron emission tomo-
graphy with 2-[18F]-fluoro-2-deoxy-D-glucose can detect recurrent ovarian
carcinoma. Gynecol Oncol 1993 ; 51 : 175-81.
12. Baum RP, Niesen A, Schröder O et al. A prospective evaluation of whole
body FDG-PET, CT scan and immunoscintigraphy in the detection of ovarian
carcinoma recurrences. Eur J Nucl Med 1998 ; 25 : 942 (abstr. OS-424).
13. Shankar LK, Alavi A, Mangan C et al. The clinical role of FDG-PET in the
management of residual and/or recurrent ovarian carcinoma. J Nucl Med
1998 ; 39 (5) : A1097.
14. Smith GT, Hubner KF, Mac Donald T, Thie JA. Potential cut savings by
F18-FDG PET as an alternative to second look laparotomy in ovarian cancer. J
Nucl Med 1998 ; 35 : 249 (abstr. 1 096).
15. Garcia MJ, Crespo-Jara AA, Marti JM et al. Impact of whole body PET
FDG in the early detection or recurrent ovarian cancer. J Nucl Med 1999 ; 40
(5) : A 424.
16. Yuan CC, Liu RS, Wang PH, Ng HT, Yeh SH. Whole-body PET with (fluo-
rine-18)-2-deoxyglucose for detecting recurrent ovarian carcinoma. Initial
report. J Reprod Med 1999 ; 44 (9) : 775-8.
17. Torizuka T, Nobezawa S, Nagashima S et al. Role of whole body FDG-PET
in management of patients with recurrent ovarian cancers. J Nucl Med 2000 ;
41 (5) : A 1318.
18. Lieberman G, Hilson AJW, Buscombe JR et al. Initial findings of a hybrid
positron emission tomography camera system for the identification and monito-
ring of ovarian cancer. J Nucl Med 1999 ; 40 (5) : 134 (résumé A 541).
19. Kerrou K, Montravers F, Grahek D et al. Detection of recurrence of ova-
rian cancer using F18-FDG scan performed on a dual-head coincidence
gamma-camera (CDET). Clin Pos Imag 2000 ; 3 (4) : 186.
20. Turlakow A, Yeung HW, Macapinlac HA et al. Peritoneal carcinosis - the
role of FDG-PET. J Nucl Med 2000 ; 41 (5) : A 140.
21. Bohdiewicz PJ, Scott GC, Juni JE et al. Indium-111 Oncoscint®CR/OV and
F18-FDG in colorectal and ovarian carcinoma recurrences. Early observa-
tions. Clin Nucl Med 1995 ; 20 (3) : 230-6.
22. Nakamoto Y, Saga T, Ishimori T et al. Clinical contribution of FDG-PET
for follow-up patients with gynecological malignancies. J Nucl Med 2000 ; 41
(S5) : 301.
GRAND PRIX ÉDITORIAL DU SNPM
Notre groupe de presse VIVACTIS MEDIA a
participé au Grand Prix Éditorial 2001
organisé par le Syndicat National de la
Presse Médicale (SNPM) le 4 octobre
dernier. La Lettre du Gynécologue a été
nominée pour le prix du meilleur éditorial
de réflexion pour Qualité, éthique, informa-
tion, précaution, accréditation et moi et moi et moi, du Pr
Yves Dumez
(La Lettre du Gynécologue, 2001 ; 259 : 3-4)
.
Un grand bravo à l’auteur
pour cette distinction.
1
/
5
100%