M Prise en charge de la douleur : avancées thérapeutiques en 2002 D

244
La Lettre du Cancérologue - volume XI - n° 6 - novembre-décembre 2002
DOULEUR
LA DOULEUR DU CANCER : SOUS-ESTIMÉE,
SOUS-ÉVALUÉE, SOUS-TRAITÉE
Malgré la mise en place de nombreux programmes de forma-
tion sur la prise en charge de la douleur du cancer, tant dans le
cadre de la formation continue que des études médicales et
infirmières, la douleur du cancer reste sous-estimée, sous-éva-
luée et sous-traitée. Pourtant, les recommandations de l’OMS
ont été largement diffusées, et les moyens thérapeutiques sont
disponibles dans les pays occidentaux. Les pays en voie de
développement restent néanmoins très défavorisés, particuliè-
rement en ce qui concerne l’accès aux traitements opioïdes.
Lors d’une évaluation préalable à la mise en place d’un pro-
gramme de prise en charge de la douleur dans un hôpital belge,
Payen et al. retrouvent une douleur modérée à sévère chez
40 % des 291 patients hospitalisés. Trente-trois d’entre eux
n’avaient aucun traitement antalgique.
Dans une étude britannique portant sur l’utilisation des res-
sources et le coût des soins palliatifs, Guest et al. montrent que
chez des patients cancéreux en phase avancée, depuis l’initiation
d’un traitement opioïde jusqu’à leur décès, la douleur n’est pas
prise en charge de façon adaptée malgré l’existence de recom-
mandations.
Au Portugal, Freitas et al. ont analysé les réponses de
450 médecins et infirmières à un questionnaire évaluant les
thérapeutiques antalgiques les plus fréquemment prescrites,
leur efficacité clinique et les difficultés de prescription. Les
Prise en charge de la douleur :
avancées thérapeutiques en 2002
Congrès mondial de la douleur (San Diego, 17-22 août 2002)
● M Luu*, MT Gatt*
* Unité douleur-soins palliatifs, hôpital Avicenne, 93009 Bobigny, Cedex.
algré les moyens disponibles, les recommandations et les nombreux programmes de formation, la
douleur du cancer reste encore sous-estimée, sous-évaluée et sous-traitée.
Le développement de modèles animaux de douleur du cancer suscite beaucoup d’espoir. Ils
devraient permettre une meilleure connaissance des mécanismes mis en jeu dans la douleur du cancer et
la mise au point de thérapeutiques antalgiques plus spécifiques.
Devant la résistance de certaines douleurs aux thérapeutiques habituelles, et particulièrement aux
opioïdes, un système de classification des syndromes douloureux permettant de prédire les difficultés de
prise en charge serait particulièrement utile. C’est dans ce but que le système de classification d’Edmonton
a été développé.
La douleur est un déterminant important de la qualité de vie des patients cancéreux. C’est également un
prédicteur potentiel des résultats cliniques, un marqueur de l’évolution de la maladie et la base de la com-
paraison des traitements. Les échelles multidimensionnelles de la douleur ont leur place au côté des
échelles de qualité de vie dans les études cliniques, les résultats obtenus avec chacune d’elles n’étant pas
superposables.
La grande majorité des douleurs cancéreuses répondent aux thérapeutiques recommandées par l’OMS.
Dans les cas de douleurs peu sensibles aux traitements opioïdes systémiques, plusieurs stratégies de
prise en charge ont été proposées. Deux d’entre elles sont développées : la rotation des opioïdes et les
blocs cœliaques.
M

245
La Lettre du Cancérologue - volume XI - n° 6 - novembre-décembre 2002
résultats montrent que la douleur du cancer tant en hospitalisa-
tion qu’en ambulatoire est souvent sous-évaluée, traitée de
façon insuffisante avec des thérapeutiques ne suivant pas des
protocoles établis.
En France, deux enquêtes téléphoniques menées par Brasseur
et Larue, l’une en 1992, l’autre en 2001, auprès d’oncologues
et de médecins généralistes, montrent qu’en dix ans, les
connaissances sur les douleurs du cancer et les traitements
morphiniques se sont améliorées, particulièrement chez les
oncologues. Néanmoins, la prévalence de la douleur du cancer
reste encore estimée comme faible, et la réticence à prescrire
un morphinique est toujours présente, même si elle a diminué.
Afin d’étudier dans quelle mesure la douleur pouvait être sous-
estimée, Knotkova et al. ont demandé à 71 patients présentant
un cancer intra-abdominal d’évaluer leur douleur à l’aide
d’une échelle numérique en 6 points et d’un questionnaire
d’évaluation multidimensionnel. Dans le même temps, les
médecins évaluaient la douleur de leur patient à l’aide d’une
échelle numérique et de l’indice de Karnofsky. Les résultats
montrent que l’évaluation de la douleur par les médecins
reflète l’auto-évaluation des patients uniquement chez ceux
dont l’indice de Karnofsky est supérieur à 30, alors qu’elle est
sous-estimée pour les patients ayant un indice de Karnofsky
inférieur. La présence d’une plus grande souffrance émotion-
nelle et d’une diminution du bien-être, qui contribuent à l’éva-
luation de la douleur chez ces patients, pourraient expliquer la
sous-estimation des médecins.
Une autre cause de la faible utilisation des morphiniques reste
la peur de la pharmacodépendance, comme le montrent Guer-
rero et al. dans une étude portant sur un questionnaire rempli
par 110 patients cancéreux ambulatoires présentant une dou-
leur sévère traitée par opioïdes. Cette peur est renforcée par
l’attitude négative de la famille vis-à-vis de la morphine. Pour
les auteurs, l’information du patient et de sa famille devrait
être un prérequis avant toute initiation d’un traitement opioïde.
UN MODÈLE ANIMAL DE DOULEUR DU CANCER
Le développement de modèles animaux de douleur du cancer
constitue une avancée importante, tant pour la compréhension
des mécanismes que pour la mise au point de thérapeutiques
spécifiques, tout particulièrement pour les douleurs par enva-
hissement nerveux périphérique et/ou osseux, qui constituent
75 % des douleurs cancéreuses chroniques et qui sont parmi
les plus difficiles à gérer.
Mantyh et al. ont développé un modèle de cancer osseux chez
la souris en injectant des cellules tumorales dans l’espace
médullaire du fémur. Ces cellules entraînent une destruction
osseuse ainsi que des comportements douloureux spontanés et
provoqués similaires à ceux retrouvés chez les patients présen-
tant des douleurs osseuses cancéreuses.
Sur le plan neurochimique, les auteurs démontrent non seule-
ment une réorganisation au niveau des afférences primaires et
de la moelle qui reçoivent les messages du membre envahi.
Cette réorganisation semble différente de celle observée dans
les modèles de douleur chronique inflammatoire et neuro-
pathique chez la souris.
Par des études de biologie cellulaire, pharmacologique et com-
portementale, les auteurs mettent en évidence le rôle de trois
facteurs dans la douleur osseuse : activité ostéoclastique exces-
sive, production de COX-2, génération d’un état de douleur
neuropathique, et ils montrent que les thérapeutiques qui
bloquent la douleur du cancer atténuent la réorganisation
neurochimique induite par la tumeur.
CARACTÉRISATION DES DOULEURS DU CANCER
Un certain nombre de patients cancéreux présentent des syn-
dromes douloureux difficiles à gérer. La possibilité de disposer
d’un système de classification des douleurs du cancer reconnu
sur le plan international, comme le système TNM pour les
tumeurs cancéreuses, permettrait d’identifier précocement ces
patients et d’améliorer ainsi leur évaluation et leur prise en
charge, qui s’avère souvent longue et complexe.
C’est dans ce but que Fainsinger et al. ont développé le sys-
tème de classification d’Edmonton (Canada). Plusieurs fois
remanié, il se compose actuellement de 5 facteurs qui auraient
une valeur pronostique concernant le contrôle de la douleur.
Constituent des facteurs de mauvais pronostic : 1) les douleurs
à composante neuropathique (compression, envahissement,
destruction ou dysfonctionnement du système nerveux central
et périphérique) ; 2) les douleurs incidentes ou provoquées par
le mouvement ou une autre activité, alors que le patient est
bien soulagé au repos ; 3) la nécessité de doses rapidement
croissantes d’opioïdes due à une augmentation de la douleur
sous-jacente ou à un phénomène de tolérance ; 4) l’existence
d’une détresse psychologique avec dépression et/ou anxiété
majeures ; 5) des antécédents d’abus de drogue ou d’alcool
pouvant prédisposer à une addiction aux opioïdes. D’autres
travaux sont encore nécessaires pour que cet outil puisse obtenir
un agrément international.
Utilisant uniquement les caractéristiques de la douleur,
Caraceni et al. ont comparé les syndromes douloureux dus au
carcinome à ceux du sarcome chez 220 patients consécutifs
(145 carcinomes, 57 sarcomes). Ils montrent que les syn-
dromes douloureux dus au sarcome sont plus difficiles à gérer
avec les opioïdes. Bien qu’il n’existe pas de différence d’inten-
sité de la douleur au repos et aux mouvements entre les deux
groupes, les douleurs neuropathiques et l’infiltration de la
paroi thoracique et des tissus mous des membres inférieurs
sont plus fréquents dans le sarcome. De plus, à contrôle antal-
gique comparable, ce dernier nécessite des doses plus impor-
tantes de morphinique.
ÉVALUATION MULTIDIMENSIONNELLE DE LA DOULEUR
DU CANCER
Parmi les nombreux questionnaires multidimensionnels dispo-
nibles pour l’évaluation de la douleur du cancer, le Brief Pain
Inventory (BPI) reste l’un des outils les plus largement utilisés.

246
La Lettre du Cancérologue - volume XI - n° 6 - novembre-décembre 2002
Il permet d’évaluer la douleur et son retentissement sur l’acti-
vité, l’humeur, la marche, les relations avec les autres, le som-
meil et la joie de vivre. Dans une étude portant sur 100 patients
cancéreux douloureux, Jage et al. montrent que cet instrument
pratique et facile d’utilisation permet de détecter une améliora-
tion du soulagement de la douleur, mais également une dimi-
nution de son retentissement comportemental et psychologique
quelques jours après la modification des thérapeutiques, ce que
ne permet pas un questionnaire de qualité de vie utilisé dans le
même temps.
Dans un essai clinique multicentrique randomisé, Thaler et al.
montrent tout l’intérêt de l’évaluation non seulement de la qua-
lité de vie mais également de la douleur. Les questionnaires
utilisés ont été le Brief Pain Inventory (BPI) et le Functional
Assessment of Cancer Therapy (FACT). Les évaluations ont
été réalisées le premier jour de chacun des 4 cycles de chimio-
thérapie : cisplatine versus cisplatine + paclitaxel dans les can-
cers du col avancés. Les résultats montrent que le BPI prédit
de façon significative la réponse à la chimiothérapie, tandis
que le BPI et le FACT (PWB : bien-être physique) prédisent
fortement la survie. La moitié des 269 patients inclus ont com-
plété les questionnaires à 4 reprises. Parmi eux (la plupart
“répondeurs”), le BPI s’est amélioré, alors que le PWB ne
s’est pas modifié. Parmi les patients n’ayant pas répondu à
tous les questionnaires (la plupart “non-répondeurs”), le BPI
s’est aggravé sous cisplatine relativement à cisplatine + pacli-
taxel, tandis que le PWB s’est aggravé légèrement dans les
deux bras de chimiothérapie.
LES RECOMMANDATIONS DE L’OMS :
TOUJOURS D’ACTUALITÉ
Les recommandations de l’OMS concernant le traitement
symptomatique de la douleur du cancer restent toujours
d’actualité. Elles permettent de soulager la grande majorité des
patients cancéreux, comme le montrent Pawe, Wosniak et al.
dans une étude portant sur 435 patients admis en unité de soins
palliatifs.
En se basant sur une étude rétrospective portant sur
235 patients cancéreux douloureux, Lesnoy et al. montrent que
75,6 % d’entre eux ont bien répondu aux traitements antal-
giques. Les auteurs soulignent que la connaissance pharmaco-
logique des opioïdes et des traitements adjuvants ainsi que la
compréhension des mécanismes de la douleur rendent possible
un soulagement adapté de la douleur chez la plupart des
patients.
La morphine est l’opioïde du niveau III de l’OMS le plus lar-
gement utilisé. Ses modalités d’utilisation sont bien codifiées,
mais certains aspects sont encore fondés sur une opinion
d’experts. Klepstad et al. , dans une étude randomisée en
double aveugle sur 37 patients ayant une douleur faible à
modérée, montrent qu’une titration simplifiée utilisant la mor-
phine à libération prolongée une fois par jour est d’efficacité
comparable et n’a pas plus d’effets secondaires qu’une titra-
tion utilisant la morphine à libération immédiate donnée toutes
les quatre heures. Ces résultats devraient entraîner la révision
de la recommandation selon laquelle la titration doit être réali-
sée avec la morphine à libération immédiate.
Dans une étude portant sur 87 patients douloureux bien équili-
brés par la morphine i.v., Mahmoud et al. confirment la
persistance d’un bon contrôle de la douleur pour la majorité
des patients par la morphine per os en utilisant le rapport de
conversion i.v./p.o. 1:3, un rapport inférieur entraînant une
aggravation de la douleur. La sévérité des effets secondaires
n’est pas affectée par le rapport de conversion.
Fallon rappelle que les recommandations de l’OMS ne doivent
pas être considérées comme une alternative aux autres straté-
gies de prise en charge de la douleur du cancer mais doivent
faire partie intégrante de l’ensemble des stratégies disponibles.
Radiothérapie, chimiothérapie, chirurgie, physiothérapie, blocs
anesthésiques, relaxation, neurostimulation transcutanée, acu-
puncture... sont des stratégies qui doivent être utilisées dans
des situations individuelles appropriées.
STRATÉGIES CLINIQUES DE PRISE EN CHARGE
DES DOULEURS PEU SENSIBLES AUX TRAITEMENTS
OPIOÏDES SYSTÉMIQUES
La prise en charge de la douleur cancéreuse chez certains
patients s’avère problématique dès lors qu’elle répond mal aux
opioïdes. Les variations individuelles de la réponse aux
opioïdes sont probablement d’origine multifactorielle. Parmi
les facteurs en rapport avec le syndrome douloureux, on
retrouve un mécanisme neuropathique et les douleurs inci-
dentes. Les facteurs en rapport avec le patient peuvent être une
détresse psychologique ainsi que tout facteur prédisposant un
patient aux effets secondaires, comme un âge avancé ou la
défaillance d’un organe majeur. Devant l’impossibilité
d’atteindre un soulagement satisfaisant sans effet secondaire
intolérable lors d’une titration graduelle, Portenoy propose
quatre stratégies :
– augmenter les doses du même opioïde en renforçant le traite-
ment des effets secondaires lorsque cela est possible ;
– changer d’opioïde afin d’obtenir un rapport analgésie/effet
secondaire plus favorable : la rotation des opioïdes ;
– utiliser des traitements pharmacologiques qui diminuent la
demande en opioïdes systémiques : co-administration d’un
analgésique non opioïde ou d’un traitement adjuvant tel que
ceux cités dans les recommandations de l’OMS. Certains syn-
dromes douloureux nécessitent des traitements spécifiques,
comme les douleurs neuropathiques, les douleurs osseuses, les
douleurs abdominales des syndromes occlusifs ;
– utilisation des techniques non pharmacologiques : anesthé-
siques, neurochirurgicales, neurostimulation, physiothérapie,
psychothérapies, autres (acupuncture...). Très variées, ces thé-
rapies sont très différentes dans leurs indications et leur mise
en œuvre.
Devant l’absence d’essais cliniques comparatifs, le choix
d’une thérapie ou d’une autre relèvera du meilleur jugement
clinique. Celui-ci pourra être guidé par une évaluation soi-
DOULEUR

247
La Lettre du Cancérologue - volume XI - n° 6 - novembre-décembre 2002
gneuse du patient et du syndrome douloureux et par une bonne
connaissance des indications des techniques disponibles. Des
réévaluations régulières permettront de repérer des modifica-
tions du syndrome douloureux pouvant nécessiter de nouvelles
explorations et un changement dans la stratégie thérapeutique.
De même, une connaissance précise des comorbidités phy-
siques (évolution de la maladie, état du patient) et psycho-
sociales permettra de clarifier le but des soins et leur faisabilité.
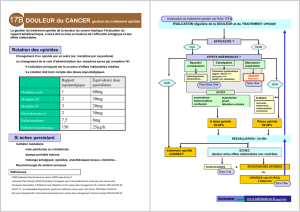
LA ROTATION DES OPIOÏDES
Les effets secondaires des opioïdes peuvent limiter la dose de
titration avec, comme conséquence, un mauvais soulagement
de la douleur. La rotation des opioïdes utilisant des doses équi-
analgésiques diminuerait les toxicités en maintenant ou en
améliorant le contrôle de la douleur.
Les recommandations préconisées par Portenoy tentent de
réduire le risque d’un relatif sous- ou surdosage alors qu’un
opioïde est arrêté et l’autre administré. Il préconise pour plus
de sécurité d’utiliser des doses inférieures à celles des tables
d’équi-analgésie. En effet, tant l’analgésie que les effets secon-
daires peuvent être supérieurs à ceux attendus. Ce phénomène
est expliqué par une tolérance croisée incomplète entre les
opioïdes et/ou par le fait que les doses équi-analgésiques ont été
calculées lors d’essais à dose unique. Il existe néanmoins deux
exceptions : le patch de fentanyl (facteur de sécurité intégré
dans la table) et la méthadone (réduction importante : de 75 à
90 %). Pour les patients âgés ou qui présentent une maladie
cardio-pulmonaire, hépatique ou rénale sévère, la dose du nouvel
opioïde pourra être réduite.
L’étude de Walsh et al. va dans ce sens. Dans leur série, 40 des
275 patients présentant principalement un cancer du sein ou du
poumon ont subi une rotation des opioïdes pour neurotoxicité,
absence de contrôle de la douleur ou nausées et vomissements
sévères. Après rotation, les effets secondaires ont diminué et le
contrôle de la douleur s’est amélioré avec une dose équi-
analgésique inférieure à celle prédite.
Dans une autre étude portant sur 800 patients en soins pallia-
tifs, Muller-Busch et al. analysent la fréquence, les raisons et
l’efficacité de la rotation des opioïdes. Celle-ci est plus fré-
quente chez les patients hospitalisés que chez les patients
ambulatoires. Les critères de sélection ne sont pas clairs et
dépendent des préférences personnelles. Ils sont le plus sou-
vent en rapport avec des raisons médicales en unité de soins
palliatifs (USP) (analgésie insuffisante et/ou effets secondaires
intolérables) alors que, pour les patients ambulatoires, ils sont
plutôt en rapport avec des raisons non médicales (peur des
opioïdes, compliance ou problème économique). La fréquence
de succès est supérieure en USP, bien que les problèmes de
douleur semblent être plus complexes, en rapport avec le stade
de la maladie. Les auteurs soulignent que, si la rotation des
opioïdes est une option thérapeutique empirique utile, les rai-
sons médicales et non médicales qui conduiront à la décision
d’y recourir ou non doivent être soigneusement prises en
compte.
LES BLOCS CŒLIAQUES NEUROLYTIQUES
Les techniques invasives conservent leur intérêt dans les dou-
leurs intenses rebelles en phase avancée de la maladie. Les
blocs neurolytiques utilisent des substances comme l’éthanol
ou le phénol et peuvent être précédés par un bloc aux anesthé-
siques locaux. Ils doivent être réalisés par des anesthésistes
entraînés, et le patient doit être bien informé des complications
possibles (déficit sensoriel et/ou moteur). En cas d’efficacité,
la diminution du traitement opioïde doit se faire par quart ou
par tiers de la dose initiale afin de prévenir la somnolence et la
dépression respiratoire.
Parmi les blocs neurolytiques, le bloc cœliaque est particuliè-
rement intéressant dans les douleurs des cancers du pancréas,
qui répondent souvent mal aux traitements opioïdes optimisés.
Wong et al. ont étudié l’effet d’un bloc cœliaque neurolytique
sur le soulagement de la douleur, la qualité de vie et la survie
des patients présentant un cancer du pancréas inopérable dans
une étude clinique prospective randomisée, en double aveugle.
Cent patients ont eu soit un bloc cœliaque neurolytique soit
l’injection d’un placebo. À une semaine, la douleur et la qua-
lité de vie ont été améliorées de façon significative dans les
deux groupes, avec un soulagement de la douleur significative-
ment plus important chez les patients ayant reçu le bloc. Avec
le temps, la douleur reste significativement moins importante
dans le groupe bloc. Cependant, la consommation d’opioïdes,
la qualité de vie et la survie totale ne diffèrent pas de façon
significative entre les deux groupes.
Dans une autre étude, Lejcko et al. montrent que le bloc
cœliaque neurolytique peut être utilisé de façon répétitive avec
un effet prolongé. La plupart des patients ont toujours besoin
d’opioïdes, mais à des doses nettement inférieures.
RÉFÉRENCES BIBLIOGRAPHIQUES
1. Brasseur L, Larue F. Surveys on oncologists and primary care physicians’
attitudes toward pain control and morphine prescribing in France : changes
from 1992 to 2001. Boulogne, France, abstr. 679.
2. Caraceni A et al. Pain syndromes due to sarcoma. A pilot study. Milan, Ita-
lie, abstr. 885.
3. Fainsinger RL. TNM classification system for cancer pain ? Edmonton,
Canada, abstr. 713.
4. Fallon MT. Advances in pharmacological management of cancer pain. Glas-
gow, Royaume-Uni, abstr. 713.
5. Fallon MT. Management of cancer pain with evidence for each strategy.
Glasgow, Royaume-Uni, An update review : refresher course syllabus.
6. Freitas DM et al. Insufficiencies, facts and contradictions in oncologic pain
therapeutics. Funchal-Madeira, Portugal, abstr. 1630.
7. Guerrero C et al. Fear of addiction in a palliative care population. Bogota,
Colombia, abstr. 160.
8. Guest JF et al. Treatment patterns and resource costs of palliative care for
advanced cancer patients starting strong opioid treatment with 12-hourly sus-
tained-release morphine or transdermal fentanyl. Northwood, Royaume-Uni,
abstr. 688.
9. Jage J et al. Guideline-based analgesic treatment in patients with cancer
pain : prospective quality assurance of analgesic effectiveness. Mainz, Alle-
magne, abstr. 1632.
10. Klepstad P et al. Immediate or sustained-release morphine for dose-finding
during start of morphine to cancer patients : a randomised, double-blind trial.
Trondheim, Norvège, abstr. 1634.

248
La Lettre du Cancérologue - volume XI - n° 6 - novembre-décembre 2002
DOULEUR
11. Knotkova H et al. Unrecognized emotional suffering in cancer patients of
lower Karnofsky performance status accounts for underestimation of their pain
by medical staff. Prague, République tchèque, abstr. 1392.
12. Lejcko J et al. The effect of plexus coeliacus neurolysis on severe cancer
abdominal pain. Pilsen, République tchèque, abstr. 585.
13. Lema JM. Invasive analgesia techniques for avanced cancer pain. Buffalo,
États-Unis, abstr. 713.
14. Lesnoy II et al. Cancer pain treatment in an Ukrainian pain relief depart-
ment. Zhitomir, Ukraine, abstr. 1638.
15. Mahmoud FA et al. The relative milligram potency ratio of intravenous to
oral morphine in cancer pain. Cleveland, États-Unis, abstr. 156.
16. Mantyh P. A mechanism-based understanding of cancer pain. Minneapolis,
États-Unis, abstr. 1082.
17. Muller-Busch HC et al. Opioid rotation in palliative care - Frequency, rea-
sons and success. Berlin, Allemagne, abstr. 158.
18. Pawe S, Wosniak P et al. The role of opioids in treatment of advanced can-
cer pain. Wroclaw, Pologne, abstr. 1618.
19. Payen MC et al. Implementation of a pain management program. Brussells,
Belgique, abstr. 704.
20. Portenoy RK. Clinical strategies for the management of cancer pain poorly
responsive to systemic opioid therapy. New York, États-Unis, An update review :
refresher course syllabus.
21. Thaler HT et al. Pain assessment as a prognostic factor and quality of life
component in advanced cervical cancer. New York, États-Unis, abstr. 1069.
22. Walsh D et al. Parenteral opioid rotation in advanced cancer. Cleveland,
États-Unis, abstr. 1623.
23. Wong GY et al. The effect of neurolytic celiac plexus block on pain relief,
quality of life, and survival in patients with unresecable pancreatic cancer : a
prospective, double-blinded, randomized clinical trial. Rochester, États-Unis,
abstr. 169.
Merci d’écrire nom et adresse en lettres majuscules
❏Collectivité .................................................................................
à l’attention de..............................................................................
❏Particulier ou étudiant
M., Mme, Mlle ................................................................................
Prénom..........................................................................................
Pratique : ❏hospitalière ❏libérale ❏autre...........................
Adresse e-mail...............................................................................
Adresse postale.............................................................................
......................................................................................................
Code postal........................Ville ……………………………………
Pays................................................................................................
Tél..................................................................................................
Merci de joindre votre dernière étiquette-adresse en cas de réabonnement,
changement d’adresse ou demande de renseignements.
ÉTRANGER (AUTRE QU’EUROPE)
FRANCE/DOM-TOM/EUROPE ❐110
€collectivités
❐92
€particuliers
❐65
ێtudiants*
*joindre la photocopie de la carte
❐90
€collectivités
❐72
€particuliers
❐45
ێtudiants*
*joindre la photocopie de la carte
LK6 Vol XI
OUI, JE M’ABONNE AU MENSUEL La Lettre du Cancérologue
Total à régler .......... €
À remplir par le souscripteur
À remplir par le souscripteur
À découper ou à photocopier
✂
ABONNEMENT : 1 an
+
ETPOUR 10 €DE PLUS !
10
€
, accès illimité aux 26 revues de notre groupe de presse disponibles sur notre site
vivactis-media.com (adresse e-mail gratuite)
+
R
RELIURE
ELIURE
❐10
€
avec un abonnement ou un réabonnement
MODE DE PAIEMENT
❐
carte Visa, Eurocard Mastercard
N°
Signature : Date d’expiration
❐
chèque
(à établir à l'ordre de La Lettre du Cancérologue)
❐
virement bancaire à réception de facture
(réservé aux collectivités)
EDIMARK - 62-64, rue Jean-Jaurès - 92800 Puteaux
 6
6
1
/
6
100%