Lire l'article complet

Hémopathies malignes
chez les sujets
immunodéprimés
dossier thématique
Abonnez-vous sur
www.edimark.fr
Correspondances en Onco-Hématologie - Vol. VIII - n° 3 - Mai-juin 2013
125
RÉSUMÉ
Summary
»
Les déficits immunitaires primitifs (DIP) constituent un groupe
génétiquement hétérogène de maladies prédisposant aux
infections récurrentes, aux manifestations dysimmunitaires et,
dans certains cas, à la survenue de néoplasies. Les hémopathies
malignes lymphoïdes sont observées dans de nombreuses formes
de DIP, surtout lorsque l’immunité cellulaire est compromise. La
survenue d’un lymphome chez un adulte jeune, aux antécédents
infectieux multiples avec des manifestations dysimmunitaires
ou développementales, doit faire rechercher l’existence d’un
DIP sous-jacent, surtout si l’hémopathie est associée à un virus
à potentiel transformant. L’établissement de ce diagnostic peut
avoir en effet des conséquences − parfois à très court terme −
sur la prise en charge du malade.
Mots-clés : Déficits immunitaires primitifs − Lymphome.
Primary immunodeficiencies (PID) are a heterogeneous
group of diseases characterized by a predisposition to
recurrent infections, dysimmunity and neoplasia. Lymphoid
malignancies occur in many forms of PID, especially
when cellular immunity is compromised. The occurrence
of lymphoma in a young adult with a history of multiple
infectious events, dysimmunity, developmental defects or
harbouring an oncogenic virus, should lead to investigate
for an underlying PID. The diagnosis of PID associated to
lymphoma has indeed a direct impact on the management
of the patient.
Keywords : Primary immunodeficiency – Lymphoma.
L
es déficits immunitaires primitifs (DIP) consti-
tuent un groupe génétiquement hétérogène
de maladies affectant le développement et/ou
la fonction des différentes composantes du système
immunitaire inné et adaptatif. Les DIP sont, le plus sou-
vent, des maladies monogéniques suivant un héritage
mendélien, mais certains ont une origine plus complexe,
polygénique. La pénétrance de la maladie, sa variabilité
d’expression et les interactions entre facteurs géné-
tiques et environnementaux contribuent également
à la diversité phénotypique des DIP. À l’exception du
déficit en IgA, toutes les formes de DIP sont rares avec
une prévalence globale d’environ 1 pour 10 000 nais-
sances vivantes. Ils sont caractérisés par une suscepti-
bilité accrue aux infections − récurrentes et/ou graves
− assortie d’une sensibilité particulière à divers types
d’agents pathogènes en fonction de la nature du déficit
immunitaire (1). Cependant, la susceptibilité aux infec-
tions n’est qu’un aspect d’un phénotype souvent plus
complexe : manifestations dysimmunitaires, troubles
développementaux, susceptibilité au développement
de cancers. Cette prédisposition à la survenue d’une
néoplasie − hématologique ou extra-hématologique
− résulte de l’interaction entre les processus physio-
pathologiques inhérents à la maladie de base (défaut
d’apoptose, maladie cassante), à un défaut d’immuno-
surveillance et, parfois, à la rencontre avec un virus
transformant (figure, p. 126).
Si, la plupart du temps, la survenue d’une néoplasie
hématologique émaille le suivi d’un patient dont le DIP
est déjà diagnostiqué, il est important de savoir évoquer
une pathologie immunitaire sous-jacente devant cer-
taines présentations de lymphome : adulte jeune, anam-
nèse infectieuse riche, antécédents de manifestations
dysimmunitaires ou développementales, association à
des virus transformants (virus Epstein-Barr [EBV], virus
herpès humain 8 [HHV-8]). Le diagnostic d’un DIP chez
un patient présentant un lymphome peut, en effet,
avoir des conséquences, à court ou à long terme, sur
la prise en charge du malade.
Quels déficits immunitaires héréditaires
faut-il rechercher lors du diagnostic
de lymphome chez un adulte jeune ?
Which primary immune deficiencies should be sought for when
diagnosing lymphoma in a young adult?
F. Touzot*
* Biothérapie, hôpital
Necker Enfants-Malades,
Paris.

Hémopathies malignes
chez les sujets
immunodéprimés
dossier thématique
Correspondances en Onco-Hématologie - Vol. VIII - n° 3 - Mai-juin 2013
126
Dans la suite de cet article, les principaux DIP à évoquer
devant la survenue d’un lymphome chez l’adulte jeune
seront abordés (tableau). La liste des DIP évoqués ci-
dessous est loin d’être exhaustive, un grand nombre
n’étant encore pas formellement caractérisés sur le
plan génétique. Il faut garder à l’esprit que tout déficit
immunitaire combiné peut se compliquer éventuelle-
ment d’une néoplasie hématologique.
Syndrome lymphoprolifératif
lié à l’X de type 1
Le syndrome lymphoprolifératif lié à l’X de type 1
(XLP-1), ou syndrome de Purtilo, est un déficit immu-
nitaire primitif caractérisé par une vulnérabilité particu-
lière vis-à-vis du virus EBV. Il est causé par des mutations
dans le gène SH2D1A codant SAP (SLAM-associated
protein), une protéine adaptatrice qui se lie au domaine
intracellulaire des récepteurs de la famille SLAM expri-
mée dans les lymphocytes T, NK et NKT (2). La plupart
des patients sont asymptomatiques avant de rencontrer
l’EBV. Cependant, 20 % des sujets peuvent présenter
des infections ORL et respiratoires à répétition révé-
lant une hypogamma globulinémie. La manifestation
clinique la plus fréquente est le syndrome d’activation
macrophagique (55 % des patients), le plus souvent
induit par une primo-infection EBV, dont l’issue est
généralement fatale. D’autres manifestations plus rares
ont été rapportées, comme des aplasies médullaires,
des vascularites, des granulomatoses lymphomatoïdes
pulmonaires ou des gastrites chroniques (3, 4). Environ
15 à 30 % des patients déficients en SAP présentent
un lymphome comme première manifestation de la
maladie avec un âge moyen au diagnostic de 15 ans
(extrêmes : 2-40 ans). Les hémopathies lymphoïdes
ne sont pas forcément associées à l’EBV, mais elles
surviennent généralement plus tôt chez les patients
infectés par l’EBV que chez les patients non infectés (2).
La majorité des lymphomes sont de type B non hodg-
kiniens (LNH-B), avec 50 à 60 % de lymphomes de type
Burkitt associés à l’EBV. D’autres variétés histologiques
ont été décrites : LNH-B immunoblastique, LNH-B à
grandes cellules (12 %), lymphome de Hodgkin (LH),
lymphome T. La localisation iléo-cæcale est préféren-
tielle, mais des atteintes cervicales, spinales ou céré-
brales ont été décrites (3, 4). Les anomalies biologiques
retrouvées chez les patients sont les suivantes :
✓
hypogammaglobulinémie, trait immunologique
le plus fréquent (67 % des cas), nécessitant une subs-
titution par immunoglobulines intraveineuses (IVIG) ;
✓absence de cellules NKT ;
✓
cytotoxicité anormale des lymphocytes cytotoxiques
spécifiques de l’EBV ;
✓diminution de la cytotoxicité NK ;
✓
déficit de la mort cellulaire induite par réactivation.
La cytométrie en flux offre un moyen rapide de dépis-
tage des patients XLP-1 par la détection de l’expression
intracytoplasmique de la protéine SAP (5). Le lien entre
la déficience en SAP et la lymphomatogenèse n’est pas
encore clairement établi. Il est possible que ce processus
soit relié à la perte de la fonction pro-apoptotique de
SAP dans les cellules T et B ainsi qu’à une altération de
la surveillance antitumorale en lien avec l’absence de
cellules NKT et les défauts de cytotoxicité NK et CD8+
observés chez ces patients (6).
Syndrome lymphoprolifératif
avec auto-immunité
Le syndrome lymphoprolifératif avec auto-immunité
(ALPS) est caractérisé par l’apparition précoce d’un
syndrome tumoral bénin (splénomégalie, lymphadéno-
pathie), d’une hypergammaglobulinémie polyclonale,
de l’accumulation d’une population polyclonale de
lymphocytes T matures TCRαβ CD4–CD8– (aussi appelés
lymphocytes T double négatifs [DN]), d’une cytopénie
multilignée auto-immune et d’un risque accru de lym-
phome (7). Dans les ALPS, l’homéostasie lymphocytaire
est perturbée par un défaut de l’apoptose cellulaire
médiée par le récepteur de surface Fas (ou CD95). La
majorité des patients présentant un ALPS sont porteurs
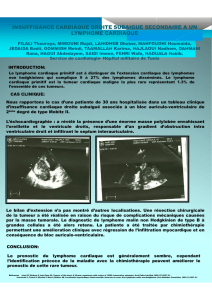
Figure. Facteurs contribuant à la lymphomagenèse au cours du déficit immunitaire primitif.
Altération génétique de gènes
suppresseurs de tumeurs
et d’oncogène
Défaut d’apoptose (ALPS)
Instabilité génétique (A-T)
Immunodéficience
Altération de
l’immuno-surveillance
Virus transformant
EBV
HHV-8
Lymphome

Correspondances en Onco-Hématologie - Vol. VIII - n° 3 - Mai-juin 2013
127
Quels déficits immunitaires héréditaires faut-il rechercher
lors du diagnostic de lymphome chez un adulte jeune ?
de mutations germinales hétérozygotes dominantes
dans le gène TNFRSF6 codant Fas (ALPS-FAS). Fait inté-
ressant, 10 à 15 % des patients présentent des mutations
somatiques hétérozygotes dominantes de TNFRSF6
(ALPS-sFAS). Par ailleurs, des mutations germinales des
gènes codant Fas ligand (Fas-L), les caspases 8 et 10,
Tableau. Déficits immunitaires primitifs associés à la survenue d’un lymphome.
Maladie Défaut
génétique
(transmission)
Signes évocateurs Anomalies
immunologiques
Explorations simples
permettant d’orienter
le diagnostic
Type de lymphome
Fréquence
Syndrome
lymphopro-
lifératif lié
à l’X de type1
(XLP-1)
SH2D1A (XL) Syndrome
hémophagocytaire
Splénomégalie
Infections
à répétition
Hypogammaglobulinémie 67 %
Déficit en lymphocytes NKT
Phénotypage des NKT
Mesure de la mort cellulaire
par réactivation
Marquage intracytoplasmique
en cytométrie en flux
LNHB, Burkitt
majoritairement EBV+
Fréquence : 30 %
Syndrome
lymphopro-
lifératif avec
auto-immunité
(ALPS)
TNFRSF6 (AD)
Autres (RA)
Syndrome tumoral
Cytopénie auto-
immune
Hypergammaglobulinémie
Excès de lymphocytes T TCRαβ
+ DN
Élévation des lymphocytes T DN,
de Fas-L, de l’IL-10 et de
la vitamine B12 plasmatique
LNH et LH
Fréquence : 7 %
Syndrome
de Buckley
STAT3 (AD) Dysmorphie, scoliose,
hyperlaxité
Infections ORL et cuta-
nées à pyogènes
Hyperéosinophilie
Hyper IgE
Lymphopénie B mémoire
LNH B essentiellement
Fréquence : 7 %
Maladies cassantes
Ataxie
Télangiectasie
ATM (AR) Ataxie
Télangiectasie
Anomalie pigmenta-
tion cutanée
Infections
récurrentes
Lymphopénie T surtout CD4+
et CD4 naïfs
Diminution des sous-classes IgG,
absence d’IgA
Cytogénétique sur
lymphocytes :
instabilité chromosomique
spontanée ou induite (MMC),
Test de sensibilité aux rayons X
ou MMC sur fibroblastes
LNH T et B
Fréquence : 15 %
Syndrome de
Nijmegen
NBS1 (AR) Microcéphalie
Retard mental modéré
Dysmorphie faciale
Taches café au lait
Lymphopénie T
Hypo- ou agammaglobulinémie
Cytogénétique sur lymphocytes :
instabilité chromosomique
spontanée ou induite (MMC),
Test de sensibilité aux rayons X
ou MMC sur fibroblastes
LNH T et B
Fréquence : 50 %
Wiskott-
Aldrich
WASP (XL) Eczéma
Infections
récurrentes
Thrombopénie
Lymphopénie T surtout CD4+
et CD4 naïfs
Proliférations lympho cytaires
diminuées (mitogènes + anti-
gènes)
Hypergammaglobulinémie
Diminution des réponses
anticorps aux antigènes poly-
saccharidiques et protéiques
Volume plaquettaire < 6 fl
Marquage intracytoplasmique
en cytométrie en flux (formes
sans expression protéique)
LNH B EBV+
Fréquence : 9 %
Cartilage Hair
hypoplasia
(CHH)
RMRP (RA) Nanisme – chondro-
dysplasie
Cheveux fins et
clairs
Infections
récurrentes
Anémie/neutropénie
Lymphopénie surtout CD4
Proliférations lympho cytaires
diminuées
(mitogènes + antigènes)
Ig variables
Radiographies du squelette LNH
Fréquence : 7%
Déficit
Immunitaire
Commun
Variable (DICV)
Majoritairement
non identifiées
(variable)
Infections respiratoires
répétées
Manifestations auto-
immunes
Atteinte granulo-
mateuse
Lymphopénie surtout CD4
Lymphopénie B-mémoire
LNH B
Fréquence globale de
8 % mais variable selon
le sous-groupe
AD: autosomique dominant; AR: autosomique récessif; DN: doubles négatifs; EBV: virus d’Epstein-Barr; FACS: Fluorescence-activated cell sorting (cytométrie en flux); Ig: immunoglobuline; LNH: lymphome non
hodgkinien; LH: lymphome de Hodgkin; MMC: mitomycine C; XL: liée à l’X.

Hémopathies malignes
chez les sujets
immunodéprimés
dossier thématique
Correspondances en Onco-Hématologie - Vol. VIII - n° 3 - Mai-juin 2013
128
ainsi que les gènes NRAS et KRAS ont été identifiés
chez un petit nombre de patients atteints du même
syndrome (8). Les éléments caractéristiques du diagnos-
tic biologique sont le nombre élevé de lymphocytes T
TCRαβ+ CD4– CD8– DN ainsi que des taux plasmatiques
élevés de Fas-L, d’interleukine 10 (IL-10) et de vitamine
B12 (7). Les manifestations d’ALPS-FAS débutent dans
les premières années de la vie, à 2,5 ans en moyenne.
L’analyse de 17 cas français d’ALPS-FAS diagnostiqués
à l’âge adulte a montré que 12 des 17 patients avaient
présenté leurs premiers symptômes pendant l’enfance,
les 5 autres patients étant devenus symptomatiques
après l’âge de 16 ans (9). Des symptômes cliniques
inhabituels et l’apparition de mutations somatiques
de Fas étaient responsables du diagnostic tardif de
ces patients. À l’âge adulte, les symptômes de l’ALPS
peuvent être moins marqués, ce qui rend le diagnostic
encore plus difficile pour des soignants non familiers
des DIP. De nombreux diagnostics différentiels ont été
évoqués dans les cas adultes : syndrome d’Evans, mala-
die de Castleman atypique, lymphadénopathie angio-
immunoblastique ou maladie de Rosai-Dorfman. Au
cours d’une étude observationnelle française menée sur
90 patients (8), il a été constaté la survenue de 7 cas de
lymphomes ; l’âge médian de survenue était de 24,5 ans
(extrêmes : 14-51 ans). Trois cas de LH ont été rapportés
et 4 cas de LNH-B à grandes cellules, dont 1 lymphome
EBV induit survenu sous traitement par immunosup-
presseur. Il est intéressant de noter que la plupart des
patients développant un lymphome sont porteurs d’une
mutation impliquant la partie intracytoplasmique (en
particulier le Death Domain) de Fas. Le processus de
lymphomatogenèse pourrait résulter de la conjugaison
d’une activation lymphocytaire B chronique, favori-
sée par l’augmentation de l’IL-10 circulante, du déficit
d’apoptose et d’un défaut d’immuno-surveillance.
Syndrome de Buckley ou syndrome
hyper-IgE autosomique dominant
Le syndrome hyper-IgE est un DIP complexe décrit pour
la première fois par S. Davis et al. en 1966 sous le nom
de “syndrome de Job”, puis par R.H. Buckley en 1972,
qui avait noté pour la première fois son association à
un taux plasmatique d’IgE très élevé. Ce syndrome, de
transmission autosomique dominante, confère une
immunodéficience sélective accompagnée d’une sus-
ceptibilité aux infections cutanées et pulmonaires à bac-
téries pyogènes (staphylocoque doré, pneumocoque
et Haemophilius influenzae essentiellement), ainsi que
des candidoses cutanéo-muqueuses chroniques (10).
Les autres anomalies notables sont une dysmorphie
faciale (front proéminent, prognathisme ou rétrogna-
thisme, traits grossiers), un retard à la chute des dents de
lait, des anomalies osseuses (ostéopénie, craniosténose,
scoliose), et une hyperextensibilité ligamentaire. Les
principaux signes biologiques sont une hyperéosinophi-
lie associée à un taux d’IgE sériques élevé. Le syndrome
de Buckley est causé par des mutations hétérozygotes
du gène STAT3 avec effet dominant négatif (11). STAT3
est une molécule assurant la transduction du signal
en aval de récepteurs de facteurs de croissance et de
cytokines (dont gp130, récepteur aux cytokines de la
famille IL-6). Les patients STAT3-déficients présentent
un déficit en lymphocytes TH17 produisant de l’IL-17A
et de l’IL-22, ainsi qu’une diminution des lymphocytes
B mémoires CD27+ circulants (12). Dans une étude
de cohorte française menée sur 60 patients STAT3-
déficients (10), l’âge moyen au diagnostic était de 17 ans
(extrêmes : 1 mois- 46 ans). La variabilité clinique était
considérable entre les individus portant la même muta-
tion et cela jusques et y compris au sein d’une même
famille. Quatre patients de la cohorte (7 %) ont présenté
un LNH au cours du suivi avec un âge moyen de début
de 21 ans (extrêmes : 8-34 ans), 2 cas de lymphome
de Burkitt (1 forme disséminée et 1 forme localisée),
1 cas de lymphome anaplasique diffus ALK-négatif, et
1 lymphome B à grandes cellules. Aucune association
avec l’EBV n’a été observée. Vingt-deux cas avaient été
rapportés précédemment dans la littérature avec un âge
de début comparable : 6 lymphomes T, 12 lymphomes
B et 4 LH. La plupart n’étaient pas associés à l’EBV. STAT3
étant un oncogène impliqué dans le développement
d’hémopathies malignes et de néoplasies diverses (13),
la survenue d’un lymphome chez les patients STAT3-
déficients est paradoxale et reste à ce jour sans expli-
cation physiopathologique claire.
Maladies “cassantes”
Le cadre des maladies “cassantes” regroupe l’ensemble
des pathologies héréditaires caractérisées par un défaut
de réparation de l’ADN. Ces pathologies sont souvent
évoquées devant la triade atteinte neurologique
− microcéphalie et/ou ataxie cérébelleuse − déficit
immunitaire et prédisposition au cancer. Des anoma-
lies cutanées comme des taches dépigmentées, une
hyperpigmentation, ou encore des taches café au lait
sont souvent associées. Le spectre phénotypique peut
cependant être très variable pour une même maladie et
pour un même type de mutation. Les étiologies molé-
culaires sont nombreuses et impliquent des facteurs

Correspondances en Onco-Hématologie - Vol. VIII - n° 3 - Mai-juin 2013
129
intervenant dans diverses voies de réparation de l’ADN,
signalisation des dommages à l’ADN, réparation des
cassures doubles brins d’ADN ou réparation des ponts
interbrins d’ADN.
L’ataxie-télangiectasie (AT) est l’exemple type de mala-
die cassante avec une fréquence d’environ 1 pour
100 000 enfants (14). Elle associe dans sa forme typique
un déficit combiné portant surtout sur l’immunité
humorale, une ataxie cérébelleuse progressive, des
télangiectasies cutanéo-muqueuses, et un risque accru
de cancers. L’AT est une maladie récessive autosomique
due à la mutation du gène ATM codant une protéine
kinase ubiquitaire qui joue un rôle clé dans le contrôle
de la réparation des cassures doubles brins de l’ADN. Des
formes variantes plus rares ont été décrites, liées à des
mutations dans d’autres facteurs de réparation. Il s’agit
de mutations de MRE11 donnant un syndrome AT-like,
ou de NBS1 responsable du syndrome de Nijmegen
caractérisé par une microcéphalie majeure (15, 16). Le
diagnostic de maladie cassante peut être fortement
suspecté par des dosages sériques (alpha-fœtopro-
téine élevée dans l’AT), des tests cytogénétiques (test
de cassures, translocations spontanées 7-14 caractéris-
tiques) ou des tests plus complexes de radiosensibilité
sur fibroblastes.
Dans l’AT, le risque de lymphome, essentiellement LNH,
est accru de 250 à 750 fois par rapport à la population
générale avec un risque d’hémopathie lymphoïde T
4 à 5 fois plus important que celui d’hémopathie B
(17). Seuls 11 cas de LH ont été décrits sur une série
de 412 patients atteints d’AT. L’instabilité génomique est
l’acteur prépondérant de la lymphomagenèse dans ce
groupe de pathologies. Il est crucial de pouvoir évoquer
le diagnostic rapidement car la radiothérapie et cer-
taines chimiothérapies (alkylants) doivent être utilisées
avec prudence du fait de la radiosensibilité.
Déficit immunitaire commun variable
Le déficit immunitaire commun variable (DICV) est un
cadre nosologique regroupant des DIP caractérisés
par un défaut de production d’anticorps et une hypo-
gammaglobulinémie. Le terme DICV n’est en rien un
diagnostic. Il englobe un groupe hétérogène de mala-
dies qui ont cependant des caractéristiques cliniques
communes : infections ORL et respiratoires récurrentes,
manifestations auto-immunes, atteinte granulomateuse
et syndrome lymphoprolifératif (18). Si certaines causes
génétiques de DICV ont été identifiées (ICOS, TACI,
BAFF-R et CD19, par exemple), la plupart des patients
restent sans diagnostic moléculaire précis. Les anoma-
lies immunologiques les plus fréquentes, en dehors
de l’hypogammaglobulinémie, sont un défaut de cel-
lules B-mémoires et une diminution des lymphocytes T
CD4 (18). Dans une cohorte américaine (n = 473), 8,2 %
des patients ont présenté une hémopathie lymphoïde. Il
s’agissait essentiellement de LNH-B (33 cas sur 39), avec
une prédominance féminine. Les lymphomes observés
dans les DICV sont généralement extraganglionnaires,
de type B, et le plus souvent EBV négatifs (19). La gravité
clinique, infectieuse, dysimmunitaire et proliférative du
DICV est liée à la profondeur du déficit immunitaire com-
biné (DIC). Ainsi, parmi les 313 patients de la cohorte
française DEFI, 28 sujets (8,9 %) présentaient un DIC
profond défini par la survenue d’une infection oppor-
tuniste et/ou un taux de CD4 inférieur à 200/mm3 (20).
Cette population de patients, plus fréquemment issus
d’unions consanguines, présente une fréquence accrue
de splénomégalie (64 % versus 31 %), d’atteinte granu-
lomateuse cutanée (43 % versus 10 %), de pathologie
gastro-intestinale (75 % versus 42 %) et de lymphome
(29 % versus 4 %). Dans ce sous-groupe, 5 patients ont
présenté des lymphomes. Trois de ces 5 lymphomes
étaient associés à l’EBV, 2 étaient des LNH et le dernier
était un LH. Les lymphomes non liés à l’EBV étaient des
LNH-B et -T. Quatre lymphomes ont été diagnostiqués
plus de 2 ans après le premier symptôme évocateur
d’une hypogammaglobulinémie. L’âge moyen de sur-
venue était de 30 ans (extrêmes : 17-62 ans).
Syndrome de Wiskott-Aldrich
Le syndrome de Wiskott-Aldrich est un DIP rare carac-
térisé par une triade associant une thrombopénie à
petites plaquettes (< 6 fl), un eczéma et un déficit immu-
nitaire combiné entraînant des infections récurrentes.
Le syndrome est causé par des mutations hémizygotes
du gène WAS (Xp11.22-23), codant la protéine Was (ou
WASP [Wiskott-Aldrich Syndrome Protein]) [21]. Cette
protéine est exprimée exclusivement dans les cellules
hématopoïétiques et joue un rôle majeur dans la poly-
mérisation de l’actine, la réorganisation du cytosque-
lette, la transduction du signal et l’apoptose (22). Les
mutations dans le gène WAS conduisent à un large
éventail de phénotypes (23), allant d’une forme bénigne
− la thrombocytopénie liée à l’X −, à l’archétype sévère
du syndrome de Wiskott-Aldrich. Le déficit immunitaire
est caractérisé par une lymphopénie progressive de
gravité variable. Les proliférations lymphocytaires T
sont diminuées en réponse aux mitogènes et antigènes
vaccinaux. Sur le plan humoral, les taux d’IgG sont nor-
maux ou élevés, avec une élévation des IgA et des IgE.
Quels déficits immunitaires héréditaires faut-il rechercher
lors du diagnostic de lymphome chez un adulte jeune ?
 6
6
1
/
6
100%