VIGI-PHARMA Bulletin d`informations pharmaceutiques Service

VIGI-PHARMA, N°9, Octobre 2007, Page
1
A
A
p
pr
ro
op
po
os
s
d
de
e
l
l’
’i
is
so
ot
tr
ré
ét
ti
in
no
oï
ïn
ne
e
(
(
R
RO
OA
AC
CC
CU
UT
TA
AN
NE
E
*
*,
,
P
PR
RO
OC
CU
UT
TA
A
*
*,
,
C
CU
UR
RA
AC
CN
NE
E
*
*)
)
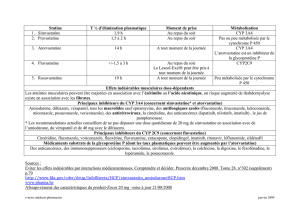
L’isotrétinoïne est un dérivé de la vitamine A utilisé dans l’acné sévère. Sa tératogénécité est
bien connue et implique une contraception obligatoire et un test de grossesse mensuel pour
les fe
mmes traitées. Ce produit est aussi responsable d’une augmentation des transaminases et
des lipides, effet qui s’avère dose-dépendant et fréquent
(pancréatites et hépatites ont été
rapportées), d’où la nécessité d’effectuer un suivi régulier des transamina
ses et des lipides
plasmatiques. Des effets indésirables psychiatriques de type dépression sévère avec tentative
de suicide, et des accidents vasculaires (infarctus, accidents vasculaires cérébraux) ont aussi été
notifiés. Un traitement par l’isotrétinoïne
orale n’est absolument pas anodin, les patients
doivent en être informés. Prescrire, 2006, n°274, 503
Folia Pharmacotherapeutica, 34, mars 2007, http://www.cbip.be (Centre belge d’information pharmacothérapeutique)
O
Os
se
el
lt
ta
am
mi
iv
vi
ir
r
(
(
T
TA
AM
MI
IF
FL
LU
U
*
*)
)
:
:
Q
Qu
ue
el
ls
s
r
ri
is
sq
qu
ue
es
s
?
?
L’Oseltamivir est un antiviral, utilisé dans le traitement préventif et curatif de la grippe chez l’adulte
et l’enfant de plus de 1an. Il s’avère peu utile dans la grippe saisonnière et que ce soit en prévention
ou en curatif il n’a pas démontré d’efficacité sur l’importance des signes cliniques ou leur morbidité.
Son efficacité est incertaine dans la grippe aviaire : aucune différence de mortalité entre patients
traités et non traités n’a été mise en évidence. En Mars 2007, le RCP du produit est modifié pour y
ajouter des effets indésirables neuropsychiatriques graves pouvant survenir chez les enfants et
adolescents. En effet, comportements suicidaires, hallucinations, convulsions, délires et troubles du
comportement (ayant pu entraîner le décès) ont été notifiés depuis sa mise sur le marché,
essentiellement au Japon (pays où il est largement prescrit dans le traitement de la grippe
saisonnière). Ces effets s’ajoutent aux effets indésirables cutanés graves dont des syndromes de
Lyell. La balance bénéfice-risque de l’Oseltamivir est en équilibre bien instable.
Tous sous Tamifluence ?, Bulletin du CRIM,Jan/Fev 2007
Tamiflu and neuropsychiatric disturbance in adolescents, BMJ, 2007 ; 334 : 1232-1233
Communiqué de presse, Mars 2007,
Afssaps/ http://afssaps.sante.fr
A
Ar
rr
rê
êt
ts
s
d
de
e
c
co
om
mm
me
er
rc
ci
ia
al
li
is
sa
at
ti
io
on
n
AGREAL
*
(Véralipride)
HALDOL
* 20 mg (Halopéridol)
SILOMAT
* (Clobutinol)
V
VI
IG
GI
I-
-P
PH
HA
AR
RM
MA
A Bulletin d’informations pharmaceutiques
Service Pharmacie
N° 9 / Octobre 2007 Centre Hospitalier Spécialisé du Jura
Rédacteurs : Christel Chalmendrier (Poste 1284) et Guy Martin (Poste 1397)
E
ED
DI
IT
TO
OR
RI
IA
AL
L
L’été s’en est allé (mais était –
il vraiment venu ?), l’automne
s’en vient, et après les
bienfaits laxatifs des
mirabelles (bien meilleures
qu’un
FORLAX
*), nous allons
profiter des noix et noisettes
de nos forêts dont la
consommation ne nuit pas à
notre santé, bien au contraire.
On ne pourrait en dire autant
de certains médicaments
dont la mise sur le marché ne
garantit pas qu’ils soient
toujours sans risque pour le
consommateur, heu pardon
le patient. Et si on a pas mal
siècles de recul sur la
consommation des noix, il
n’en est pas vraiment de
même pour les médicaments.
Même si une nouvelle
molécule met 10 ans pour
arriver sur le marché, cela ne
veut pas dire que l’on connaît
forcément tout d’elle, d’où
parfois quelques surprises
dans les premières années de
mise sur le marché. A
l’époque où il existe une forte
tendance à aller plus vite
dans tous les domaines, s’il y
a un domaine où réflexion,
patience et vigilance sont
nécessaires c’est bien celui de
la santé, non ?
Méditons-y et profitons des
noix, tiens !
V
VE
EI
IL
LL
LE
E
S
SA
AN
NI
IT
TA
AI
IR
RE
E
●
AGREAL
* (Véralipride) : enfin retiré du marché. Le véralipride est un médicament
neuroleptique utilisé dans les bouffées de chaleur liées à la ménopause alors qu’il n’a jamais montré
son efficacité dans cette indication. Avec une balance bénéfice-risque qui penchait du côté des effets
indésirables psychiatriques et neurologiques, c’est un retrait bienvenu bien que très tardif ….
●
ACOMPLIA
* (Rimonabant) : des effets indésirables essentiellement psychiatriques. Le
rimonabant, premier médicament antagoniste des récepteurs CB1 aux cannabinoïdes a été promu
pour le traitement adjuvant de l’obésité. Un an après sa commercialisation, les effets indésirables
rapportés sont surtout d’ordre neuropsychique : troubles de l’humeur avec symptômes dépressifs,
anxiété, irritabilité, sensations vertigineuses et troubles du sommeil, et d’ordre digestif. Au vue de ces
données, le RCP réactualisé précise que le rimonabant est désormais contre indiqué chez les patients
présentant une dépression caractérisée ou chez les patients traités par antidépresseurs et ne doit pas
être utilisé chez des patients ayant des antécédents d’idées suicidaires ou de troubles dépressifs, sauf
si le bénéfice attendu du traitement l’emporte sur le risque. NDLR : Cette dernière précision étonne un peu
pour un médicament dont le dossier d’évaluation clinique montrait qu’il avait pour seul bénéfice une perte de quelques
kilos, réversible en quelques mois après l’arrêt du traitement.
●
AVANDIA
* (Rosiglitazone) et
ACTOS
* (Pioglitazone) : augmentation de l’incidence des
fractures chez les patientes traitées au long cours. Cet effet indésirable s’ajoute aux autres risques
connus pour cette classe : risque d’insuffisance cardiaque et oedèmes maculaires. Plus récemment,
s’ajoutent des données inquiétantes sur un risque accru d’infarctus du myocarde (rosiglitazone) et de
cancer de la vessie (pioglitazone). En 2007, mieux vaut se passer des glitazones dans le traitement du
diabète de type II.
Voir le site Afssaps/ http://afssaps.sante.fr

VIGI-PHARMA, N°9, Octobre 2007, Page
2
S
ST
TA
AT
TI
IN
NE
ES
S
:
:
P
P
O
OI
IN
NT
T
S
SU
UR
R
L
LE
ES
S
E
EF
FF
FE
ET
TS
S
I
IN
ND
DE
ES
SI
IR
RA
AB
BL
LE
ES
S
Les statines – atorvastatine (
TAHOR
*), fluvastatine (
FRACTAL
*,
LESCOL
*), pravastatine (
ELISOR
*,
VASTEN
*), rosuvastatine (
CRESTOR
*
) et
simvastatine (
LODALES
*,
ZOCOR
*) – sont les médicaments hypocholestérolémi
ants les plus fréquemment prescrits. Les plus anciennes
sont sur le marché depuis 1988, ce qui donne un recul suffisant pour évaluer leurs effets indésirables.
►Effets indésirables musculaires : les plus connus et préoccupants
Toutes les statines sont concernées.
Les patients présentent des symptômes mineurs tels que
: douleur ou sensibilité musculaire inexpliquée, fatigue musculaire,
crampes, associés ou non à une augmentation modérée de la créatine-phosphokinase (CPK < 5 X Normale).
Cette toxicité est dose-dépendante.
Exceptionnellement peut survenir une rhabdomyolyse, associée ou non à une insuffisance rénale. Elle apparaît en quelques jours,
généralement en début de traitement ou lors d’une augmentation de posologie ou du fait d’une interaction médicamenteuse
:
myalgies intolérables, faiblesse musculaire importante, destruction musculaire massive (CPK > 30 ou 40 X Normale) conduisant
à une myoglobinurie. Le pronostic est conditionné par la gravité de l’insuffisance rénale associée.
Les situations qui prédisposent à l’atteinte musculaire (sans préjuger de sa sévérité) et pour lesquelles un dosage des CPK avant
traitement est préconisé sont : les sujets atteints
personnellement ou ayant un membre de leur famille atteint d’une maladie
musculaire génétique, les sujets atteints d’une hypothyroïdie et ne prenant pas de traitement, une insuffisance rénale, une
consommation excessive d’alcool, l’âge > 70 ans, les sujets
ayant déjà présenté des effets musculaires à la suite d’un traitement
hypocholestérolémiant.
Tout symptôme musculaire inexpliqué apparaissant sous traitement doit faire pratiquer un dosage des CPK, en fonction des
résultats la posologie sera alors ajustée.
Dans le collimateur
: la rosuvastatine pour laquelle les données montrent un risque plus élevé d’effets indésirables musculaires et
rénaux par rapport aux autres statines. (NDLR : cette statine n’a pas été évaluée sur des critères cliniques de morbi-mortalité.)
►Polyneuropathies périphériques
Effet indésirable rare.
Il s’agit de polyneuropathies sensitives ou sensitivomotrices avec des troubles objectifs de la sensibilité et une diminution voire
une abolition des réflexes ostéotendineux ; parfois associées à une diminution sévère de la force musculaire des membres atteints.
Cet effet semble être favorisé par une insuffisance rénale ou un diabète.
►Tendinopathies
D’incidence faible, elles touchent le tendon d’Achille dans la moitié des cas et peuvent conduire à des ruptures tendineuses.
►Effets indésirables hépatiques et pancréatiques
Elévations transitoires et modérées des transaminases
Rares cas d’hépatites et de pancréatites.
►Effets indésirables rénaux et génito-urinaires
Insuffisance rénale, protéinurie et néphropathie
Impuissance.
►Autres effets indésirables
Affections auto-immunes : Polymyosite et lupus érythémateux ont été rapportés.
Céphalées, sensations vertigineuses, insomnies, vision trouble, dysgueusies.
S
ST
TA
AT
TI
IN
NE
ES
S
:
:
P
P
O
OI
IN
NT
T
S
SU
UR
R
L
LE
ES
S
I
IN
NT
TE
ER
RA
AC
CT
TI
IO
ON
NS
S
M
ME
ED
DI
IC
CA
AM
ME
EN
NT
TE
EU
US
SE
ES
S
►Pourquoi certaines statines sont plus à risque d’interactions que d’autres
Atorvastatine et simvastatine sont métabolisées par l’isoenzyme CYP 3A4 du cytochrome P450
; la fluvastatine est
principalement métabolisée par l’isoenzyme CYP 2C9 ;
pravastatine et rosuvastatine ne sont que peu ou pas métabolisées par le
cytochrome P450.
Simvastatine et atorvastatine exposent à d’avantages interactions d’ordre pharmacocinétique que fluvastatine, pravastatine et
rosuvastatine. Elles sont sensibles aux
inhibiteurs enzymatiques du CYP 3A4 qui entraînent une augmentation de leur
concentration plasmatique et donc du risque musculaire. Les principaux inhibiteurs du CYP 3A4 sont
: amiodarone, diltiazem,
vérapamil, la plupart des macrolides (sauf spiramycine
), des antifongiques azolés, des antirétroviraux, la cimétidine, le jus de
pamplemousse. L’acide fusidique augmente les effets de la simvastatine et de l’atorvastatine.
Les inhibiteurs de l’isoenzyme CYP 2C9 qui augmentent les effets de la fluvastatine sont
: cimétidine, fluconazole, fluoxétine,
fluvoxamine, entacapone, clopidrogel, sildénafil.
Attention aux fibrates
: l’association d’un fibrate à une statine, quelle qu’elle soit est déconseillée du fait du risque majoré de
rhabdomyolyse.
►Risque hémorragique
L’association de toutes les statines avec un anticoagulant oral augmente l’effet anticoagulant (surveillance rapprochée de l’INR).
►Conclusion
Pravastatine et Simvastatine sont les statines les mieux évaluées du point de vue morbi-mortalité et sont celles dont on dispose d’une plus
longue expérience d’utilisation. Chez les patients polymédicamentés ou consommateurs de jus de pamplemousse, la pravastatine s’avère
la statine de premier choix.
Prescrire, 2006, n°276, 692-695 et n°278 (supp), 64-66
Prescrire, 2007, n°282, 269-270
Minidossier du SIPS. Hôpital Bicêtre. Août 2006, N°3
Afssaps, Mise au point sur le risque musculaire des statines
http://agmed.sante.gouv.fr/htm/10/statine/point.htm
Réflexion : « Le cholestérol ne bouche pas les artères », Entretien avec Dr de Lorgeril. Le Monde, Mercredi 13 Juin 2007

VIGI-PHARMA, N°9, Octobre 2007, Page
3
1
/
3
100%