sentinelle - Collections

SENTINELLESENTINELLE Volume 10, numéro 6 — Décembre 2004 ISSN # 2-89342-027-7
CLOSTRIDIUM DIFFICILE : QU’EN EST-IL?
CONTEXTE
INFORMATIONS CLINIQUES
POUR UNE UTILISATION JUDICIEUSE DES ANTIBIOTIQUES
AIDE-MÉMOIRE POUR L’ÉVALUATION ET LA PRISE EN CHARGE D’UN
PATIENT ATTEINT DE DIARRHÉE ASSOCIÉE AU C. DIFFICILE
TRAITEMENT DE LA COLITE À CLOSTRIDIUM DIFFICILE
1 sur 1 04-12-23 13:47

Au cours de l’année 2003, certains
microbiologistes de la région de
Montréal et d’autres régions périphé-
riques, dont la Montérégie, ont observé
une augmentation de la fréquence et de la sévérité des
infections nosocomiales à
Clostridium difficile
. La situation
a été signalée aux autorités de la santé publique en avril
2004. En juin 2004, le ministère de la Santé et des Services
sociaux (MSSS) a mandaté le Comité sur les infections
nosocomiales du Québec (CINQ) pour élaborer des lignes
directrices provinciales sur la prévention et le contrôle du
C. difficile
et pour mettre en place un système de
surveillance obligatoire du
C. difficile
par les centres
hospitaliers de soins généraux et spécialisés (CHSGS).
Les lignes directrices intérimaires ont été diffusées en
novembre dernier aux CHSGS ainsi qu’aux centres
hospitaliers de soins de longue durée (CHSLD). La version
finale de ce document est attendue pour la fin décembre
2004. L’infection à
C. difficile
ne remplit pas tous les
critères pour être incluse dans la liste des maladies à
déclaration obligatoire (MADO). Toutefois, le nouveau
système de surveillance couvre l’ensemble du territoire
québécois et permettra de mieux documenter la situation
émergente au Québec sans nécessiter la collecte
d’information nominative. Tous les hôpitaux du Québec
participent au système de surveillance. Un portrait
provincial est attendu au début de 2005.
Parmi les autres actions entreprises pour cette
problématique, une table régionale de prévention des
infections nosocomiales a été formée à partir du comité
régional sur les bactéries multirésistantes qui existait déjà
en Montérégie. Cette table regroupe les microbiologistes et
les professionnels en prévention des infections des CHSGS
ainsi que des représentants des CLSC, des CHSLD, de
l’Agence (Direction de santé publique et Direction des
affaires hospitalières et médicales) et des directeurs des
services professionnels hospitaliers. Son mandat est de
faciliter les actions régionales et d’harmoniser les pratiques.
C
LOSTRIDIUM
DIFFICILE
:
QU’EN EST-IL?
Volume 10, numéro 6 — Décembre 2004 ISSN # 2-89342-027-7
À la demande du ministre Couillard, une tournée des
CHSGS a été complétée en Montérégie le 22 novembre
dernier pour obtenir un portrait de l’implantation des lignes
directrices provinciales et les difficultés rencontrées. Un
portrait de la situation en CHSLD a également été obtenu
par des entrevues téléphoniques.
Enfin, des dépliants sur le
C. difficile
s’adressant à la
population ont été distribués en novembre aux éta-
blissements du réseau ainsi qu’aux médecins et aux
pharmaciens du territoire.
La diarrhée associée au
C. difficile
(DACD) n’est pas une source d’in-
fection fréquente dans la commu-
nauté mais elle constitue la cause
infectieuse la plus fréquente de
diarrhée acquise dans un milieu de soins pour adultes.
Moins de 5 % de la population est porteur de la bactérie. La
majorité des personnes colonisées demeurent asymptoma-
tiques étant donné l’équilibre qui s’établit avec les autres
bactéries intestinales. La rupture de cet équilibre, principa-
lement par la prise d’antibiotiques, permet au
C. difficile
de
se multiplier. On a émis l’hypothèse que pour un patient
hospitalisé, une antibiothérapie à large spectre perturberait la
flore intestinale favorisant ainsi la colonisation par voie orale
avec le
C.difficile
présent dans l’environnement. Selon cette
étude, de 20 à 50 % des patients hospitalisés seraient
susceptible d’acquérir la bactérie. La production de toxine
par la bactérie et la capacité de l’hôte à développer des
anticorps dirigés contre cette toxine sont déterminants pour
le développement ou non de la maladie.
L’infection à
C. difficile
se manifeste par une diarrhée
aqueuse ayant une odeur caractéristique avec ou sans symp-
tômes accompagnateurs tels une fièvre et des douleurs
abdominales diffuses. La sévérité de l’infection est variable
allant de simples diarrhées transitoires qui guérissent avec
le traitement approprié (majorité des cas) à des formes
CONTEXTE
informations
cliniques
S
UPPLÉMENT
Clostridium
difficile
Ce bulletin d’information est produit
par la Direction de santé publique
de l’Agence de développement de réseaux locaux de services
de santé et de services sociaux de la Montérégie

graves. Ces formes graves peuvent entraîner différentes com-
plications dont le mégacôlon toxique pouvant mener à la
perforation colique et au choc septique chez les personnes
les plus vulnérables. Une étude réalisée par Dre Loo et
collaborateurs, de janvier à juin 2004 dans 12 centres
hospitaliers particulièrement touchés, indique une mortalité
plus élevée que précédemment rapportée, pouvant atteindre
8,6 %. L’hypothèse de la circulation d’une souche plus
virulente est actuellement retenue.
Le
C. difficile
se transmet à
partir des mains ou de
l’environnement contaminés de
la personne souffrant de
diarrhée. Le personnel et les
visiteurs peuvent se contaminer
les mains lors de leurs contacts
avec la personne malade ou en
touchant à certains objets de son
environnement. Le patient est contagieux lorsqu’il présente
de la diarrhée. Plus la diarrhée est sévère, plus le risque de
contamination de l’environnement est élevé. Le
C. difficile
est une bactérie produisant des spores qui persistent dans
l’environnement pour de longues périodes. C’est pourquoi le
lavage des mains ainsi que les mesures de prévention des
infections sont primordiales pour briser la chaîne de
transmission.
Dans la vaste majorité des cas, la prise d’un antibiotique est
le facteur précipitant l’émergence clinique de l’infection à
C. difficile
. Plusieurs classes d’antibiotiques ont été impli-
quées comme facteurs de risque, mais la relation causale
avec une classe en particulier reste difficile à établir compte
tenu de la présence de nombreux facteurs confondants
rendant ces études non comparables. Néanmoins, certains
antibiotiques dont la clindamycine, l’ampicilline,
l’amoxicilline-acide clavulanique, les céphalosporines de 2e
et 3e génération et les fluoroquinolones, en particulier
les C-8-méthoxy-fluoroquinolones, semblent présenter un
risque accru. La prise d’une combinaison d’antibiotiques et la
durée de l’antibiothérapie augmentent également le risque
d’acquisition de l’infection. Les conditions sous-jacentes de
l’hôte (âge avancé, maladie sous-jacente sévère, chirurgie, en
particulier digestive) et les facteurs épidémiologiques locaux
constituent d’autres facteurs de risque importants. Plus
récemment, des études ont démontré une association entre
les traitements contre l’acidité gastrique et le risque de
DACD, en particulier pour les inhibiteurs de la pompe à
protons.
Le traitement de 1re ligne demeure le métronidazole. Sauf
pour les cas sévères, la vancomycine constitue une 2e ligne,
car une surutilisation pourrait mener à l’émergence d’in-
fections à entérocoques résistant à la vancomycine (ERV).
Une version modifiée de la section des lignes directrices qui
aborde le traitement de la colite à
C. difficile
se trouve au
verso de l’aide-mémoire ci-joint.
½ Confirmer le diagnostic d’infection bactérienne.
½ Prélever les cultures appropriées avant d’initier l’antibio-
thérapie.
½ Choisir l’antibiothérapie initiale selon le guide thérapeutique
local.
½ Cibler l’antibiothérapie en fonction des résultats de la
culture.
½ Passer à la voie orale dès que possible.
½ Réduire la durée de l’antibiothérapie au minimum.
½ Éviter de traiter la colonisation, les bactériuries asympto-
matiques (sauf chez les femmes enceintes ou avant une
manipulation urologique majeure) et les infections virales
des voies respiratoires.
Nous remercions Dre Nathalie Lussier et Dr Charles Frenette,
microbiologistes-infectiologues à l’Hôpital Charles-LeMoyne,
pour leur collaboration à la rédaction de cet article.
Références
Comité sur les infections nosocomiales du Québec. 2004.
Prévention et contrôle de la diarrhée nosocomiale associée au
Clostridium difficile au Québec - Lignes directrices intérimaires
pour les centres hospitaliers.
2e édition
.
Institut national de santé
publique du Québec, 43 pages + annexes.
2004. “Hospital-Acquired Infection.
C. difficile
: by the
numbers”.
CMAJ
, 171(11) : 1331-1332.
Johnson S., Gerding DN. 1998. “
Clostridium difficile
–
Associated Diarrhea ”. Clin Infect Dis, 26 :1027-1036.
Les lignes directrices pour la prévention et le contrôle de la
diarrhée nosocomiale associée au
C. difficile
recommandent
l’application des pratiques de base et de précautions addi-
tionnelles pour la DACD (voir aide-mémoire ci-joint). Elles
recommandent également :
d’utiliser les antibiotiques de façon appropriée et de
former un comité de surveillance responsable de la
surveillance quantitative et qualitative des antibiotiques
dans chaque centre hospitalier;
de respecter le ratio minimal d’un professionnel en
prévention des infections (PPI) par 133 lits de courte durée
et d’un PPI par 250 lits de longue durée;
de mettre en place un système de surveillance de l’in-
fection.
POUR UNE UTILISATION JUDICIEUSE
DES ANTIBIOTIQUES

Éliminer les autres causes de diarrhée (laxatifs, médicaments, reprise du transit après une chirurgie, maladies inflammatoires,
nutrition entérale par tube nasogastrique, colite ischémique, fécalome).
Appliquer des précautions additionnelles pour la DACD
(en milieu de soins) :
½ port de gants et d’une blouse à manches longues dès l’entrée dans la chambre d’un patient atteint;
½ information au patient, au personnel et aux visiteurs des précautions recommandées;
½ lavage des mains au lavabo avec un savon antiseptique pour le patient, le personnel et les visiteurs;
½ isolement des patients atteints (chambre privée ou cohorte) et utilisation de matériel dédié (stéthoscope, sphygmomano-
mètre, thermomètre, saturomètre, etc.);
½ désinfection du matériel réutilisable et de l’environnement du patient atteint à l’aide de produits à base de chlore,
comme l’eau de Javel : 1 partie d’eau de Javel (concentration 5 à 6 %) diluée dans 9 parties d’eau;
½ signalement de la situation à l’établissement qui reçoit un patient atteint lors des transferts.
Confirmer le diagnostic
½ Recherche de toxine du
C. difficile
dans les selles.
½ Sigmoïdoscopie à envisager lorsque :
un diagnostic rapide est nécessaire en l’absence d’autres options;
le patient n’a pas de selles (i.e. iléus);
d’autres étiologies sont suspectées;
la recherche de toxine est négative et le diagnostic est fortement suspecté.
IL N’EST PAS RECOMMANDÉ DE FAIRE UN TEST DE CONTRÔLE À LA FIN D’UN TRAITEMENT DE DACD
NI DE DÉPISTER LES PERSONNES ASYMPTOMATIQUES, MÊME POUR LES CONTACTS DES CAS DE DACD.
AIDE-MÉMOIRE POUR L’ÉVALUATION ET LA PRISE EN CHARGE
D’UN PATIENT ATTEINT DE DIARRHÉE ASSOCIÉE AU
C. DIFFICILE
Prise récente d’antibiotiques (4-8 semaines).
Contact étroit avec des personnes atteintes de DACD.
Hospitalisation en cours ou récente.
Histoire récente de DACD (rechutes fréquentes).
QUAND SOUPÇONNER UNE DIARRHÉE
ASSOCIÉE AU
CLOSTRIDIUM DIFFICILE
(DACD)?
LORSQU’ON SOUPÇONNE UNE DACD
LORSQUE LE DIAGNOSTIC EST CONFIRMÉ
½ Maintenir l’application des précautions additionnelles pour la DACD au moins 72 heures après l’arrêt de la diarrhée (en
milieu de soins).
½ Choisir le traitement approprié (algorithme au verso).

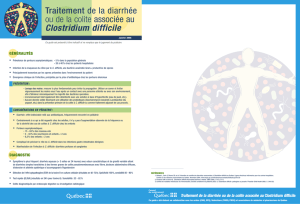
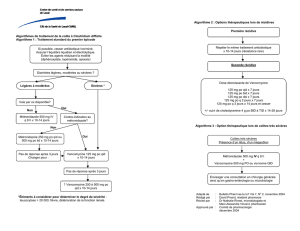
TRAITEMENT DE LA COLITE À CLOSTRIDIUM DIFFICILE*
Reconsidérer l’indication de l’antibiothérapie.
Réévaluer l’usage des narcotiques.
Éviter les antipéristaltiques tels que lopéramide/ImodiumMD et diphénoxylate/LomotilMD.
En présence d’une antibiothérapie concomitante, considérer de prolonger le traitement
antibiotique contre le
C. difficile
d’une semaine après l’arrêt de celle-ci.
Premier épisode
Cas de sévérité légère à modérée Cas sévères ou contre-indication au
métronidazole(1)
Cas très sévères
Présence d’un iléus, d’un mégacôlon
Métronidazole (MTZ) 500 mg PO
TID (ou 250 mg QID) pour
7-14 jours
Vancomycine 125- 500 mg PO QID
via TNG (tube nasogastrique)
et métronidazole 500 mg IV TID
Envisager une consultation
en chirurgie générale ainsi
qu’en gastro-entérologie ou
microbiologie-infectiologie
Si détérioration ou
non-réponse après 3 à 5 jours
Vancomycine 125 mg PO QID
pour 14 jours
Si détérioration ou non-réponse après
3 à 5 jours :
Consultation en gastro-entérologie
ou microbiologie-infectiologie
Première récidive
Récidive(s)(2)
> 1 Récidive
Si réponse au
MTZ lors du
premier épisode
Si échec au
MTZ lors du
premier épisode
Métronidazole 500 mg
PO TID pour 10-14 jours
Vancomycine 125 mg
PO QID pour 10-14 jours
Vancomycine 125 mg PO QID pour 7 jours
125 mg PO BID pour 7 jours
125 mg PO DIE pour 7 jours
125 mg q 2 jours pour 7 jours
125 mg q 3 jours pour 14 jours
1. Une maladie sévère est définie en présence de l'un ou l'autre des critères suivants :
> 8 selles/ 24 heures, hémorragie digestive basse instable, To > 38.6o C, leucocytose > 20,000, perforation colique, sepsis secondaire à la colite.
2. Toujours reconfirmer le diagnostic.
*Adapté par le Comité sur les infections nosocomiales du Québec (CINQ) à partir du Protocole de l’Hôpital Maisonneuve-Rosemont (Collaboration : services de gastro-
entérologie et de médecine interne; départements de microbiologie-infectiologie et de pharmacie)
Ce bulletin d’information est produit avec la collaboration de l’équipe maladies transmissibles
de la Direction de santé publique de la Montérégie
Coordonnatrice : Yolaine Rioux
Directrice : Docteure Jocelyne Sauvé
1
/
5
100%