L’ Comment défi nit-on, en 2012, une tumeur hormonosensible ? DOSSIER THÉMATIQUE

384 | La Lettre du Cancérologue • Vol. XXI - n° 8 - octobre 2012
DOSSIER THÉMATIQUE
L’hormonothérapie
dans les cancers du sein
Comment défi nit-on, en 2012,
une tumeur hormonosensible ?
How to define hormone sensitive breast tumors in 2012?
J.M. Guinebretière*, F. Spyratos**
* Service de pathologie, hôpital
René-Huguenin, institut Curie, Saint-
Cloud.
** Service d’oncogénétique, hôpital
René-Huguenin, institut Curie, Saint-
Cloud.
L’
effi cacité des traitements hormonaux dans
le cancer du sein est connue de longue date,
grâce à G.T. Beatson : c’est lui qui, le premier,
en réalisant des ovariectomies chez des patientes
atteintes de tumeurs du sein inopérables, provoqua
une diminution importante de la taille des tumeurs (1).
Mais il apparut rapidement, après l’identifi cation du
rôle thérapeutique de la castration, que ce traitement
ne bénéfi ciait qu’à un nombre limité de patientes, de
l’ordre de 30 % (2). Cela suscita de nombreux travaux
pour comprendre l’effet de la castration et rechercher
des facteurs prédictifs de la réponse. La découverte des
estrogènes (3) et de leur métabolisme apporta une
première réponse. Celle des récepteurs aux estrogènes
(RE) [4] et leur caractérisation (5) permirent d’expli-
quer que les effets des estrogènes étaient limités aux
organes qui seuls expriment ces récepteurs spécifi ques
et offrirent une voie de recherche thérapeutique pour
contrer leur action, conduisant aux premiers médica-
ments antiestrogènes. Mais elles fournirent également
un outil prédictif, car les premiers résultats des études
cliniques montrèrent que la présence des récepteurs
hormonaux (RH) dans les tumeurs (6) était corrélée
à l’effi cacité du traitement antihormonal. Le concept
d’hormonosensibilité était né. Si une autre forme de
récepteur, dite β, a été récemment identifi ée, son rôle
est mal connu, sans lien prouvé avec la sensibilité
aux traitements antihormonaux ou le pronostic des
cancers du sein, à la différence du REα, le seul qui soit
évalué en routine et qui sera détaillé ici.
Quels sont les techniques
utilisées et leurs avantages
respectifs ?
Les premières analyses s’effectuaient sur des tissus
tumoraux congelés, homogénéisés puis ultra-
centrifugés pour obtenir une fraction “cytosolique”
à partir de laquelle était réalisé le dosage. Elles
mettaient en œuvre des techniques biochimiques
classiques : les travaux princeps de E.V. Jensen et al.
faisaient appel à des gradients de saccharose, puis,
lorsque l’intérêt clinique de la mesure des RE s’est
imposé, les méthodes ont évolué pour permettre
leur utilisation en routine (6, 7). Ce furent d’abord
les hormones radiomarquées, qui permettent de
calculer un nombre de sites liant l’hormone spéci-
fi quement (8) et de déterminer leur constante de
dissociation (méthode au charbon-dextran [DCC]
et calculs selon la méthode de Scatchard). Puis les
anticorps monoclonaux et la méthode immuno-
enzymatique (EIA [enzyme immunoassay]), plus
simple et nécessitant des quantités moindres de
tissu, ont progressivement remplacé le DCC à la
fi n des années 1980. La mesure du récepteur à la
progestérone (RP) est venue compléter celle du RE,
dont la synthèse dépend du RE fonctionnel et qui
représentait le témoin de la fonctionnalité du RE. Les
résultats étaient exprimés en femtomoles par milli-
gramme de protéines avec un seuil placé à 10 (DCC)
ou 15 (EIA) fmol/mg.
Les avantages de ces techniques biochimiques sont
multiples. D’abord, elles font appel à une techno-
logie parfaitement calibrée, sensible et reproduc-
tible. Ensuite, elles offrent une analyse quantitative
donnant une valeur numérique. Cette valeur est
importante, car, comme l’a montré E.V. Jensen,
la réponse à l’hormonothérapie − que ce soit par
castration ou par tamoxifène − est meilleure chez
les patientes dont les tumeurs présentent les taux de
RE les plus élevés. Enfi n, elles sont accessibles à un
contrôle qualité qui s’est rapidement mis en place à
l’échelon européen à partir des années 1970 avec la
diffusion de ce test à l’ensemble des cancers infi ltrants
pour décider de la nécessité d’une hormono thérapie.

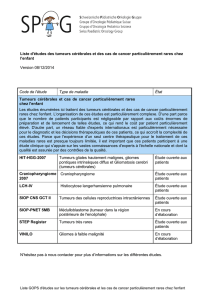
Figure 1. Carcinome infiltrant constitué par une
stromaréaction fi breuse prédominante (coloration
à l’hématoxyline-éosine-safran [HES], × 100). La
composante infi ltrante formée de tubes et de travées
est minoritaire, intriquée avec la composante intra-
canalaire d’architecture massive.
La Lettre du Cancérologue • Vol. XXI - n° 8 - octobre 2012 | 385
Résumé
L’hormonosensibilité est aujourd’hui évaluée en routine au diagnostic de carcinome infiltrant par l’expres-
sion des récepteurs hormonaux en immunohistochimie. Le seuil de positivité a été défini initialement à
10 % de cellules marquées, car il s’agit de la valeur qui assure la meilleure corrélation avec la méthode
biochimique. Une étude récente, qui ne fait pas l’unanimité, suggère que le seuil d’efficacité clinique est
à 1 %. Il a été évalué à partir d’un matériel tissulaire, peu représentatif et différent de celui qui est utilisé
en routine. Des études publiées sur les tumeurs dont l’expression pour les RH est comprise entre 1 et 10 %,
on peut retenir qu’elles sont rares et touchent moins de 1 % de la population, que leurs caractéristiques
histologiques, cliniques et évolutives les rattachent au groupe des tumeurs RH négatives et que l’hormo-
nothérapie n’apporte pas de bénéfice significatif.
Mots-clés
Cancer du sein
Tumeurs du sein
Récepteurs
hormonaux
Pronostic
Facteur prédictif
Hormonothérapie
Summary
The hormone sensitivity is
today routinely evaluated
at the time of the diagnosis
of invasive cancer by means
of immunohistochemical
method. Initially the threshold
of positivity, 10% of positive
cancer cells, was defined as
the threshold best correlated
with results of the biochemical
method. A recent and contro-
versial publication suggests a
different threshold, 1%, based
on the correlation with clinical
response. However it was
established on a special mate-
rial, less representative and
different from those usually
used. Two new publications
studied features of tumor with
expression between 1 and 9%:
these tumors represent a very
small group of tumors, less than
1% of the whole population,
and their histologic, clinical
and evolutive features are
very similar to the RH negative
group, and the hormonal treat-
ment brings no survival benefi t.
Keywords
Breast cancer
Breast neoplasm
Hormonal receptors
Prognosis
Predictive factor
Cependant, elles ont également d’importantes
contraintes car elles nécessitent un fragment de
tumeur congelée, ce qui implique un circuit particu-
lier de gestion des fragments biopsiques ou chirurgi-
caux. La prise en charge des prélèvements doit être
immédiate, dès leur réalisation, pour éviter la dégra-
dation des protéines, qui survient très rapidement.
Il est nécessaire de disposer d’un circuit de froid à
−80 ou à −180 °C pour conserver avant le test le
fragment de tumeur que le pathologiste aura prélevé
de la pièce d’exérèse chirurgicale et macrodisséqué.
Outre la diffi culté de réunir les conditions techniques
et de rassembler l’équipe (disponibilité), il faut que
la tumeur soit facilement identifi able et de taille
suffi sante pour qu’un fragment représentatif puisse
être prélevé pour le test sans danger pour l’analyse
diagnostique de la pièce d’exérèse. Avec le succès
du développement du dépistage organisé et indivi-
duel du cancer du sein, les tumeurs sont de plus en
plus petites et ne sont généralement plus palpables,
ce qui ne permet pas toujours au pathologiste de
les identifi er sur le prélèvement chirurgical ou de
prélever un fragment suffi sant pour cette analyse.
Il n’y avait généralement pas de contrôle micro-
scopique du fragment utilisé, qui pouvait n’être
que peu cellulaire, être nécrosé ou incomplète-
ment représentatif, constitué majoritairement par
la composante in situ ou la stromaréaction.
Enfi n, l’analyse s’effectuait à partir d’un broyat tissu-
laire, et la mesure prenait donc en compte l’ensemble
des cellules présentes − cellules infl ammatoires, vais-
seaux et fi broblastes du stroma, tissu épithélial et
conjonctif normal et cellules carcinomateuses infi l-
trantes − mais aussi in situ (fi gure 1). En cas de tumeur
de petite taille, peu cellulaire ou de stroma abondant,
les cellules normales ou les éléments infl ammatoires
sont majoritaires par rapport aux cellules tumorales,
minimisant artifi ciellement la mesure par dilution.
La seconde méthode qui s’est progressivement déve-
loppée et qui a remplacé la méthode biochimique
comme référence, ou gold standard, est l’immuno-
histochimie (IHC). Cette technique était alors large-
ment répandue dans les laboratoires de pathologie
pour le diagnostic, notamment la caractérisation des
tumeurs. Elle présente différents avantages en plus
de l’accessibilité de la technique implantée dans la
plupart des laboratoires.
➤
Le test peut être réalisé sur un fragment fi xé
et inclus en paraffi ne et utiliser le matériel qui a
permis de poser le diagnostic. Il n’est plus néces-
saire de disposer d’un circuit particulier (chaîne de
froid, congélation) ni d’user un fragment supplé-
mentaire et spécifi que pour l’analyse, qu’il devient
diffi cile d’obtenir avec la diminution de la taille des
tumeurs. Il est aussi possible de réaliser l’analyse de
façon rétrospective en cas de tumeurs de découverte
fortuite.
➤L’analyse porte uniquement sur la composante
infiltrante, indépendamment de la quantité de
tumeur et de stroma présente, puisqu’il s’agit d’une
technique morphologique. Il est possible de séparer
l’expression des composantes in situ et infi ltrante,
dont l’expression diffère parfois (fi gure 1).

Figure 2. Immunomarquage pour le récepteur à
l’estrogène (× 100). Marquage hétérogène associant
une composante infi ltrante négative majoritaire et
une composante positive et intense à la fois in situ
et infi ltrante.
Figure 3. Immunomarquage pour le récepteur à la progestérone (× 200). Sont pris en
compte le pourcentage de noyaux de cellules carcinomateuses infi ltrantes marquées et
l’intensité du marquage, ici variable, faible, modérée et intense.
386 | La Lettre du Cancérologue • Vol. XXI - n° 8 - octobre 2012
Comment défi nit-on, en 2012, une tumeur hormonosensible ?
DOSSIER THÉMATIQUE
L’hormonothérapie
dans les cancers du sein
➤
Il devient possible d’identifier des tumeurs
d’expression hétérogène alors que la méthode
biochimique évalue une expression moyenne sans
possibilité de reconnaître ces tumeurs dont la
prise en charge diffère (fi gure 2). Il est étonnant
qu’aujourd’hui l’importance de cette hétéro généité
comme sa répercussion clinique n’ont pas été
étudiées malgré la facilité de sa détection.
À la suite de cette nouvelle indication, la méthode
immunohistochimique, développée initialement
pour le diagnostic, s’est progressivement améliorée :
elle est d’abord devenue plus sensible, permettant
d’identifi er des tumeurs avec un très faible niveau
d’expression, puis plus reproductible avec le déve-
loppement d’automates de coloration. Des contrôles
de qualité externe se sont mis en place parallèle-
ment au niveau national (AFAQAP [Association fran-
çaise d’assurance qualité en anatomie et cytologie
pathologiques]) et européen (UK NEQAS [United
Kingdom National External Quality Assessment
Service], NordiQC).
Quels sont les seuils utilisés ?
Pour la biochimie, première technique utilisée, le
seuil a été défi ni en fonction de l’effi cacité du traite-
ment avec une valeur évaluée à 20 puis à 10 fmol/mg
pour le DCC et 15 fmol/mg pour l’EIA. Au-dessous
de cette valeur, l’action du traitement était observée
dans moins de 10 % des cas alors que, au-dessus, elle
atteignait 60 %. Ces seuils ont été déterminés chez
des patientes métastatiques, mais se sont avérés
similaires dans un contexte adjuvant (9). La présence
d’une faible action en cas de tests négatifs s’explique
par des problèmes techniques du dosage et par
l’hétérogénéité tumorale pour les RH, le fragment
analysé ne contenant pas le contingent positif.
Pour l’IHC, le seuil a été établi comme la valeur qui
assurait la meilleure concordance avec la technique
biochimique, qui était alors la méthode de réfé-
rence. Il a ainsi été établi à plus de 10 % de noyaux
marqués de cellules carcinomateuses infi ltrantes (10).
Les 2 données analysées sont l’intensité de marquage
− défi nie comme nulle, faible, modérée ou forte −
et le pourcentage de cellules tumorales marquées
(figure 3). Plusieurs systèmes ou scores ont été
proposés − comme le H-score (11) et le Q-score (12),
qui apprécient de façon plus quantitative l’expression
par rapport au résultat positif/négatif −, mais les rares
études ayant évalué l’impact clinique de ces scores
n’ont pas identifi é d’intérêt supplémentaire (13) ;
elles portaient toutefois sur une population limitée.

La Lettre du Cancérologue • Vol. XXI - n° 8 - octobre 2012 | 387
DOSSIER THÉMATIQUE
Et la polémique apparut
Une publication récente a remis en question la
valeur du seuil de 10 % utilisée de longue date
en pratique clinique (14). Celle-ci a évalué un
nouveau score fondé sur l’intensité de marquage
et le pourcentage de cellules marquées en IHC.
Chacun est réparti en différentes classes (tableau I),
puis combiné ensemble pour donner des valeurs
allant de 0 (absence de marquage) à 8 (marquage
intense de plus de 2 tiers de cellules tumorales).
L’intérêt de ce nouveau score est de fournir une
évaluation simple et quantitative de l’expression
des RH. Sa validation a été effectuée sur une popu-
lation de 1 982 patientes, testées au préalable par
méthode biochimique, ce qui a permis de comparer
sa valeur à celle de la méthode biochimique en
fonction de l’effi cacité clinique. L’analyse montre
d’abord que ce score est prédictif d’une réponse au
traitement et que, plus il est élevé, meilleure sera
la réponse au traitement antihormonal. Enfi n, sa
valeur prédictive serait plus élevée que celle de la
méthode bio chimique. Le seuil de positivité calculé
dans cette étude était de 1 %. À la différence des
autres études, il ne s’agit pas de la valeur assurant
la meilleure concordance avec la méthode biochi-
mique mais du seuil qui est le mieux corrélé avec
la réponse au traitement. Cela est possible grâce
à la taille importante de la population testée, aux
données cliniques et à la longueur du suivi. De par
son intérêt quantitatif, ce score a rapidement été
utilisé, et la valeur seuil fi xée à 1 % introduite dans
les recommandations nord-américaines (15).
Les problèmes qu’elle suscite
Si l’intérêt de ce score n’est pas discuté, le seuil de
1 % l’est, en revanche, pour des raisons techniques.
Le matériel utilisé pour cette étude est en effet très
particulier, correspondant au reliquat des broyats
utilisés pour le dosage biochimique. Ceux-ci ont été
conservés dans de l’azote liquide puis décongelés,
fi xés en formol et inclus en paraffi ne pour réaliser
l’étude immunohistochimique. Ils concernent donc
un matériel différent de celui utilisé habituellement
par le pathologiste. Il s’agit même d’un matériel
déconseillé pour de telles analyses, parce qu’il est
congelé, ce qui altère l’immunogénicité, parce qu’il
est fragmenté et que son analyse morphologique
est diffi cile, sans témoin positif interne identifi able
(lobules ou canaux) et, enfi n, parce qu’il est de petite
taille, donc peu représentatif. Ainsi la mauvaise
qualité du matériel utilisé peut donc expliquer le
choix d’un seuil bas. Cela explique aussi que, bien
que l’IHC identifi e davantage de tumeurs RH+ que la
biochimie, dans cette étude la détection par IHC soit
inférieure à celle de la biochimie : 70,5 % de tumeurs
RH+ par IHC contre 78,9 % par biochimie (16).
Aujourd’hui, le taux de tumeurs positives en IHC
dépasse même 80 %.
Quelles sont les données
récentes ?
À la suite de cette publication, bien que ce score
soit de plus en plus fréquemment utilisé, une polé-
mique est née sur le seuil de positivité à utiliser,
différents centres préférant garder le seuil de 10 %,
parce qu’il a été établi à partir du matériel utilisé en
routine, alors que d’autres utilisent ce nouveau score
avec la norme de 1 % parce qu’il est lié à la réponse
au traitement. Aucune nouvelle étude n’a encore
essayé de répondre à cette question, car l’établis-
sement d’un seuil nécessite de grandes populations
de patientes avec un long suivi clinique. Toutefois,
quelques données récentes apportent un éclairage
nouveau sur ce problème : d’abord, la fréquence des
patientes ayant une tumeur dont l’expression des
RE ou des RP est située entre 1 et 10 %, c’est-à-
dire qui seraient considérées comme positives pour
Tableau I. Score d’Allred pour évaluer les récepteurs aux
estrogènes et à la progestérone par immunohistochimie.
Ce score est obtenu en ajoutant la note de l’intensité
du marquage (0 à 3) à celle du pourcentage de cellules
marquées (1 à 5). Le total varie de 0 (absence de marquage)
à 8 (marquage intense de plus de 2 tiers de cellules tumo-
rales). Le seuil de positivité est défi ni à 3 (marquage faible
de 1 à 10 % des cellules tumorales).
Pourcentage de cellules tumorales
marquées (noyaux)
Score
< 1 % 1
Entre 1 et 10 % 2
Entre 11 et 33 % 3
Entre 34 et 66 % 4
> 66 % 5
Intensité du marquage des cellules
tumorales marquées (noyaux)
Score
Absence de marquage 0
Marquage faible 1
Marquage modéré 2
Marquage intense 3

388 | La Lettre du Cancérologue • Vol. XXI - n° 8 - octobre 2012
Comment défi nit-on, en 2012, une tumeur hormonosensible ?
DOSSIER THÉMATIQUE
L’hormonothérapie
dans les cancers du sein
le seuil de 1 % mais négatives pour le seuil de 10 %.
Elle est très faible dans le groupe français du GEFPICS
(groupe d’évaluation des facteurs pronostiques par
immunohistochimie dans les cancers du sein) : moins
de 1 % des tumeurs testées, alors qu’elle représente
3 % dans l’étude de J.M. Harvey et al. (14). Dans
l’essai thérapeutique BIG 1-98, seules 56 patientes
sur les 6 126 incluses étaient dans ce groupe, c’est-
à-dire moins de 1 % (17).
Ce problème de seuil ne concerne donc que très
peu de patientes. La valeur prédictive du test ne
peut être infl uencée par le choix entre ces 2 seuils.
La seconde étude porte sur les caractéristiques biolo-
giques de ces tumeurs (18). Elles ont été établies sur
une population de 465 patientes pour lesquelles
était disponible, en plus des RH déterminés par
IHC sur microbiopsie, du matériel congelé obtenu
avant l’intervention. Celui-ci a été utilisé pour une
analyse génomique de microarray par puce Affyme-
trix HG-U133A. Les données de génomique obtenues
ont permis de déterminer l’ARN messager (ARNm)
des REα, la classifi cation moléculaire (19) établie
par le prédicteur PAM 50 Breast Cancer Intrinsic Clas-
sifi er (20) et enfi n le SET (Sensitivity to Endocrine
Therapy) index, signature moléculaire de prédic-
tion à l’hormonothérapie récemment publiée (21)
et constituée de 165 gènes. Les patientes ont été
réparties en 4 classes (RE−, entre 1 et 9 %, 10 %,
plus de 10 %), et les 3 données ARNm de REα, la
classifi cation moléculaire et le SET index calculés
pour chacune des classes (tableau II).
Pour la deuxième classe (> 1 à 9 %) des noyaux
positifs, les tumeurs sont majoritairement de type
basal-like (48 %) et HER2 (32 %). Le taux d’ARNm
des RE était négatif dans plus de 75 % des cas et le
SET index était faible dans tous les cas, témoignant
d’une hormonorésistance. Ainsi, les caractéristiques
biologiques des tumeurs entre 1 et 9 % sont en très
grande majorité identiques à celles des tumeurs RH−.
La dernière étude concerne les caractéristiques
cliniques et pathologiques de ces patientes (22).
La population étudiée correspond à 1 257 patientes
triple-négatives chez qui HER2 n’était pas présent ou
n’était pas amplifi é et dont les RH étaient inférieurs
à 10 %, prises en charge au MD Anderson Cancer
Center (États-Unis) entre le 1
er
janvier 1990 et le
1
er
janvier 2009. Elle a été stratifi ée en 3 classes
(tableau III) : RE−, RE+ entre 1 et 5 % et RE+ entre
6 et 10 %. Les caractéristiques cliniques (taille, âge)
et histologiques (grade Scarff, Bloom et Richardson
[SBR], N, emboles, type histologique), le type de trai-
tement local et général et l’évolution ont été calculés
pour chacune des classes. Il n’y avait aucune diffé-
rence entre les groupes pour la taille, l’âge, le type
histologique, le nombre de patientes N+, les emboles,
le traitement local ni la chimiothérapie. Le grade dimi-
nuait à mesure que le taux de RE augmentait. Il n’a
pas été observé de différence de survie ni de lien entre
celle-ci et le taux des RH ou de l’hormono thérapie.
Les caractéristiques cliniques et histologiques et
l’évolution des tumeurs entre 1 et 10 % sont donc
très proches de celles des tumeurs en dessous de 1 %.
Tableau II. Caractéristiques biologiques selon l’expression immunohistochimique des récepteurs hormonaux (RH) [18].
Taux de cellules
RH+ (%)
n Type moléculaire ARNmRE+
(%)
Luminal A
(n)
Luminal B
(n)
Her2
(n)
Basal
(n)
Normal
(n)
0 183 2 1 51 111 18 8,7
1 à 9 25 0 2 8 12 3 24
10 62111167
> 10 251 120 61 38 16 16 92
Tableau III. Caractéristiques cliniques et histologiques selon le taux d’expression des récepteurs hormonaux (RH) pour la population triple-négative du MD
Anderson Cancer Center (États-Unis) [22].
Taux de positivité
des RH
(%)
Âge (%) Taille (%) Grade SBR (%) Emboles (%)
≤ 50 ans > 50 ans T1 T2 T3-4 1-2 3 Non Oui
< 1 49 51 53 40 7 9 91 71 29
1 à 5 48,5 51,5 55 36 9 15 85 75 25
6 à 10 53 47 63 34 3 20 80 78 22
SBR: grade Scarff, Bloom et Richardson.
 6
6
 7
7
1
/
7
100%