1 Chimie bio-organique des phénols, notion de polyphénols

1
Chimie bio-organique des phénols, notion de
polyphénols
- Importance des phénols dans les sciences pharmaceutiques ;
- nombreuses substances naturelles, nombreux médicaments ;
- une physico-chimie particulière qu’il faut bien connaître.
A- Fonction phénol
Fonction hydroxyle portée par un carbone aromatique (benzène par exemple) :
B- Représentant le plus simple = « le phénol »
C- Composés phénoliques = « les phénols »
- phénols plus ou moins substitués ;
- éventuellement polycycliques ;
- grande diversité des structures (vide infra).
D- Notion de molécules polyphénoliques = « les polyphénols »
- Des molécules peuvent contenir plusieurs fonctions phénoliques et plusieurs cycles
aromatiques phénoliques ;
- c’est notamment le cas de nombreuses substances naturelles.
OH
R
R'
"les phénols"
OH
R
R'
OH
"les polyphénols"
Remarques :
- écriture commode : le groupement fonctionnel est sur un radical aryle
1
, il est possible d’écrire les
phénols comme indiqué ci-contre ;
- au delà d’une nomenclature officielle simple2, les phénols ont souvent des noms d’usage.
Ar OH
1 De même que celui des alcools est fixé sur un radical alkyle.
2 Préfixe « hydroxy- ».
I- Introduction
II- Phénols : définition
,
structures

1- Phénols et polyphénols PAES – 2012-2013 2
A- Capacité de délocalisation d’un doublet de l’atome d’oxygène
- L’oxygène est dans un état d’hybridation sp2 ;
- le doublet non liant de l’orbital pz peut se délocaliser vers le cycle aromatique ;
- c’est la possibilité de recouvrement avec les orbitales pz du cycle benzénique qui explique cette délocalisation :
- conséquence : énergie de stabilisation importante (~40 kcal/mole, ~167 kJ/mole).
B- Conséquences sur la réactivité
OH
acidité notable du proton
basicité tr ès f aible
rupturedelaliaisonC-O difficile
activation du cycle aromatique
(substitutions électrophiles
favorisées)
- Plusieurs milliers de substances naturelles sont de nature phénolique ;
- elles appartiennent à différentes classes phytochimiques3 et ont, par conséquent, des voies de biosynthèse
différentes ;
- les structures sont très diverses4 :
3 Cette notion a été entrevue dans le cours du Pr Guy Lewin. Les molécules phénoliques (et polyphénoliques, cf page 12) peuvent appartenir à la
classe des polyacétates, des alcaloïdes, des terpènes etc. Les grandes voies de biosynthèse des substances naturelles seront appréhendées à
partir de la deuxième année. On peut retenir dès à présent que les voies métaboliques qui conduisent à des molécules phénoliques constituent les
voies essentielles de formation des cycles aromatiques dans la nature.
4 On parle de « diversité moléculaire ».
III- Caractéristi
q
ues moléculaires et consé
q
uences sur la réactivité
I
V
- Exem
p
les de substances naturelles
p
hénoli
q
ues

1- Phénols et polyphénols PAES – 2012-2013 3
- De nombreuses molécules possédant une fonction phénol ont une activité biologique ou un rôle essentiel
pour l’organisme. À titre d’exemple :
- la tyrosine est un acide aminé essentiel ;
- la dopamine est un neurotransmetteur ;
- l’adrénaline est produite par l’organisme en cas de stress :
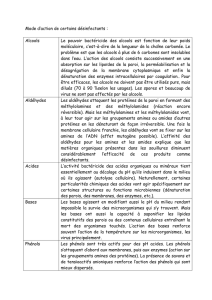
Application 1 :
Parmi les molécules suivantes, lesquelles possèdent une fonction phénol ?
- Le plus souvent, les phénols sont des solides cristallins ;
- les associations intermoléculaires sont en général importantes (liaison hydrogène) les points d’ébullition sont
élevés ;
- la solubilité dans l’eau varie, notamment avec le pH de la solution (vide infra) ;
- les phénols ont une odeur en général marquée5.
- Il existe de très nombreuses méthodes ;
- générales ou spécifiques ;
- nous n’étudierons ici que quelques exemples sélectionnés.
A- Préparation par hydrolyse d’un halogénure d’aryle
- Méthode intuitivement intéressante et générale6 ;
- en réalité difficile à mettre en œuvre.
5 Les phénols de faible masse moléculaire peuvent être volatils, on les trouvera par exemple dans des huiles essentielles (c’est le cas du thymol – à
odeur bien caractéristique – évoqué au paragraphe précédent).
6 En regard, par exemple, de la réaction correspondante pour l’accès aux alcools « classiques ».
V
I- Quel
q
ues
p
ro
p
riétés
p
h
y
sicochimi
q
ues des
p
hénols
V
II- Pré
p
aration des
p
hénols
V
- Rôles biolo
g
i
q
ues des
p
hénols

1- Phénols et polyphénols PAES – 2012-2013 4
Cl Cl
etc
Cl
OH
Na
O
2+NaCl+H
2O
>300°C
pression
catalyseur
OH
acidif ication pour génér er
le phénol
conditions drastiques
Application 2 :
En vous aidant du mécanisme d’hydrolyse d’un halogénure d’aryle, expliquez la formation des dioxines à partir des
ortho-chlorophénols à haute température. Proposez un mécanisme.
B- Préparation par fusion alcaline d’acides sulfoniques aromatiques
- Méthode générale d’accès aux phénols ;
- conditions de la réaction :
SO3H O Na
~350°C
fusion
ArSO3H+NaOH ArSO3Na + H2O
ArSO3Na + 2 NaOH ArONa + Na2SO3+H
2O
acidification
H
OH
bilandelaréaction:
phénol
acide benzène
sulfonique
C- Un exemple de synthèse industrielle du phénol : procédé par oxydation du cumène
- Applicable au phénol sensu stricto ;
- procédé industriel en deux temps7 :
7 En termes de procédés industriels, il existe plusieurs variantes pour cette synthèse qui demeure aujourd’hui une des plus utilisées pour la
préparation du phénol. Les deux étapes sont exothermiques et doivent être réalisées dans des réacteurs différents.

1- Phénols et polyphénols PAES – 2012-2013 5
1 oxydation du cumène8 en présence d’oxygène :
2 décomposition en milieu acide :
OH Me
Me
O
Me
Me
OOH+
milieu acide : H2SO4
pression, ~60 °C
hydroperoxyde
de cumène phénol acétone
pas de perte de matière
- mécanisme de la décomposition : - complexe -
- Les phénols présentent des propriétés très intéressantes et souvent exploitées en chimie organique, chimie
pharmaceutique et chimie des substances naturelles.9
A- Acidité des phénols
1- Éléments de comparaison
Les phénols présentent un caractère acide, exemple de la comparaison avec le cyclohexanol :
OH OH
pKa~10 pKa~16
versus
phénol cyclohexanol
8 On notera que le cumène (tout comme l’acide benzène sulfonique évoqué plus haut) est facilement accessible industriellement par la chimie
« classique » du benzène.
9 Ce sont essentiellement les propriétés liées à la liaison O-H qui sont étudiées cette année.
V
III- Réactivité des
p
hénols
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
1
/
28
100%