JFR 2010 - Imagerie et PMA : que doit savoir...

JFR 2010 - Imagerie et PMA : que doit savoir le radiologue ?
Mis à jour le 05/07/2011 par
SFR
A Jalaguier
-Coudray, I Thomassin-Naggara . Paris
Article issu du Quotidien des JFR 2010
- Mardi 26 Octobre
En association avec l
’
hormonologie, l
’
imagerie est indispensable au
clinicien de l
’
assistance médicale à la procréation (AMP) à toutes les
étapes de sa pratique. L
’
échographie pelvienne par voie endovaginale
est au premier plan et joue un rôle déterminant à toutes les étapes de
l
’
AMP (1).
Avant le début de la prise en charge, l
’
imagerie va permettre de réaliser
le bilan étiologique d
’
infertilité : l
’
hystérosalpingographie reste
l
’
examen incontournable pour évaluer la perméabilité tubaire, même si
plusieurs auteurs évaluent actuellement la perméabilité tubaire en IRM
après cathétérisme utérin et injection de contraste afin de supprimer
l
’
irradiation engendrée par l
’
hystérosalpingographie classique (2, 3).
L
’
échographie endovaginale recherche également des lésions tubaires
(hydrosalpinx) mais permet aussi de dépister d
’
autres pathologies
impliquées dans l
’
infertilité (4) comme une endométriose pelvienne, de
l
’
adénomyose utérine, des myomes utérins ou des malformations utérines pouvant gêner l
’
implantation
de l
’
embryon. L
’
IRM pelvienne peut être indiquée en cas d
’
échographie pelvienne anormale pour faire un
bilan exhaustif des lésions d
’
endométriose pelvienne profonde, faire une cartographie optimale des
myomes ou compléter le bilan de malformations utérines (5).
L
’
échographie pelvienne, combinée aux dosages hormonaux (FSH, œstradiol, AMH) a également un rôle
pronostic majeur pour prédire le taux de réussite de l
’
AMP en évaluant la réserve ovarienne (6). En effet,
le comptage des follicules antraux (follicules mesurés de 2 à 10 mm à J3 du cycle) est un reflet de la
réserve ovarienne et permet d
’
orienter les traitements (stimulation ovarienne).
Actuellement l
’
IRM pelvienne n
’
a pas sa place en routine pour établir des facteurs pronostics de réussite
de l
’
implantation. Cependant, de nombreuses études ont montré que les variations physiologiques de
l
’
utérus au cours du cycle pouvaient être suivies en IRM pelvienne.
Ainsi, l
’
IRM pelvienne permet de visualiser les contractions utérines. Physiologiquement, les
contractions utérines au cours de la phase proliférative permettent de faciliter le transport des
spermatozoïdes vers les trompes, et la diminution de ces contractions lors de la phase sécrétoire
faciliterait l
’
implantation du blastocyste (7). De même, des modifications de la vascularisation de la
zone myométriale interne ont été décrites lors de la phase péri
-
ovulatoire et ovulatoire (8). Des
pathologies comme l
’
endométriose pelvienne et l
’
adénomyose vont altérer ces processus physiologiques
et contribuer à diminuer la fertilité (9).
Avant de débuter une stimulation hormonale, une mammographie est recommandée seulement dans
certaines situations : si une anomalie clinique est retrouvée lors de l
’
examen, chez les patientes ayant
un âge supérieur à 37 ans ou ayant un haut risque de cancer du sein. Dans ce cas, une mammographie
numérique associée à une échographie mammaire est à privilégier chez ces patientes jeunes ayant une
densité mammaire souvent élevée.
Au cours de la prise en charge, l
’
imagerie, toujours combinée aux dosages hormonaux, permet une
surveillance de la croissance folliculaire en évaluant le nombre de follicules sélectionnés. Les résultats
échographiques permettent au clinicien d
’
ajuster la dose de stimulation, d
’
arrêter la stimulation s
’
il
existe un risque d
’
hyperstimulation avec réponse ovarienne majeure ou, si le ou les follicules sont
arrivés à maturité (diamètre folliculaire moyen entre 17 et 18 mm), de déclencher l
’
ovulation par
injection HCG dans le cadre d
’
une insémination ou encore de programmer une ponction folliculaire s
’
il
s
’
agit d
’
une FIV (10
-
12).
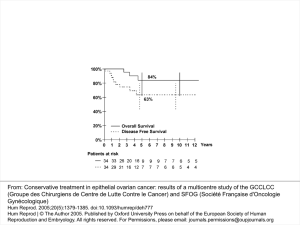
À long terme, la problématique posée par le traitement en AMP est
l
’
augmentation du risque de cancers gynécologiques (sein, ovaires,
utérus). Si les premières études de la littérature semblaient démontrer
l
’
existence d
’
une augmentation du risque de cancer du sein chez les
patientes ayant bénéficié d
’
un traitement par procréation médicalement
assistée, les études de cohorte et cas témoins les plus récentes
tendent à prouver l
’
absence de lien. Ces résultats sont à interpréter
avec prudence compte tenu de la présence de nombreux facteurs
confondants (infertilité, nulliparité, densité mammaire...) et de
l
’
absence d
’
étude permettant un suivi suffisamment long pour atteindre
l
’
âge moyen de survenue de cancer du sein (13
-
16). En ce qui concerne
le risque de cancer ovarien, aucun sur
-
risque n
’
a été constaté dans les
différentes études (17
-
19). En revanche, l
’
exposition prolongée au
citrate de clomiphéne augmenterait le risque de cancer de l
’
endomètre
(20).
En conclusion, l
’
imagerie occupe une place fondamentale dans l
’
AMP et

le radiologue a un rôle important dans la prise en charge de ces
patientes.
Fig. 1 – Échographie : Coupe sagittale médiane sur l
’
utérus pour mesure
de l
’
endomètre en cours de stimulation.
Fig. 2 – IRM : Coupe sagittale en pondération T2 : Endométriose sous
péritonéale postérieure avec aspect de symphyse du Douglas.
Références
1. Thurmond AS. Imaging of female infertility. Radiol Clin North Am. 2003 Jul;41(4):757
-
67
2. Frye RE, Ascher SM, Thomasson D. MR hysterosalpingography: protocol development and refinement
for simulating normal and abnormal fallopian tube patency
--
feasibility study with a phantom. Radiology.
2000 Jan;214(1):107
-
12.
3. Sadowski EA, Ochsner JE, Riherd JM, Korosec FR, Agrawal G, Pritts EA, Kliewer MA. MR
hysterosalpingography with an angiographic time
-
resolved 3D pulse sequence: assessment of tubal
patency. AJR Am J Roentgenol. 2008 Nov;191(5):1381
-
5.
4. Steinkeler JA, Woodfield CA, Lazarus E, Hillstrom MM. Female infertility: a systematic approach to
radiologic imaging and diagnosis. Radiographics. 2009 Sep
-
Oct;29(5):1353
-
70
5. Imaoka I, Wada A, Matsuo M, Yoshida M, Kitagaki H, Sugimura K. MR imaging of disorders associated
with female infertility: use in diagnosis, treatment, and management. Radiographics. 2003 Nov
-
Dec;23
(6):1401
-
21
6. Scheffer GJ, Broekmans FJ, Looman CW, Blankenstein M, Fauser BC, teJong FH, teVelde ER. The
number of antral follicles in normal women with proven fertility is the best reflection of reproductive
age. Hum Reprod. 2003 Apr;18(4):700
-
6
7. Leyendecker G, Kunz G, Wildt L, Beil D, Deininger H. Uterine hyperperistalsis and dysperistalsis as
dysfunctions of the mechanism of rapid sperm transport in patients with endometriosis and infertility.
Hum Reprod. 1996 Jul;11(7):1542
-
51
8. Thomassin
-
Naggara I, Balvay D, Cuenod CA, Daraï E, Marsault C, Bazot M. Dynamic contrast
-
enhanced MR imaging to assess physiologic variations of myometrial perfusion. Eur Radiol. 2010 Apr;20
(4):984
-
94
9. Kunz G, Beil D, Huppert P, Leyendecker G. Structural abnormalities of the uterine wall in women with
endometriosis and infertility visualized by vaginal sonography and magnetic resonance imaging. Hum
Reprod. 2000 Jan;15(1):76
-
82
10. Duran HE, Morshedi M, Kruger T, Oehninger S.Hum Reprod Update. 2002 Jul
-
Aug;8(4):373
-
84.
Intrauterine insemination: a systematic review on determinants of success.
11. Frattarelli JL, Levi AJ, Miller BT, Segars JH.A prospective assessment of the predictive value of basal
antral follicles in in vitro fertilization cycles. Fertil Steril. 2003 Aug;80(2):350
-
5
12. Aboulghar M. Prediction of ovarian hyperstimulation syndrome (OHSS). Estradiol level has an
important role in the prediction of OHSS. Hum Reprod. 2003 Jun;18(6):1140
-
1
13. Land JA, Evers JL. Risks and complications in assisted reproduction techniques: Report of an ESHRE
consensus meeting. Hum Reprod. 2003 Feb;18(2):455
-
7
14. Pike MC, Spicer DV, Dahmoush L, Press MF. Estrogens, progestogens, normal breast cell
proliferation, and breast cancer risk. Epidemiol Rev. 1993;15(1):17
-
35.
15. Burkman RT, Tang MT, Malone KE. Infertility drugs and the risk of breast cancer: findings from the
National Institute of Child Health and Human Development Women
’
s Contraceptive and Reproductive
Experiences Study. Fertil Steril. 2003 Apr;79(4):844
-
51.
16. Rossing MA, Daling JR, Weiss NS, Moore DE, Self SG. Risk of breast cancer in a cohort of infertile
women. Gynecol Oncol. 1996 Jan;60(1):3
-
7.
17. Potashnik G, Lerner
-
Geva L, Genkin L, Chetrit A, Lunenfeld E, Porath A. Fertility drugs and the risk of
breast and ovarian cancers: results of a long
-
term follow
-
up study. Fertil Steril. 1999 May;71(5):853
-
9.
18. Venn A, Watson L, Lumley J, Giles G, King C, Healy D. Breast and ovarian cancer incidence after
infertility and in vitro fertilisation. Lancet. 1995 Oct 14;346(8981):995
-
1000.
19. Crit Rev Oncol Hematol. 1997 Jan;25(1):1
-
9. Estrogen action in human ovarian cancer. Clinton GM,
Hua W.
20. Calderon
-
Margalit R, Friedlander Y, Yanetz R, Kleinhaus K, Perrin MC, Manor O, Harlap S, Paltiel O.
Cancer risk after exposure to treatments for ovulation induction. Am J Epidemiol. 2009 Feb 1;169
(3):365
-
75.
1
/
2
100%