Anesthésie-réanimation en chirurgie du

36-575-A-10
Anesthésie-réanimation
en
chirurgie
du
cancer
de
l’œsophage
B.
Capron,
H.
Le
Frêche,
C.
Mariette,
G.
Lebuffe
La
chirurgie
pour
cancer
de
l’œsophage
est
associée
à
une
morbimortalité
périopératoire
élevée
en
lien
avec
des
complications
pulmonaires
et
chirurgicales,
notamment
la
fistule
anastomotique.
L’évolution
des
techniques
chirurgicales
et
d’anesthésie-réanimation
a
permis
une
meilleure
approche
dans
la
compré-
hension
des
mécanismes
physiopathologiques
et
une
meilleure
prise
en
charge
dans
la
prévention
et
le
traitement
de
ces
complications.
La
recherche
préopératoire
des
facteurs
de
risque
de
morbimortalité
permet
d’identifier
les
patients
à
risque
de
complication.
Aussi,
la
morbidité
pulmonaire
est
influencée
par
la
stratégie
anesthésique
associant
l’analgésie
péridurale,
l’optimisation
du
remplissage
et
la
ventilation
protectrice.
Ces
procédures
anesthésiques
favorisent
également
la
réhabilitation
et
l’extubation
précoces.
Dans
ce
contexte,
l’anesthésie
générale
associée
à
une
analgésie
locorégionale
est
la
technique
de
choix.
La
surveillance
postopératoire
doit
être
multidisciplinaire
afin
de
diagnostiquer
et
traiter
précocement
les
complications.
La
place
d’un
traitement
immunomodulateur
comme
la
corticothérapie
reste
à
définir.
©
2014
Elsevier
Masson
SAS.
Tous
droits
réservés.
Mots-clés
:
Anesthésie
;
Œsophagectomie
;
Cancer
œsophagien
;
Analgésie
péridurale
thoracique
;
Ventilation
unipulmonaire
;
Immunomodulation
;
Syndrome
de
détresse
respiratoire
aiguë
Plan
■Introduction
1
■Chirurgie
hirurgie
et
retentissement
2
■Prise
en
charge
préopératoire
2
Épidémiologie
3
Évaluation
préopératoire
3
Sélection
des
patients
opérables
5
Préparation
préopératoire
5
■Prise
en
charge
peropératoire
5
Gestion
anesthésique
5
Analgésie
locorégionale
périmédullaire
6
Technique
chirurgicale
7
Mise
en
condition
7
Gestion
de
la
ventilation
7
Stratégie
d’optimisation
hémodynamique
8
Gestion
de
la
transfusion
8
Antibioprophylaxie
8
Complications
peropératoires
8
■Prise
en
charge
postopératoire
8
Surveillance
de
la
plastie
digestive
8
Analgésie
postopératoire
:
l’analgésie
péridurale
thoracique
9
Kinésithérapie
et
mobilisation
précoce
9
Ventilation
non
invasive
9
Nutrition
postopératoire
9
Immunomodulation
10
Complications
postopératoires
10
■Conclusion
11
Introduction
Le
cancer
de
l’œsophage
touche
chaque
année
près
de
4300
personnes
en
France
(données
INRS
2011),
en
particulier
les
hommes
(sex-ratio
de
2,75)
pour
lesquels
il
constitue
la
quatrième
cause
de
mortalité
par
cancer.
Les
trois
quarts
de
ces
tumeurs
sont
des
cancers
épidermoïdes,
liés
à
la
consommation
d’alcool
et
de
tabac.
Le
second
type,
l’adénocarcinome,
développé
sur
endobra-
chyœsophage,
survient
dans
un
contexte
d’obésité
et
de
reflux
gastro-œsophagien.
Son
incidence
est
en
constante
augmentation
de
fac¸on
parallèle,
mais
retardée
par
rapport
à
ce
qui
est
observé
aux
États-Unis
depuis
plus
de
20
ans [1].
Le
pronostic
du
cancer
de
l’œsophage
est
sombre
du
fait
d’un
diagnostic
tardif
et
du
mauvais
terrain,
et
stagne
à
environ
10
%
de
survie
à
cinq
ans [2,
3].
Lorsque
la
tumeur
est
«
facilement
»
résécable
et
le
patient
opérable,
le
traitement
curatif
de
référence
est
la
chirurgie,
per-
mettant
d’obtenir
une
probabilité
de
survie
à
cinq
ans
de
l’ordre
de
30
%[3],
mais
entraînant
une
morbimortalité
périopératoire
élevée,
liée
principalement
aux
complications
pulmonaires
et
chi-
rurgicales [4].
La
prise
en
charge
périopératoire
du
cancer
de
l’œsophage
a
considérablement
évolué
ces
dernières
années
grâce
à
une
amé-
lioration
de
la
sélection
des
patients,
à
l’apparition
de
techniques
chirurgicales
mini-invasives,
ainsi
qu’à
une
optimisation
de
la
prise
en
charge
anesthésique
depuis
la
phase
préopératoire
jusqu’à
la
réhabilitation
postopératoire.
EMC
-
Anesthésie-Réanimation 1
Volume
11
>
n◦2
>
avril
2014
http://dx.doi.org/10.1016/S0246-0289(13)59009-8
© 2014 Elsevier Masson SAS. Tous droits réservés. - Document téléchargé le 11/04/2014 par SCD Paris Descartes (292681)

36-575-A-10 Anesthésie-réanimation
en
chirurgie
du
cancer
de
l’œsophage
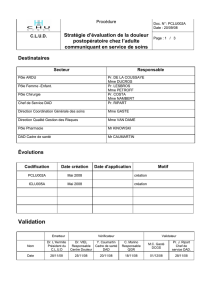
Figure
1.
Principes
de
réalisation
d’une
œsophagectomie
avec
rempla-
cement
de
l’œsophage
par
gastroplastie
(flèche).
Chirurgie
et
retentissement
Les
deux
principales
voies
d’abord
pour
la
résection
d’une
tumeur
œsophagienne
sont
la
voie
transthoracique
(TT)
droite,
avec
une
anastomose
au
sommet
du
thorax
ou
en
cervical,
et
la
voie
trans-hiatale
(TH),
avec
une
anastomose
cervicale
sans
tho-
racotomie.
La
voie
TT
offre
une
meilleure
dissection
tumorale
et
ganglionnaire
intrathoracique,
associée
à
un
risque
moindre
de
lésions
des
organes
adjacents.
Avec
la
voie
TH,
une
diminution
de
la
morbidité
postopératoire
est
théoriquement
attendue,
en
lien
avec
la
gravité
moins
importante
des
fistules
et
une
durée
d’intervention
plus
courte.
Le
choix
de
la
technique
chirurgicale
est
dépendant
de
l’état
général
et
de
l’évaluation
préopératoire
du
patient,
des
constata-
tions
peropératoires
et
de
la
philosophie
de
l’équipe
chirurgicale
quant
à
l’étendue
de
la
résection
et
la
technique
de
reconstruc-
tion.
Toutefois,
l’ensemble
de
la
littérature
chirurgicale
s’accorde
sur
le
fait
que
le
facteur
pronostique
le
plus
important
dans
le
cancer
de
l’œsophage
est
la
résection
complète
macroscopique
et
microscopique.
Ce
type
de
résection
ne
pouvant
être
réalisé
que
par
une
résection
en
bloc
de
la
tumeur
primitive
et
des
ganglions
régionaux,
la
voie
TT
est
devenue
la
technique
chi-
rurgicale
de
référence
associée
aux
meilleurs
taux
de
survie
à
5
ans
variant
de
43
à
49
%
contre
0
à
11
%
en
cas
de
résection
incomplète [5].
Les
points
communs
des
différentes
techniques
sont
la
libé-
ration
complète
de
l’estomac,
ou
gastrolyse,
puis
la
formation
d’un
tube
avec
l’estomac
libéré
(gastroplastie)
(Fig.
1).
Ce
temps
abdominal
est
réalisé
par
laparotomie
ou
par
laparoscopie.
L’intervention
est
poursuivie
par
la
libération
totale
de
l’œsophage
le
plus
souvent
par
une
thoracotomie
ou
une
thoracoscopie
droite.
Pour
les
tumeurs
du
bas
œsophage,
l’intervention
de
Lewis-
Santy,
ou
double
voie,
sera
réalisée
par
une
laparoscopie
ou
une
laparotomie
associée
à
une
thoracotomie
ou
une
thoracoscopie
droite.
La
gastroplastie
est
anastomosée
avec
l’œsophage
natif
en
intrathoracique
(Fig.
2).
En
cas
de
tumeur
du
tiers
supérieur
de
l’œsophage,
l’œsophagectomie
totale
nécessite
le
rétablissement
de
la
continuité
par
une
gastroplastie
raccordée
par
voie
cervicale
gauche.
La
technique
nécessite
une
triple
voie
d’abord
de
la
cavité
abdominale,
du
thorax
à
droite
et
du
cou
en
cervical
gauche.
La
Figure
2.
Intervention
par
double
voie
d’abord,
abdominal
et
thora-
cique
droit
(intervention
de
Lewis-Santy).
L’installation
habituelle
consiste
à
placer
d’abord
le
patient
en
décubitus
dorsal
pour
la
réalisation
du
temps
abdominal,
puis
en
décubitus
latéral
gauche
pour
le
temps
thoracique.
La
gastroplastie
préparée
par
laparotomie
ou
laparoscopie
est
ensuite
anasto-
mosée
en
intrathoracique
avec
l’œsophage
natif,
avec
des
fils
de
repérage
(pointillé).
Figure
3.
Intervention
d’Akiyama,
avec
une
triple
voie
d’abord,
consis-
tant
à
réaliser
en
premier
la
gastroplastie,
puis
à
l’ascensionner
dans
un
trajet
rétrosternal
et
à
l’anastomoser
à
l’œsophage
cervical.
L’exérèse
de
l’œsophage
et
de
la
tumeur
est
réalisée
ensuite
par
thoracotomie
droite.
position
de
la
plastie,
rétrosternale
ou
dans
le
lit
médiastinal
pos-
térieur,
définit
l’intervention
d’Akiyama
(Fig.
3)
ou
de
Mc
Keown
(Fig.
4).
Dans
certains
cas,
l’ouverture
du
thorax
est
évitée
par
la
voie
TH,
avec
une
laparotomie
et
un
abord
cervical
gauche
(Fig.
5).
Prise
en
charge
préopératoire
Bien
que
durant
ces
30
dernières
années
la
mortalité
postopé-
ratoire
de
la
chirurgie
de
l’œsophage
ait
diminué
pour
atteindre
3
à
11
%
selon
les
auteurs [4,
6–8],
la
morbidité
–en
grande
partie
2EMC
-
Anesthésie-Réanimation
© 2014 Elsevier Masson SAS. Tous droits réservés. - Document téléchargé le 11/04/2014 par SCD Paris Descartes (292681)

Anesthésie-réanimation
en
chirurgie
du
cancer
de
l’œsophage 36-575-A-10
Figure
4.
Intervention
de
Mc
Keown,
avec
une
triple
voie
d’abord,
consistant
à
réaliser
en
premier
l’exérèse
de
l’œsophage
et
de
la
tumeur
par
thoracotomie
droite,
puis
à
réaliser
la
gastroplastie
et
à
l’ascensionner
dans
un
trajet
médiastinal
postérieur,
et
à
l’anastomoser
à
l’œsophage
cervical.
Figure
5.
Intervention
par
double
abord
abdominal
et
cervical
(œsophagectomie
sans
thoracotomie
ou
œsophagectomie
par
voie
trans-hiatale).
La
dissection
de
l’œsophage
est
aveugle
du
défilé
cervi-
comédiastinal
à
la
carène.
Son
exérèse
libère
le
médiastin
postérieur
où
sera
positionnée
la
gastroplastie.
respiratoire
–
reste
élevée
(30–40
%).
Son
amélioration
dépend
de
la
connaissance
précise
des
facteurs
de
risque
afin
d’effectuer
une
sélection
appropriée
des
patients,
du
choix
de
la
technique
chi-
rurgicale
et
de
sa
réalisation,
et
de
l’optimisation
de
la
prise
en
charge
périopératoire.
Épidémiologie
Facteurs
de
mortalité
après
œsophagectomie
L’expérience
de
l’équipe
chirurgicale,
le
nombre
d’œsophagectomies
réalisées
annuellement
et
la
morbidité
pulmonaire
(notamment
l’insuffisance
respiratoire
aiguë
et
le
syndrome
de
détresse
respiratoire
aiguë)
sont
les
principaux
critères
influenc¸ant
la
mortalité
postopératoire [9,
10].
Parmi
les
facteurs
liés
au
patient,
le
risque
de
décès
est
augmenté
en
cas
de
diabète
et
chez
les
sujets
dyspnéiques
et/ou
âgés [11].
Facteurs
de
morbidité
postopératoire
Les
facteurs
associés
à
une
augmentation
de
la
morbidité
car-
diorespiratoire
peuvent
être
:
•liés
au
patient
:
diabète,
existence
d’une
dyspnée,
maladie
vasculaire
périphérique,
antécédent
d’accident
vasculaire
céré-
bral,
bronchopathie
chronique
obstructive
(BPCO)
;
classe
ASA
(supérieure
ou
égale
à
3)
;
perte
de
poids
(supérieure
à
10
%
les
six
derniers
mois)
;
radiothérapie
dans
les
90
jours
précédant
la
chirurgie [11] ;
•
liés
à
la
chirurgie
:
caractère
«
propre–contaminé
»
de
la
chirur-
gie
;
transfusion
peropératoire,
durée
de
la
chirurgie [11].
Les
facteurs
associés
spécifiquement
à
la
survenue
des
complications
pulmonaires
postopératoires
sont
l’âge,
le
taba-
gisme,
la
présence
de
comorbidités,
un
volume
expiratoire
maximal
par
seconde
(VEMS)
inférieur
à
65
%
de
la
valeur
théo-
rique,
une
limitation
à
l’exercice
physique,
et
l’abord
chirurgical
par
voie
TT [9,
10,
12].
Évaluation
préopératoire
Évaluation
cardiorespiratoire
Le
bilan
paraclinique
de
base
comprend
la
réalisation
d’explorations
fonctionnelles
respiratoires,
avec
évaluation
de
la
DLCO
(diffusion
libre
du
CO)
et
de
la
gazométrie
artérielle.
Mais
c’est
l’évaluation
de
la
tolérance
à
l’effort
qui
sera
la
plus
adéquate
pour
refléter
les
fonctions
pulmonaires
et
car-
diovasculaires
du
patient.
Cette
capacité
fonctionnelle
peut
être
exprimée
en
équivalents
métaboliques
(MET),
correspondant
à
une
valeur
de
consommation
d’oxygène
et
pouvant
être
estimée
à
l’interrogatoire
par
l’activité
physique
réalisable
par
le
patient [13]
(Tableau
1).
Une
valeur
de
consommation
en
oxygène
(VO2)
maximale
à
moins
de
20
et
15
ml
kg–1 min–1 a
été
respectivement
associée
à
44
et
86
%
de
complications
cardiorespiratoires [14].
Un
test
de
marche
pourra
être
également
pratiqué
à
l’occasion
du
bilan
préopératoire,
afin
d’évaluer
de
manière
objective
la
réserve
fonctionnelle
du
sujet.
Ce
test
consiste
à
demander
au
patient
de
marcher
le
plus
vite
possible
pendant
six
minutes,
en
incluant
des
périodes
de
repos
si
besoin.
Une
oxygénothérapie
peut
être
administrée
afin
de
maintenir
une
saturation
artérielle
en
oxygène
supérieure
à
90
%.
La
distance
parcourue
est
notée
en
fin
de
test.
Une
distance
parcourue
inférieure
à
200
m
serait
un
facteur
indépendant
de
mortalité
postopératoire
lors
d’une
chi-
rurgie
de
réduction
pulmonaire [15].
Son
utilisation
en
pratique
quotidienne
est
devenue
systématique,
mais
sa
véritable
valeur
prédictive
reste
à
démontrer
spécifiquement
pour
la
chirurgie
de
l’œsophage.
L’électrocardiogramme
sera
réalisé
systématiquement.
Une
échocardiographie
de
repos
sera
proposée
en
fonction
des
don-
nées
de
l’interrogatoire
(notion
de
dyspnée)
ou
de
l’examen
clinique
(souffle
cardiaque).
Chez
un
patient
coronarien
ou
présentant
plusieurs
facteurs
de
risque
cardiovasculaire,
la
chirurgie
œsophagienne
est
considérée
comme
«
une
chirurgie
à
risque
intermédiaire
»,
correspondant
à
une
fréquence
d’événements
cardiaques
périopératoires
comprise
entre
1
et
5
%.
L’évaluation
du
risque
cardiaque
repose
sur
le
score
de
Lee
clinique
(Tableau
2).
La
présence
de
trois
facteurs
chez
un
patient
aux
capacités
fonctionnelles
limitées
ou
non
évaluables
nécessite
la
réalisation
d’un
test
de
dépistage
d’une
cardiopathie
ischémique [16].
EMC
-
Anesthésie-Réanimation 3
© 2014 Elsevier Masson SAS. Tous droits réservés. - Document téléchargé le 11/04/2014 par SCD Paris Descartes (292681)

36-575-A-10 Anesthésie-réanimation
en
chirurgie
du
cancer
de
l’œsophage
Tableau
1.
Estimation
du
risque
chirurgical
en
fonction
de
la
capacité
fonctionnelle
du
patient
(d’après [13]).
Aptitude
physique
(échelle
de
Dukes)
MET
VO2estimée
(ml
kg–1 min–1)
Activité
physique
réalisable
sans
symptômes
Risque
chirurgical
estimé
Excellente
>
10
>
35
Natation
Tennis
en
simple
Ski
de
fond
Athlétisme
Basket-ball
Faible
Très
bonne
à
bonne
7–10
24,5–35
Tennis
en
double,
football
Danse
Gros
travaux
d’entretien
dans
la
maison
Courir
sur
une
courte
distance
Monter
en
haut
d’une
colline
Monter
deux
étages
ou
plus
Marcher
rapidement
sur
terrain
plat
Modérée 4–7
14–24,5
Monter
deux
étages
Faire
du
ménage
Faible
<
4<
14 Marcher
sur
terrain
plat
à
3–5
km
h–1
Marcher
à
l’intérieur
de
son
domicile
Faire
sa
toilette,
s’habiller,
manger
D’intermédiaire
à
élevé
Non
évaluable ? ? Aucune
MET
:
équivalent
métabolique
;
VO2:
valeur
de
consommation
en
d’oxygène.
Tableau
2.
Score
de
risque
cardiaque ade
Lee [16].
Calcul
du
score
de
Lee
classique
Facteur
de
risque
Calcul
du
score
de
Lee
clinique
1
point
Chirurgie
à
haut
risque
:
chirurgie
vasculaire
supra-inguinale,
intrathoracique
ou
intrapéritonéale
1
point
Coronaropathie
:
antécédent
d’infarctus
du
myocarde,
angor
clinique,
utilisation
de
nitrés,
onde
Q
à
l’ECG
ou
test
non
invasif
de
la
circulation
coronaire
positif
1
point
1
point
Insuffisance
cardiaque
:
antécédent
d’insuffisance
cardiaque
congestive,
d’œdème
pulmonaire,
dyspnée
nocturne
paroxystique,
crépitants
bilatéraux,
galop
B3
ou
redistribution
vasculaire
radiologique
1
point
1
point
Antécédent
d’accident
vasculaire
cérébral
ischémique
ou
d’accident
cérébral
ischémique
transitoire
1
point
1
point
Diabète
insulinorequérant
1
point
1
point
Insuffisance
rénale
chronique
définie
par
une
créatininémie
>
2
mg/dl
(177
mol/l)
1
point
aLe
risque
d’événement
cardiaque
périopératoire
en
chirurgie
non
cardiaque
en
fonction
du
nombre
de
points
obtenus
avec
le
score
de
Lee
sera
respectivement
de
:
0
point
:
0,4
%
;
1
point
:
0,9
%
;
2
points
:
7
%,
3
points
ou
moins
de
3
points
:
11
%.
Des
scores
pronostiques
sont
proposés
pour
stratifier
le
risque
cardiorespiratoire
et
permettre
une
sélection
dirigée
des
candi-
dats
à
une
œsophagectomie.
Ils
sont
volontiers
établis
à
partir
de
critères
comme
l’âge,
la
performance
physique
et
le
VEMS [17]
(Tableau
3).
Évaluation
de
la
fonction
hépatique
La
réalisation
d’une
œsophagectomie
chez
un
patient
cir-
rhotique
augmente
le
risque
de
décès
postopératoire.
L’ascite
est
la
complication
la
plus
fréquente,
probablement
associée
à
l’interruption
de
la
circulation
collatérale
œsophagienne
au
cours
de
la
chirurgie.
Les
facteurs
préopératoires
à
prendre
en
compte
sont
le
degré
d’insuffisance
hépatocellulaire
estimé
par
le
score
de
Child
et
le
taux
de
prothrombine [18].
Une
chirurgie
œsopha-
gienne
peut
être
envisagée
chez
les
patients
avec
un
score
de
Child-Pugh
A,
voire
B,
et
un
taux
de
prothrombine
(TP)
supérieur
à
60
%[19,
20].
Les
complications
pulmonaires
ne
semblent
pas
plus
élevées
chez
le
cirrhotique.
Effets
secondaires
des
traitements
néoadjuvants
Les
traitements
néoadjuvants
entraînent
une
augmentation
de
la
morbidité
respiratoire [11],
liée
à
une
immunodépression
et
à
une
altération
des
capacités
de
diffusion
pulmonaire
estimée
par
la
mesure
de
la
DLCO [12].
L’association
fréquente
du
cisplatine
et
du
5-fluorouracil
requiert
une
évaluation
cardiaque
et
hématolo-
gique
2
à
4
semaines
après
la
fin
des
séances.
Évaluation
de
l’état
nutritionnel
(cancer
et
difficultés
d’alimentation)
Le
cancer
de
l’œsophage
et
ses
difficultés
d’alimentation
favo-
risent
la
dénutrition.
Celle-ci
augmente
le
risque
de
complications
infectieuses
et
de
fistule
anastomotique
par
altération
du
système
immunitaire
et
des
capacités
de
cicatrisation.
La
pathologie
carcinologique,
la
dysphagie,
et
les
traitements
néoadjuvants
sont
les
principaux
facteurs
de
risque
de
dénutri-
tion [21] (Tableau
4).
L’interrogatoire
doit
rechercher
la
présence
d’autres
facteurs
de
dénutrition
(Tableau
5),
et
l’existence
d’une
dénutrition
définie
selon
les
critères
suivants
:
indice
de
masse
corporelle
(IMC)
supé-
rieur
ou
égal
à
18,5
kg/m2ou
inférieur
à
21
kg/m2chez
le
sujet
de
plus
de
70
ans,
ou
perte
de
poids
récente
d’au
moins
10
%,
ou
albu-
minémie
inférieure
à
30
g/l,
indépendamment
de
la
protéine
C
réactive
(C
reactive
proteine
[CRP]) [21].
Ces
données
de
l’interrogatoire
permettent
de
stratifier
le
risque
nutritionnel
du
patient
et
d’établir
la
stratégie
de
prise
en
charge
nutritionnelle
préopératoire.
En
l’absence
de
dénutri-
tion,
le
patient
bénéficie
de
conseils
diététiques
et
de
l’apport
de
compléments
nutritionnels.
En
revanche,
s’il
est
dénutri,
une
assistance
nutritionnelle
préopératoire
de
7
à
10
jours
est
pré-
conisée.
Dans
les
deux
cas,
il
est
recommandé
de
prescrire
en
préopératoire,
pendant
5
à
7
jours,
un
mélange
nutritif
utilisable
par
voie
digestive
et
contenant
une
association
de
pharmaconutri-
ments
démontrée
pour
réduire
la
morbidité
postopératoire [21,
22].
4EMC
-
Anesthésie-Réanimation
© 2014 Elsevier Masson SAS. Tous droits réservés. - Document téléchargé le 11/04/2014 par SCD Paris Descartes (292681)

Anesthésie-réanimation
en
chirurgie
du
cancer
de
l’œsophage 36-575-A-10
Tableau
3.
Score
de
risque
de
Ferguson
et
Durkin [17].
Facteur
évalué
Segmentation
Score
AÂge
>
50
ans <
51
0
51–60
1
61–70
2
71–80
3
>
80
4
BVEMS
(en
pourcentage
de
la
normale)
≥
90
0
80–89,9
1
70–77,9
2
60–69,9
3
<
60
4
CPerformance
physique Activité
normale
0
Activité
soutenue
limitée 1
Ambulatoire
et
autonome,
mais
activité
professionnelle
impossible
2
Autonomie
limitée,
confinement
au
fauteuil
ou
au
lit
d’au
moins
50
%
3
Perte
complète
d’autonomie
4
Total
A
+
B
+
CIncidence
des
complications
cardiorespiratoires
en
fonction
de
la
valeur
du
score
0–1
21
%
2–3
41
%
4–5
46
%
6–7
62
%
≥
8
91
%
VEMS
:
volume
expiratoire
maximal
par
seconde.
Évaluation
des
comorbidités
liées
aux
facteurs
de
risque
du
cancer
Le
carcinome
épidermoïde
est
la
forme
anatomopatholo-
gique
la
plus
fréquente
du
cancer
de
l’œsophage.
Toutefois,
l’adénocarcinome
est
en
constante
progression [23].
Cette
évo-
lution
reflète
une
diminution
des
terrains
alcoolotabagiques
et
surtout
l’incidence
croissante
du
reflux
gastro-œsophagien
(RGO)
et
de
l’obésité
morbide
étant
les
principaux
facteurs
de
risque
de
l’endobrachyœsophage
et
de
sa
transformation
vers
l’adénocarcinome [1].
Ces
patients
se
présentent
le
plus
souvent
avec
un
meilleur
état
général
et
nutritionnel,
notamment
ceux
porteurs
d’un
adénocarcinome
sur
RGO.
Sélection
des
patients
opérables
À
l’issue
du
bilan
préopératoire,
une
chirurgie
curative
n’est
possible
que
chez
15
à
20
%
des
patients
en
raison
de
contre-
indications
liées
au
terrain
ou
à
l’extension
tumorale.
Les
indications
thérapeutiques
sont
les
mêmes
pour
les
carcinomes
épidermoïdes
et
les
adénocarcinomes,
malgré
leurs
différences
en
termes
de
physiopathologie
et
d’anatomopathologie.
Les
critères
de
non-opérabilité
sont
présentés
dans
le
Tableau
6.
Préparation
préopératoire
La
précocité
de
la
consultation
préanesthésique
est
essentielle
pour
préparer
au
mieux
à
l’intervention.
Le
sevrage
tabagique
est
à
réaliser
le
plus
tôt
possible,
soit,
dans
l’idéal,
au
moins
huit
semaines
avant
la
procédure
chirurgicale.
Passé
ce
délai,
son
bénéfice
pour
diminuer
les
complications
pul-
monaires
n’a
pas
été
prouvé.
Toutefois,
aucun
effet
délétère
sur
la
morbidité
postopératoire
n’a
été
observé
lorsque
le
sevrage
est
réalisé
plus
tardivement.
Il
convient
donc
d’inciter
les
patients
à
l’arrêt
systématique
de
toute
consommation
tabagique
avant
la
chirurgie [24].
La
préparation
respiratoire
concerne
tous
les
patients,
notam-
ment
ceux
porteurs
des
comorbidités
pulmonaires.
Elle
comporte
une
information
et
une
éducation
du
patient
sur
l’analgésie
périmédullaire
et
la
nécessité
d’une
physiothérapie
respira-
toire
postopératoire
(spirométrie
incitative
et
éducation
aux
manœuvres
d’évacuation
des
sécrétions).
Un
programme
de
réhabilitation
respiratoire
peut
être
discuté
dès
le
stade
IIA
des
patients
porteurs
d’une
BPCO
(VEMS
entre
50
et
80
%
et
VEMS/CV
inférieurs
à
70
%),
dans
la
mesure
où
le
bénéfice
attendu
de
celui-ci
tient
compte
du
risque
de
report
de
l’intervention
chirurgicale.
Il
dure
en
moyenne
de
2
à
4
semaines
et
comprend
une
réédu-
cation
à
l’effort,
de
la
kinésithérapie
et
une
optimisation
du
traitement
médical [25,
26].
Prise
en
charge
peropératoire
La
prise
en
charge
peropératoire
de
l’œsophagectomie
repose
principalement
sur
la
prévention
des
complications
respiratoires,
la
précocité
du
sevrage
ventilatoire,
une
réhabilitation
postopéra-
toire
rapide,
et
la
garantie
de
la
viabilité
de
la
plastie
digestive.
Dans
ce
contexte,
l’association
d’une
anesthésie
générale
à
une
analgésie
locorégionale
périmédullaire
per-
et
postopératoire
apparaît
comme
la
stratégie
de
choix.
Gestion
anesthésique
Aucune
recommandation
particulière
concernant
l’utilisation
d’un
agent
anesthésique
plutôt
qu’un
autre
ne
peut
être
faite.
Le
recours
aux
procédures
anesthésiques
(intraveineuse
ou
par
inhalation)
à
objectif
de
concentration
avec
monitorage
de
la
profondeur
de
l’anesthésie
semble
être
intéressant.
Les
béné-
fices
attendus
en
sont
une
réduction
des
doses
d’hypnotique
administrées
permettant
une
optimisation
hémodynamique,
un
sevrage
respiratoire
précoce
et
une
diminution
de
l’exposition
aux
hypnotiques
dont
les
conséquences
neurologiques
à
long
terme
semblent
incertaines.
En
effet,
des
données
expérimentales
sug-
gèrent
un
effet
délétère
des
agents
halogénés
sur
les
fonctions
cognitives [27].
Ces
résultats
restent
incertains
en
clinique
tant
la
physiopathologie
des
dysfonctions
cognitives
postopératoires
est
complexe [28].
EMC
-
Anesthésie-Réanimation 5
© 2014 Elsevier Masson SAS. Tous droits réservés. - Document téléchargé le 11/04/2014 par SCD Paris Descartes (292681)
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
1
/
14
100%