L Leucoencéphalopathie multifocale progressive après biothérapies

La Lettre de l’Infectiologue • Tome XXVI - n° 3 - mai-juin 2011 | 101
MISE AU POINT
Leucoencéphalopathie
multifocale progressive
après biothérapies
Progressive multifocal leukoencephalopathy
related to biotherapies
P. Vermersch*, O. Outteryck*
* Université de Lille − Nord-de-France
(EA2686).
L
a leucoencéphalopathie multifocale progres-
sive (LEMP) est une affection rare, secon-
daire à la réactivation du virus JC dans le
système nerveux central (SNC). Cette infection
virale s’observait surtout dans le cours évolutif
de certaines affections malignes, notamment
hématologiques, ou secondaires à une immuno-
suppression prolongée. Bien que l’avènement des
trithérapies ait favorisé sa diminution, la LEMP
s’observe souvent au cours du sida. L’affection
connaît un net regain d’intérêt depuis l’arrivée
de certaines biothérapies, entraînant une immu-
nosuppression sélective.
La LEMP en bref
Généralités
Les premières descriptions de LEMP datent de
plus d’un demi-siècle, chez des patients atteints
de maladie de Hodgkin et de leucémie lymphoïde
chronique (1). Un cas clinique de démence avec
lésions de nature démyélinisante avait été rapporté
dès 1930 (2). Le nombre de cas a été nettement
augmenté avec l’épidémie du sida, diminuant
ensuite sans les faire disparaître avec l’utilisation
des traitements antirétroviraux. Toutes ces circons-
tances, ainsi que les cas survenant au cours de
certains traitements cytotoxiques – avec la fluda-
rabine notamment (3) –, mettaient l’accent sur
le rôle majeur de l’immunosuppression à l’origine
de la LEMP. D’autres circonstances sont associées
à un risque accru de développer une LEMP, dont
la sarcoïdose (4) ou le lupus systémique. Outre
les agents cytotoxiques et certaines biothérapies
(cf. infra), des cas ont été recensés après cortico-
thérapies exclusives souvent très prolongées.
L’infection par le virus JC est fréquente et au moins
la moitié de la population a déjà été infectée par ce
dernier et a développé des anticorps antivirus JC (5).
Du virus JC est retrouvé dans différents tissus,
notamment la rate, le rein et la moelle hémato-
poïétique. Il est excrété de façon fréquente dans
les urines. Des cellules hématopoïétiques progéni-
trices, mais aussi les lymphocytes B et les cellules
pré-B pourraient être des réservoirs du virus (6).
Les mécanismes responsables du passage du virus
du sang vers le SNC ne sont pas connus. La primo-
infection pourrait se faire par voie respiratoire, le
plus souvent chez le sujet jeune. Le virus JC est
un virus à ADN de type polyomavirus. In vitro, le
virus JC infecte les cellules monocytaires et les
lymphocytes B alors que les variants pathogéniques
infectent volontiers les oligodendrocytes et les
astrocytes, responsables des lésions de démyélini-
sation et des signes de LEMP. Les mécanismes qui
sous-tendent les mutations du virus natif vers la
forme pathogène ne sont pas connus. Lors d’une
LEMP, des anticorps dirigés contre le variant VP1
sont presque toujours détectés dans le sang. La

102 | La Lettre de l’Infectiologue • Tome XXVI - n° 3 - mai-juin 2011
Résumé
La leucoencéphalopathie multifocale progressive (LEMP) est une infection opportuniste rare due au virus JC, qui
connaît un regain d’intérêt avec l’utilisation de certaines biothérapies, par exemple l’efalizumab, le rituximab
et le natalizumab. L’efalizumab a été rapidement retiré du marché après les 4 premiers cas. La mortalité liée à
la LEMP est beaucoup plus élevée avec le rituximab qu’avec le natalizumab, probablement du fait de la patho-
logie sous-jacente. Plus de 100 cas de LEMP sont survenus sous natalizumab dans l’indication de la sclérose
en plaques. Des plans de gestion du risque sont imposés avec l’utilisation de ces produits, notamment sur
les plans clinique et radiologique. La présence d’anticorps antivirus JC, une durée de traitement supérieure à
2 ans et l’utilisation préalable d’immunosuppresseurs sont des facteurs de risque reconnus d’une LEMP sous
natalizumab. Des techniques ultrasensibles d’amplification génique permettent un diagnostic plus rapide,
augmentant le taux de survie. Une restauration immunitaire est le seul traitement efficace.
Mots-clés
Leuco-
encéphalopathie
multifocale
progressive
Rapport bénéfice-
risque
Efalizumab
Rituximab
Natalizumab
Summary
Progressive multifocal leuko-
encephalopathy (PML) is a rare
opportunistic infection due to
reactivation of JC virus into the
central nervous system. The
interest for PML is increased
with the use of different
biotherapies, like efalizumab,
rituximab or natalizumab.
Efalizumab has rapidly been
removed from the market after
the first 4 cases. The mortality
rate is higher with rituximab
compared with natalizumab
probably due to underlying
diseases. More than 100 cases
have been described with the
use of natalizumab in multiple
sclerosis patients in post
marketing. Risk management
plans are mandatory for these
drugs in specific conditions
including clinical and MRI data.
Presence of antibodies against
JC virus, more than two years
of treatment duration and
previous use of immunosup-
pressant drugs are risk factors
for natalizumab-induced PML.
Ultrasensitive quantitative PCR
techniques are now available,
allowing a rapid diagnosis,
increasing the survival rate
and clinical outcomes.
Keywords
Progressive multifocal
leukoencephalopathy
Benefit risk ratio
Efalizumab
Rituximab
Natalizumab
pénétration cellulaire pourrait se faire via le récep-
teur sérotoninergique 5-HT2A retrouvé à la surface
de différentes cellules notamment gliales, lympho-
cytes B ou cellules épithéliales du rein (7).
Signes cliniques
Ces signes sont très variés (8) et peu spécifiques.
Pour cette raison, l’apparition de signes neurolo-
giques dans un contexte à risque de LEMP doit faire
évoquer ce diagnostic. Les troubles cognitifs et des
modifications de la personnalité sont fréquents.
Sur le plan cognitif, des troubles du langage, des
difficultés mnésiques ou un syndrome frontal sont
observés. Des troubles du champ visuel, notam-
ment sous la forme d’une hémianopsie latérale
homonyme, ne sont pas rares, des crises convul-
sives sont plus rares. Sur le plan moteur, ce sera
l’apparition d’une hémiparésie, d’un syndrome
cérébelleux ou d’une dysarthrie qui révélera la
maladie. Un syndrome médullaire isolé est excep-
tionnel (9).
Comment poser le diagnostic ?
À la moindre suspicion, une imagerie par réso-
nance magnétique (IRM) encéphalique doit être
réalisée en urgence. Les séquences T2 FLAIR
sont les plus sensibles pour détecter les lésions.
Celles-ci sont souvent volumineuses, unilobaires
ou beaucoup plus diffuses, sans effet de masse
et généralement non ou peu rehaussées par le
gadolinium. Elles occupent la substance blanche,
parfois dessinant les fibres en U, envahissant
la capsule interne et le corps calleux, et, dans
certains cas, infiltrant les structures profondes
comme le thalamus ou le noyau lenticulaire. Leurs
contours sont parfois mal limités. Si les images
sont caractéristiques ou si le contexte clinique
oriente malgré tout vers une infection opportu-
niste du SNC, une ponction lombaire (PL) doit être
réalisée en y incluant une PCR (Polymerase Chain
Reaction) quantitative ultrasensible. Au besoin,
l’IRM et la PL doivent être répétées. La positivité
permet de poser le diagnostic.
Traitement
La restauration immunitaire est le seul traitement
efficace. La mortalité est élevée et varie de 20 à
100 % selon les contextes cliniques. De nombreux
traitements sont proposés, dont le cidofovir (10), la
cytarabine (11), ou encore l’interleukine 2 ou plus
récemment la méfloquine et la mirtazapine. Si des
résultats positifs ont été rapportés, il ne s’agit bien
souvent que de cas cliniques isolés et aucune conclu-
sion ne peut être faite quant à leur réel intérêt.
La LEMP secondaire
aux biothérapies
Un regain d’intérêt est apparu avec l’apparition des
cas de LEMP secondaire à l’utilisation des biothé-
rapies, et notamment d’anticorps monoclonaux.
Ces cas rendent plus complexe l’utilisation de ces
produits et plus difficile l’appréciation de leur rapport
bénéfice-risque. Les cas les plus représentatifs l’ont
été avec l’efalizumab, le rituximab et le natalizumab.
Efalizumab
L’efalizumab a été retiré du marché en mai 2009
sur décision du promoteur après notification de la
Food and Drug Administration (FDA) et demande
de suspension par l’European Medicinal Evaluation
Agency (EMEA) [12]. Cet anticorps monoclonal
était dirigé contre le CD11a, la sous-unité α de LFA1
(figure 1). En l’absence de l’efalizumab, LFA1 se lie
à ICAM1, étape importante pour la pénétration
tissulaire des lymphocytes activés. Les résultats des
études avaient conduit à une autorisation de mise
sur le marché (AMM) aux États-Unis en 2003 et en
Europe en 2004 pour certaines formes de psoriasis.
Au moment du retrait, 4 cas de LEMP − 3 certains
et 1 probable −, ont été observés. Sur les 3 cas bien
documentés, 2 patients sont décédés. Ces patients
avaient été traités durant plus de 3 ans en mono-
thérapie et aucun n’avait reçu en même temps d’im-
munosuppresseurs. Au-delà de 3 ans de traitement,
le risque de LEMP pouvait être établi à 1 cas sur
400 patients traités.

Inhibiteurs de molécules d’adhésion
Flux sanguin
Sélectines
Tissu cérébral
Lame basale endothéliale
Gaine de myéline Nœud de Ranvier
VCAM-1
VLA-4
LFA-1
ICAM-1
Mucine
Lymphocyte T
Figure 1. Inhibition des molécules d’adhésion VLA-4 et LFA-1 par le natalizumab et l’efa-
lizumab. La présence de ces anticorps empêche les lymphocytes de se lier à leurs ligands
et donc de pénétrer ensuite dans le SNC au travers la barrière hémato-encéphalique.
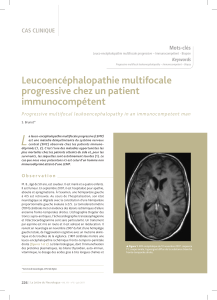
Figure 2. Large lésion bifrontale en hypersignal sur
les séquences T2 FLAIR chez une patiente traitée par
rituximab pour une maladie de Waldenström.
La Lettre de l’Infectiologue • Tome XXVI - n° 3 - mai-juin 2011 | 103
MISE AU POINT
Rituximab
Cet anticorps monoclonal chimérique est dirigé
contre CD20 ; il cible donc l’activité des lymphocytes
de la lignée B. Les premières AMM ont été obtenues
en 1997 aux États-Unis et en 1998 en Europe. Il est
utilisé en onco-hématologie, et notamment dans les
lymphomes malins non hodgkiniens, ou encore dans
certaines formes sévères d’anémies hémolytiques
auto-immunes, de purpuras thrombopéniques ou de
dysglobulinémies (figure 2), et dans des pathologies
dysimmunitaires, le plus souvent en combinaison,
comme c’est le cas dans le lupus systémique ou la
polyarthrite rhumatoïde où il est associé au métho-
trexate. Son utilisation dans la sclérose en plaques
(SEP) est très rare et n’est pas validée. Dans les indi-
cations validées, en raison du risque iatrogène, il
bénéficie d’un plan de gestion du risque. La fréquence
des LEMP sous rituximab n’est pas précisée. Dans
le lupus systémique, le risque a été évalué à 1 cas
sur 4 000 patients traités. La mortalité semble très
élevée, établie à 89 % dans une série de 57 cas (13).
Elle semble plus élevée, proche de 100 %, lorsque le
diagnostic est porté dans les 3 mois qui suivent la
dernière perfusion de rituximab et lorsque le patient a
bénéficié, préalablement ou en combinaison, d’autres
traitements immunosuppresseurs. Parmi les méca-
nismes potentiellement en cause dans les LEMP sous
rituximab, outre la déplétion durable des lympho-
cytes B, il est évoqué l’expansion secondaire des
lymphocytes pré-B, porteurs de virus JC, et l’impact
possible du rituximab sur la lignée lymphocytaire T.
Natalizumab
La survenue de cas de LEMP sous natalizumab a
renouvelé l’attention portée à cette pathologie
opportuniste. Ces cas ont, par ailleurs, grande-
ment influencé notre façon d’apprécier le rapport
bénéfice-risque dans la prise en charge de patients
atteints de SEP. Le natalizumab est un anticorps IgG4
humanisé dirigé contre la sous-unité α de VLA-4
(figure 1). Il inhibe la liaison entre VLA-4 exprimé
sur la membrane lymphocytaire et VCAM-1 exprimé
à la surface de la cellule endothéliale de la paroi
vasculaire, diminuant de façon efficace la pénétration
lymphocytaire dans le SNC. Il a reçu une AMM dans
des formes rémittentes de SEP aux États-Unis et en
Europe, et dans des formes sévères de maladie de
Crohn (MC) aux États-Unis. Dans la SEP, l’indication
est plus restrictive en Europe, limitée aux formes
qualifiées de très actives d’emblée ou ne répondant
pas à un traitement bien conduit par interféron β. Les
2 premiers cas ont été observés au cours de l’étude
SENTINEL, chez des patients recevant un traitement
associant natalizumab et interféron β (14, 15). Un
troisième cas est survenu chez un patient atteint
de MC traitée par mono thérapie. En février 2005,
le promoteur Biogen Idec a préféré suspendre la
commercialisation du natalizumab afin de procéder
à une réévaluation du rapport bénéfice-risque chez
les patients traités par cette molécule dans les diffé-
rentes études. La reprise de la commercialisation
s’est faite, selon les pays, en 2006 et en 2007 avec
un plan de gestion du risque et un encouragement à
inclure les patients dans des cohortes et des registres.

3,0
2,5
2,0
1,5
1,0
0,5
0,0 0,20
1,00
2,80
1,50
1,01
1,23
0,07
0,01
0,00
0,66
0,44
0,28
1,27
1,68
2,18
1,65
1,03
0,60
Essai
clinique
Post-
marketing
1-12
Infusions
13-24
Infusions
25-26
Infusions
37-48
Infusions
Incidence pour 1 000 patients
Figure 3. Incidence globale des LEMP sous natalizumab dans les études cliniques et selon
le nombre de perfusions (moyenne et IC95) [16].
Figure 4. IRM en séquence
FLAIR d’une LEMP sous
natalizumab. Combinaison
des images de SEP et d’une
image caractéristique d’une
LEMP, dans la région pariéto-
occipitale.
104 | La Lettre de l’Infectiologue • Tome XXVI - n° 3 - mai-juin 2011
Leucoencéphalopathie multifocale progressive après biothérapies
MISE AU POINT
◆Nombre de cas de LEMP sous natalizumab
Depuis la réintroduction du natalizumab, 102 cas
ont été déclarés sur une population exposée de
près de 80 000 patients. Dans cette population,
plus de 32 000 patients sont ou ont été traités
durant au moins de 2 ans et près de 15 000, durant
au moins 3 ans. Le risque global est de 1,23 pour
1 000 patients (figure 3) [16], résultat proche de
celui qui était observé dans les suites des études
cliniques (1/1 000) [17].
◆Caractéristiques des cas de LEMP
sous natalizumab
Pour ces cas survenant chez des patients atteints de
SEP, la moindre modification clinique, qu’elle soit
clinique ou encore plus psychocomportementale, doit
faire avant tout évoquer une probable LEMP avant
d’envisager la possibilité d’une poussée. La réalisa-
tion d’une IRM encéphalique en urgence s’impose au
moindre doute. Les séquences T2 FLAIR sont les plus
sensibles pour détecter les lésions de LEMP et doivent
être comparées aux clichés réalisés antérieurement.
Sur le plan clinique, les manifestations les plus
fréquentes sont cognitives ou comportementales ;
elles sont résumées dans le tableau I. Dès qu’une
LEMP est suspectée, le traitement doit être inter-
rompu et les investigations initiées. Si l’IRM est évoca-
trice (figure 4) ou simplement suspecte (tableau II),
il faut réaliser une analyse du liquide cérébro-spinal
comprenant une PCR quantitative pour le virus JC,
en s’assurant que le laboratoire dispose d’une tech-
nique ultrasensible. En effet, le nombre de copies
est souvent faible, parfois inférieur à 100/ml. Si, à
l’issue de ces examens, le doute persiste, ils doivent
être renouvelés. La mortalité des patients atteints de
LEMP sous natalizumab est de l’ordre de 20 %, soit un
pourcentage bien moindre que dans d’autres circons-
tances (18). Une prise en charge tardive, des lésions
plus étendues à l’IRM et un âge plus avancé sont
associés à un risque plus élevé d’évolution fatale (18).
Le nombre de cas de LEMP sous natalizumab a
permis de dégager des facteurs de risque qui sont
au nombre de trois : une durée de traitement de
plus de 2 ans, un traitement immunosuppresseur
antérieur (quelle que soit l’ancienneté) et surtout la
détection dans le sérum d’anticorps dirigés contre le
virus JC. En effet, dans tous les cas où cela a pu être
analysé, les patients qui ont déclenché une LEMP
sous natalizumab avaient, avant le début clinique
de celle-ci, des anticorps antivirus JC. À l’opposé,
les patients négatifs pour le test (environ 45 % des
patients) sont a priori protégés contre ce risque.
Il est donc désormais possible d’établir une stra-
Tableau I. Comparaison sémiologique d’une poussée de sclérose en plaques (SEP) et de la
leucoencéphalopathie multifocale progressive (LEMP).
SEP LEMP
Début Aigu Subaigu
Évolution Quelques heures ou jours
Stabilisation secondaire
Le plus souvent amélioration
spontanée
Plusieurs semaines
Aggravation progressive
Présentations cliniques
les plus fréquentes
Névrite optique
Troubles sensitifs subjectifs
Myélopathie partielle
Diplopie
Paraparésie
Modifications du comportement
Changement de personnalité
Aphasie
Épilepsie
Altérations du champ visuel
rétrochiasmatiques
Ataxie cérébelleuse
Hémiparésie

La Lettre de l’Infectiologue • Tome XXVI - n° 3 - mai-juin 2011 | 105
MISE AU POINT
tification du risque, important pour la discussion
avec nos patients (tableau III) [19]. La vérification
de la fiabilité du test ELISA pour la détection de ces
anticorps est en cours d’évaluation.
◆Prise en charge
Si la suspicion est importante, il est conseillé, sans
attendre le résultat de la PCR, de réaliser des échanges
plasmatiques (EP), susceptibles de restaurer plus rapi-
dement le système immunitaire au niveau du SNC. Des
approches médicamenteuses sont parfois proposées
(cf. supra). De façon quasi constante, il est observé un
syndrome inflammatoire de reconstitution immuni-
taire (IRIS) 2 à 10 semaines après les EP, possiblement
un peu plus tard sans EP. Ce syndrome peut aggraver
transitoirement et parfois de façon importante le
tableau clinique. À l’IRM, l’IRIS se manifeste par une
extension des lésions accompagnées d’un œdème et
de prises de gadolinium hétérogènes. Une corticothé-
rapie initialement à fortes doses doit être proposée en
cas d’IRIS. L’arrêt du natalizumab s’accompagne par
ailleurs fréquemment d’une reprise évolutive de la
maladie dans les mois qui suivent l’arrêt du traitement.
Les médecins sont confrontés à un nouveau challenge
dans ces pathologies, dont la SEP : l’évaluation néces-
saire du rapport bénéfice-risque avec ces biothérapies.
La stratification du risque sous natalizumab est une
première approche de médecine personnalisée. ■
Tableau II. Comparaison des lésions IRM de SEP et de LEMP.
SEP LEMP
Localisation Focale le plus souvent
périventriculaire, sous-corticale,
parfois corticale,
sous-tentorielle de petite taille,
corps calleux de petites tailles
ou multiples
Moelle épinière
Plus diffuse, parfois extensive
plurilobée, substance blanche
profonde ou sous-corticale,
fibres en U, substance grise
profonde, sous-tentorielle
en plage
Limites Bien définies Mal définies, contours flous
Rehaussement
par le gadolinium
Souvent prise de contraste en
anneau ou pleine
Possible +++ mais hétérogène
Extension Stabilisation rapide puis légère
régression
Extension progressive,
parfois controlatérale
Infiltration profonde
Tableau III. Stratification du risque en fonction de la sérologie antivirus JC, de la prise antérieure
d’immunosuppresseurs et de la durée de traitement (19).
Statut antivirus JC
Négatif Positif
Traitement antérieur par immunosuppresseurs
Non Oui
Exposition
au natalizumab
0-2 ans ≤ 0,11/1 000
(IC95 : 0-0,59)
0,35/1000
(IC95 : 0,19-0,60)
1,2/1000
(IC95 : 0,58-2,2)
> 2 ans 2,8/1 000
(IC95 : 2,0-3,8)
8,1/1 000
(IC95 : 5,4-11,6)
1. Astrom KE, Mancall EL, Richardson EP Jr. Progressive
multifocal leuko-encephalopathy; a hitherto unrecognized
complication of chronic lymphatic leukaemia and Hodgkin’s
disease. Brain 1958;81:93-111.
2. Hallervorden J. Eigennartige und nicht rubizierbare
Prozesse. In: Bumke O, ed. Handbuch der Geiteskranhe-
tinen. Berlin: Springer, 1930:1063-107.
3. Gonzalez H, Bolgert F, Camporo P, Leblond V. Progressive
multifocal leukoencephalitis (PML) in three patients treated
with standard-dose fludarabine (FAMP). Hematol Cell Ther
1999;41:183-6.
4. Mackowiak-Cordoliani MA, De Seze J, Stojkovic T, Ferriby D,
Ingrand D, Vermersch P. Sarcoïdose et leucoencéphalopa-
thie multifocale progressive. Rev Neurol 2001;157:547-50.
5. Padgett BL, Walker DL. Prevalence of antibodies in human
sera against JC virus, an isolate from a case of progressive
multifocal leukoencephalopathy. J Infect Dis 1973;127:467-
70.
6. Monaco MC, Atwood WJ, Gravell M, Tornatore CS, Major EO.
JC virus infection of hematopoietic progenitor cells, primary
B lymphocytes, and tonsillar stromal cells: implications for
viral latency. J Virol 1996;70:7004-12.
7. Elphick GF, Querbes W, Jordan JA et al. The human polyo-
mavirus, JCV, uses serotonin receptors to infect cells. Science
2004;306:1380-3.
8. Weber T. Progressive multifocal leukoencephalopathy.
Neurol Clin 2008;26:833-54.
9. Mathew RM, Murmane M. MRI in PML : bilateral medullary
lesions. Neurology 2004;63:2380.
10. De Luca A, Fantoni M, Tartaglione T, Antinori A.
Response to cidofovir after failure of antiretroviral
therapy alone in AIDS-associated progressive multifocal
leukoencephalopathy. Neurology 1999;52:891-2.
11. Aksamit AJ. Treatment of non-AIDS progressive multifocal
leukoencephalopathy with cytosine arabinoside. J Neurovirol
2001;7:386-90.
12. FDA statement on the voluntary withdrawal of raptiva
from the US market. http://www.fda.gov/NewEvents/
Newsroom/PressAnnouncements/2009/ucm149561.htm.
13. Carson KR, Evens AM, Richey EA et al. Progressive
multifocal leukoencephalopathy after rituximab therapy
in HIV-negative patients: a report of 57 cases from the
Research on Adverse Drug Event and Reports project. Blood
2009;113:4834-40.
14. Kleinschmidt-DeMasters BK, Tyler KL. Progressive multi-
focal leukoencephalopathy complicating treatment with
natalizumab and interferon beta-1a for multiple sclerosis.
N Engl J Med 2005;353:369-74.
15. Langer-Gould A, Atlas SW, Green AJ, Bollen AW, Pelletier D.
Progressive multifocal leukoencephalopathy in a patient
treated with natalizumab. N Engl J Med 2005;353:375-81.
16. Gold R, Foley J, Vermersch P et al. Overview of clinical
outcomes in cases of natalizumab-associated progres-
sive multifocal leukoencephalopathy. Neurology 2011;
76(suppl4):S51.002.
17. Yousry TA, Major EO, Ryschkewitsch C et al. Evaluation of
patients treated with natalizumab for progressive multifocal
leukoencephalopathy. N Engl J Med 2006;354:924-33.
18. Vermersch P, Kappos L, Gold R et al. Clinical outcomes
of natalizumab-associated progressive multifocal
leukoencephalopathy. Neurology 2011, May 11. Epub
ahead of print.
19. Sandrock A, Hotermans C, Richman S et al. Risk stra-
tification for progressive mulifocal leukoencephalopathy
(PML) in MS patients: role of prior immunosuppressant use,
natalizumab-treatment duration, and JCV antibody status.
Neurology 2011;76(suppl4):P03248.
Références bibliographiques
Conflit d’intérêts. Patrick Vermersch déclare avoir un conflit
d’intérêts avec Biogen Idec (honoraires, frais de congrès, aide
à la recherche).
1
/
5
100%