L Leucoencéphalopathie multifocale progressive chez un patient immunocompétent

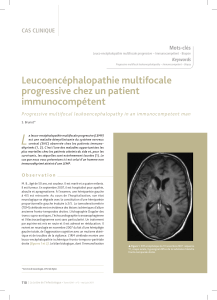
▲ Figure 1. IRM encéphalique du 10 novembre 2007 : séquence
T1, coupe axiale, hyposignal diffus de la substance blanche
fronto-temporale droite.
226 | La Lettre du Neurologue • Vol. XV - n° 6 - juin 2011
CAS CLINIQUE
Mots-clés
Leuco-encéphalopathie multifocale progressive – Immunocompétent - Biopsie
Keywords
Progressive multifocal leukoencephalopathy – Immunocompetent – Biopsy
Leucoencéphalopathie multifocale
progressive chez un patient
immunocompétent
Progressive multifocal leukoencephalopathy in an immunocompetent man
S. Brunot*
* Service de neurologie, CHU de Dijon.
L
a leuco-encéphalopathie multifocale progressive (LEMP)
est une maladie démyélinisante du système nerveux
central (SNC) observée chez les patients immuno-
déprimés (1, 2). C’est l’une des maladies opportunistes les
plus mortelles chez les patients atteints du sida et, pour les
survivants, les séquelles sont extrêmement lourdes (1). Le
cas que nous vous présentons ici est celui d’un homme non
immunodéprimé atteint d’une LEMP.
Observation
M. B., âgé de 50 ans, est soudeur. Il est marié et a quatre enfants.
Il est fumeur. En septembre 2007, il est hospitalisé pour apathie,
aboulie et apragmatisme. À l’examen, une hémiparésie gauche
à 4/5 est retrouvée. Au cours de l’hospitalisation, son état
neurologique se dégrade avec la constitution d’une hémiparésie
proportionnelle gauche évaluée à 2/5. La tomodensitométrie
(TDM) cérébrale met en évidence des lésions ischémiques d’allure
ancienne fronto-temporales droites. L’échographie Doppler des
troncs supra-aortiques, l’échocardiographie transœsophagienne
et l’électrocardiogramme sont sans particularité. Un traitement
par aspirine est mis en route et il est adressé en rééducation. Il
revient en neurologie en novembre 2007 du fait d’une hémiplégie
gauche totale, de l’aggravation cognitive avec un mutisme akiné-
tique et de troubles de la vigilance. L’IRM cérébrale montre une
leuco-encéphalopathie ischémique fronto-temporo-pariétale
droite (figures 1 et 2). Le bilan biologique, dont l’immunoxation
des protéines plasmatiques, les bilans thyroïdien, auto-immun,
vitaminique, le dosage des acides gras à très longues chaînes et

▲ Figure 2. IRM encéphalique du 10 novembre 2007 : séquence
T2, coupe axiale, atteinte de la substance blanche fronto-tempo-
rale droite.
▲ Figure 3. IRM encéphalique du 8 décembre 2007 : séquence
T1, atteinte de la substance blanche et des fibres en U au niveau
de l’hémisphère droit.
La Lettre du Neurologue • Vol. XV - n° 6 - juin 2011 | 227
CAS CLINIQUE
celui de l’enzyme de conversion de l’angiotensine sont normaux.
Les anticorps antineuronaux sont négatifs. Les sérologies des hépa-
tites B et C, VIH-1 et -2, CMV, EBV, HTLV-1 et -2, Lyme, légion-
nelle, Whipple, mycoplasme, Chlamydiae, syphilis sont négatives.
La ponction lombaire n’est pas inammatoire. Les PCR herpès, CMV
et JC40 sont négatives dans le liquide céphalorachidien (LCR), de
même que la recherche de la protéine 14-3-3. La biopsie des glandes
salivaires accessoires est sans particularité. Le bacille de Koch n’est
retrouvé ni dans les sécrétions bronchiques ni dans le LCR. L’arté-
riographie cérébrale est sans anomalie. Le tableau neurologique du
patient s’aggrave avec une atteinte de la sixième paire crânienne
gauche et une mydriase réactive. Des traitements d’épreuve sont
entrepris : augmentation de la dose d’antiagrégant plaquettaire,
introduction d’antibiotiques à large spectre et corticothérapie.
La biopsie cérébrale frontale droite réalisée à la mi-décembre met
en évidence une leuco-encéphalopathie démyélinisante, de type
infectieux. L’hybridation in situ conrmera le diagnostic de LEMP
en février 2008. L’IRM cérébrale de contrôle en décembre évoque
un aspect de LEMP devant l’atteinte des bres en U, le caractère
multifocal en hyposignal T1 et en hypersignal T2 (figures 3 et 4).
M. B décède le 4 janvier 2008 après deux jours de coma. L’autopsie
montre une lésion massive de démyélinisation de la substance
blanche dont l’aspect histologique est en accord avec une LEMP,
atteignant massivement le côté droit et s’étendant focalement à
l’hémisphère gauche.
Discussion
La LEMP est une maladie rare entraînant une démyélinisation du
SNC. Elle est due au virus JC et affecte surtout les sujets immuno-
déprimés (1, 3). L’incidence de cette pathologie a été multipliée
par 50 depuis la n des années 1970, à la faveur de l’émergence du
VIH (3). Près de 90 % des adultes sont porteurs de ce virus, 30 %
l’excrètent dans leurs urines (2). Il n’engendre des symptômes
qu’en cas d’immunodépression, et le plus souvent chez des sujets
de 50 à 70 ans (4). Moins de 1 % des cas ont été rapportés chez
des patients n’ayant pas de problème d’immunodépression (5).
Récemment, la LEMP a fait l’objet de nombreuses publications
comme effet indésirable possible du traitement par natalizumab
dans la sclérose en plaques (SEP).
L’évolution clinique est rapide et la médiane de survie varie de
trois à six mois selon les études (5, 6). Certains patients peuvent
survivre plusieurs années, mais au prix de lourdes séquelles neuro-
logiques (1).
Chez les patients immunodéprimés de façon chronique, le début
est subaigu et les décits sont graves d’emblée (1, 2). Les symp-
tômes les plus fréquents sont un décit moteur et des troubles
cognitifs (50 % des cas) [5]. Les autres signes sont des troubles
aphasiques, de l’équilibre, visuels (altération du champ visuel ou
paralysie oculomotrice), sensitifs, ainsi que des céphalées (15 % des
cas). Les crises d’épilepsie surviennent chez 10 % des patients (5).
Certains examens complémentaires peuvent aider au diagnostic.
Le scanner cérébral met en évidence des lésions hypodenses au
niveau de la substance blanche. Il n’y a pas d’effet de masse ni
de prise de contraste (5). L’IRM encéphalique montre des lésions

▲ Figure 4.IRM encéphalique du 8 décembre 2007 : séquence
T2 TSE, coupe axiale.
228 | La Lettre du Neurologue • Vol. XV - n° 6 - juin 2011
CAS CLINIQUE
multiples, limitées à la substance blanche, sous-corticales et ne
respectant pas les bres arquées juxta-corticales, en hypersignal
sur les séquences T2, et un rehaussement typique en périphérie
dans 5 à 10 % des cas. Les centres semi-ovales et les lobes frontaux,
pariétaux et occipitaux sont les plus fréquemment touchés (3).
La ponction lombaire est très importante, surtout dans l’élimi-
nation de diagnostics différentiels (5). En général, il y a moins de
1. Koralnik IJ. New insights into progressive multifocal
leukoencephalopathy. Curr Opin Neurol 2004;17:365-70.
2. Boren EJ, Cheema GS, Naguwa SM, Ansari AA, Gers-
hwin ME. The emergence of progressive multifocal
leukoencephalopathy (PML) in rheumatic diseases.
J Autommun 2008;30:90-8.
3. Pelosini M, Focosi D, Rita F et al. Progressive multi-
focal leukoencephalopathy: report of three cases in HIV-
negative hematological patients and review of literature.
Ann Hematol 2008;87:405-12.
4. Norkin LC. Papovaviral persistent infections. Microbiol
Rev 1982;46:384-425.
5. Berger JR. Progressive multifocal leukoencephalopathy.
Curr Neurol Neurosci Rep 2007;7:461-9.
6. Cinque P, Koralnik IJ, Clifford DB. The evolving face
of human immunodeficiency virus-related progres-
sive multifocal leukoencephalopathy: defining a
consensus terminology. J Neurovirol 2003;9(suppl. 1):
88-92.
7. Bossolasco S, Calori G, Moretti F et al. Prognostic
significance of JC virus DNA levels in cerebrospinal
fluid of patients with HIV-associated progressive multi-
focal leukoencephalopathy. Clin Infect Dis 2005;40:
738-44.
Références bibliographiques
20 cellules par mm
3
(entre 2 et 8). Une protéinorachie importante
(supérieure à 2 g/l) est retrouvée dans plus de la moitié des cas.
L’hypoglycorachie est observée chez moins de 15 % des patients.
Mais l’essentiel est la recherche du virus par la technique de
PCR, qui a une grande spécicité (96 à 100 %) et une sensibilité
moyenne (50 à 75 %) [3]. Un taux élevé d’ADN du virus JC retrouvé
par PCR dans le LCR est un facteur de mauvais pronostic pour la
survie du patient (7). Cette analyse est nettement moins invasive
que l’étude anatomopathologique qui reste, cependant, l’examen
de référence. Sa sensibilité varie de 64 à 96 % et sa spécicité
est de 100 % (6). Il existe une triade caractéristique pour décrire
l’histologie de cette maladie : multiples foyers de démyélinisation,
bordés par des oligodendrocytes ayant un noyau volumineux et
des inclusions basophiles et par des astrocytes inhabituels, de
grande taille, au noyau hyperchromatique (3). La PCR du virus
sur les tissus biopsiés conrme le diagnostic (3).
Le diagnostic est établi grâce à un faisceau d’arguments cliniques,
radiologiques et biologiques (PCR positive dans le LCR) [2].
Des critères diagnostiques ont été établis récemment (6). Il s’agit
soit d’une LEMP “histologiquement conrmée” (détection de
l’ADN viral par PCR sur les pièces de biopsie), soit d’une LEMP
“biologiquement conrmée” (détection de l’ADN viral par PCR
dans le LCR), ou bien d’une LEMP “possible” (aspects cliniques
et radiologiques compatibles malgré une PCR négative).
Les diagnostics différentiels sont peu nombreux : SEP, leuco-
encéphalopathies secondaires aux traitements immunosuppres-
seurs, aux chimiothérapies et à d’autres infections (herpès virus,
cryptocoque, aspergillus) du SNC.
Il n’y a pas de traitement spécique. En cas de LEMP développée
dans le cadre d’une infection par le VIH, le traitement par anti-
rétroviraux diminue l’immunosuppression et donne d’assez bons
résultats (3).
La pertinence de notre observation repose sur deux faits :
d’une part, il peut exister des cas de LEMP chez des patients
non immuno déprimés, et d’autre part, la biopsie cérébrale est
nécessaire pour établir le diagnostic, dans la mesure où la PCR
du LCR peut être négative. ■
1
/
3
100%