évaluation des repercussions oesophagiennes procedurales lors d

ÉVALUATION DES REPERCUSSIONS
OESOPHAGIENNES PROCEDURALES
LORS D’ABLATION PAR
RADIOFREQUENCE D’ARYTHMIE PAR
FIBRILLATION ATRIALE
S. TISSIER (1) , M. ANDRONACHE (2) , C. BARBARY (1),
V. LAURENT (2), S. BEOT (1), D. REGENT (1)
- CHU NANCY - Brabois - 2006 -
-Département d’imagerie médicale (1) et de cardiologie (2) -

Introduction
Les procédures électrophysiologiques ablatives endocavitaires
prennent de plus en plus de place dans l’arsenal thérapeutique des
troubles du rythme et de la conduction cardiaque.
Les ablations par radiofréquence (RF) endocavitaire reposent sur
l’interruption électrique de voies de conduction pathologiques et/ou
la destruction de foyers déclencheurs spécifiques des troubles
traités.
Le traitement de la fibrillation atriale (FA) par cette méthode ablative
endocavitaire par voie percutanée est de plus en plus utilisé. son
principe consiste à détruire les cellules déclenchantes en utilisant
l’énergie délivrée par radiofréquence.

Introduction
Cette technique récente expose à certaines complications parmi
lesquelles les sténoses et occlusions veineuses pulmonaires.
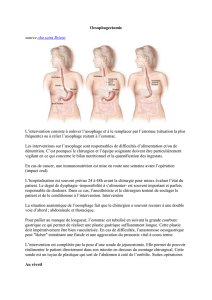
En raison de la proximité anatomique de la face postérieure de
l’atrium gauche avec le mur antérieur de l’œsophage, ce dernier
peut subir un traumatisme thermique lors de la procédure.
Dans certain cas cet effet collatéral va conduire à une complication
redoutable : la fistule oeso-atriale.
La connaissance des relations anatomiques entre l’atrium gauche,
les veines pulmonaires et la face antérieure de l’œsophage devient
primordiale avant la procédure et permet au cardiologue
électrophysiologiste interventionnel de réduire le risque de lésion
thermique oesophagienne et donc la chance de formation d’un trajet
fistuleux.

Table des matières
Généralités
Principes de traitement de la FA par RF
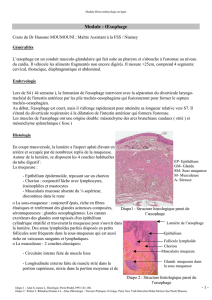
Anatomie de l’oesophage
La fistule oeso-atriale
Étude anatomique pré-procédurale par scanner cardiaque
Matériels et méthodes
Anatomie atriale gauche et des veines pulmonaires
Relations entre l’œsophage, l’atrium gauche et les veines pulmonaires
Discussion
Étude anatomique post-procédurale par scanner cardiaque
Complications
Contrôle de la position oesophagienne
Discussion
Conséquences pratiques : méthode nancéenne
Conclusion

Principes de traitement de la FA par RF
Généralités
L’ablation par radiofréquence (RF) de la FA est la procédure la plus couramment
réalisée dans notre centre. Son principe repose sur la destruction de foyers
déclencheurs ectopiques de l’arythmie siégeant à proximité des ostia des
veines pulmonaires (VP) [ablation spécifique] ou des voies de conduction peri-
ostiales et atriales par des lignes ablatives [ablation-deconnexion] notamment le
long du mur atrial posterieur.
Cartographie post-procédure et visualisation des
lignes d’ablation-deconnexion : peri-ostiales, inter-
ostiale supérieure et mitro-pulmonaire inférieure
KT Carto
KT abation
Ablation spécifique de chaque foyer
déclencheur ostial détecté par cartographie
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
 45
45
 46
46
1
/
46
100%