Diabète : “tu me fends le cœur” I XX

Informations
Informations
La Lettre du Cardiologue - n° 404 - avril 2007
10
Diabète : “tu me fends le cœur”
XXe Journée de l’APIC
(Samedi 25 novembre 2006 [2e partie])
N. Laredj*
* Institut du Cœur, groupe hospitalier de la Pitié-Salpêtrière, Paris.
LA REVASCULARISATION DU DIABÉTIQUE
P. Henry (Paris)
Il existe actuellement entre 800 000 et 1 500 000 diabétiques
méconnus en France, et près de 50 % des patients non diabé-
tiques admis en soins intensifs cardiologiques sont en réalité
prédiabétiques. Il est également important de rechercher
une ischémie silencieuse chez le diabétique, car elle est plus
fréquente, avec une prédominance de lésions tritronculaires
sévères, de mauvais pronostic. Le dépistage de l’ischémie silen-
cieuse doit être réalisé chez les patients diabétiques qui ont des
facteurs de risque cardiovasculaire associés, qui présentent des
symptômes, même frustes, une autre atteinte vasculaire ou
encore une protéinurie. L’ancienneté du diabète ne semble pas
être un facteur déterminant dans la recherche d’une ischémie ;
elle permet essentiellement de préciser l’importance de la sévé-
rité des complications du diabète, en particulier des lésions de
microangiopathie.
Le risque de resténose avec les stents nus
Les facteurs prédictifs de resténose coronaire sont essentielle-
ment la taille de l’artère, la longueur de la lésion et la présence
ou non d’un diabète. Dans de nombreuses études telles que
RAVEL et SIRIUS, dans les sous-groupes de diabétiques, le
pourcentage de resténose est signifi cativement plus élevé chez
les patients qui ont un stent nu que chez ceux ayant un stent
actif (respectivement 41 % versus 0 % dans l’étude RAVEL à six
mois, p = 0,002 ; 48 % versus 8 % dans l’étude SIRIUS, p < 0,001).
Dans le groupe stent actif (CYPHER), le taux de revascularisation
était signifi cativement plus faible à deux ans, ainsi que le risque
d’événements cardiovasculaires majeurs défi nis par la mortalité
toute cause, l’infarctus et la revascularisation à deux ans.
Dans la méta-analyse des études TAXUS II, IV, V et VI – stents
actifs au paclitaxel –, qui a étudié le sous-groupe de diabétiques,
le taux de resténose était signifi cativement plus élevé chez les
patients avec un stent nu que chez ceux qui avaient un stent
actif, quel que soit leur traitement antidiabétique (traitement
oral ou insulinothérapie), de même que le taux de revascula-
risation à neuf mois.
Le risque de thrombose de stent
Il existe chez le diabétique, comparé aux autres patients, un
risque accru de rupture de plaque et de thrombose, en rapport
avec une “hyperagrégation plaquettaire” encore plus marquée,
une augmentation des récepteurs plaquettaires à la glycopro-
téine IIb/IIIa, ainsi qu’une sécrétion plus importante de facteurs
prothrombotiques tels que le fi brinogène, le facteur Willebrand,
les facteurs VII et VIII, PAI-1 ; d’où l’intérêt d’un blocage complet
ou du moins effi cace de l’agrégation plaquettaire. À cet eff et,
les anti-GPIIb/IIIa jouent un rôle important lors d’une procé-
dure d’angioplastie, comme le montrent les études EPILOG et
EPISTENT. La mortalité à un an était signifi cativement plus
faible chez les patients diabétiques ayant bénéfi cié d’abciximab
per procédure que dans le groupe contrôle.
Le risque de thrombose de stent est d’autant plus présent que
les lésions coronaires sont complexes, plus longues, siégeant sur
de petits vaisseaux ou sur des bifurcations, fréquemment sur
des stents longs. Ce risque est également proportionnel à l’âge
des patients et à la présence de comorbidités associées.
La revascularisation chirurgicale chez le diabétique
Si une indication de revascularisation chirurgicale est retenue,
il est actuellement recommandé de privilégier un pontage tout
artériel, par les artères mammaires internes, en particulier chez
le diabétique. La mortalité intra-hospitalière après un pontage
aortocoronarien reste supérieure à celle de l’angioplastie coro-
naire, et elle est d’autant plus élevée que le patient présente des
comorbidités associées.
Quelle revascularisation chez le diabétique ?
Dans l’essai ARTS II, réalisé chez 607 patients bénéfi ciant d’un
stent actif au sirolimus (26 % de diabétiques), et qui a inclus les
données de son prédécesseur ARTS I (comparant le pontage
aortocoronarien et les stents nus chez 1 202 patients, dont 18 %
de diabétiques ayant des lésions coronaires tritronculaires), les
résultats à un an n’ont pas démontré de diff érence signifi cative
entre les stents actifs et la revascularisation chirurgicale, et
ce concernant la mortalité totale, l’infarctus ou la réinterven-
tion. En revanche, il existait une diff érence nette entre les deux
groupes de stents, en faveur des stents actifs. Dans l’étude BARI,
la mortalité cardiovasculaire à cinq ans est signifi cativement plus
élevée chez les diabétiques qui ont bénéfi cié d’une angioplastie
que dans le groupe chirurgie.
>>>

Informations
Informations
Intestin
Acarbose
Metformine
Sulfonylurées
Glitazones
Glucose
Insuline
Foie
Pancréas
Muscle
+
+
+
––
–
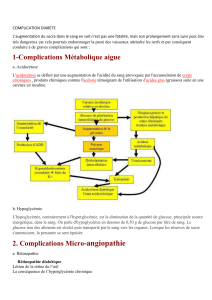
Figure 1. Le site d’action des antidiabétiques oraux.
La Lettre du Cardiologue - n° 404 - avril 2007
12
En pratique, la revascularisation chirurgicale est réservée aux
patients diabétiques qui présentent des lésions coronaires
diff uses, en particulier les diabétiques sous insuline, et seulement
si les artères mammaires internes sont fonctionnelles.
Conclusion
Le diabète étant une maladie chronique, notre objectif
thérapeutique primaire est de stabiliser la progression de la
maladie. Le diabétique peut être assimilé à un tabagique qui
fume deux paquets par jour et qui ne veut pas arrêter, ou à
un patient qui a un taux de LDL-c à 1,90 g/l et qui ne veut
pas prendre de statine. Notre rôle est d’abord de contrôler le
diabète (cible de HbA1c < 7 %) et les autres facteurs de risques
cardiovasculaires, de traiter le syndrome métabolique (HTA,
dyslipidémie, etc.), et de dépister précocement les complica-
tions du diabète.
Les problèmes qui se posent chez les diabétiques sont les
suivants :
– l’HTA est souvent mal contrôlée alors que les objectifs tension-
nels sont plus diffi ciles à atteindre chez les diabétiques ;
– la dyslipidémie est souvent difficile à traiter (types VI et
IIb) ;
– quel est le traitement du HDL-c bas ?
– les traitements antiagrégants plaquettaires doivent-ils être
calqués sur ceux des non-diabétiques en prévention secon-
daire ?
– faut-il traiter la dysfonction endothéliale ?
En pratique, il faudrait en premier lieu équilibrer la glycémie
pendant la revascularisation et utiliser tout l’arsenal théra-
peutique pendant la procédure, puis assurer, dans un second
temps, une prise en charge globale du patient et de ses facteurs
de risque associés : équilibrer le diabète, traiter l’hyperten-
sion artérielle, corriger la dyslipidémie et assurer un suivi
rapproché.
FLASH D’ACTUALITÉ : LES FUTURS TRAITEMENTS
DU DIABÈTE DE TYPE 2
J. Girard (Paris)
Les agents pharmacologiques actuellement disponibles pour
baisser la glycémie chez le diabétique ont des mécanismes d’ac-
tion diff érents (fi gure 1) :
– les sulfonylurées augmentent la sécrétion d’insuline ;
– l’acarbose retarde l’absorption des sucres ;
– les glitazones augmentent principalement le captage muscu-
laire du glucose ;
– la metformine diminue la production hépatique du
glucose ;
– les analogues de l’insuline corrigent la carence en insuline.
La perspective actuelle serait de développer chez le diabétique de
type 2 d’autres agents thérapeutiques, qui agiraient de manière
spécifi que :
– en améliorant la sécrétion d’insuline en réponse au
glucose ;
– en mimant l’action de l’insuline ;
– en l’augmentant (insulinorésistance) ;
– en inhibant la production hépatique de glucose ;
– en induisant la néogenèse et la prolifération, et/ou en dimi-
nuant l’apoptose des cellules β pancréatiques.
Les nouveaux agents thérapeutiques améliorant
la sécrétion d’insuline en réponse au glucose
Les glinides, comme les sulfonylurées, agissent sur la fermeture
du canal K-ATP, mais leur action est plus rapide et de moins
longue durée. Leur intérêt est de mimer la sécrétion rapide
d’insuline lors des repas ; ils restaurent ainsi la phase rapide
d’insulinosécrétion chez le diabétique.
Le glucagon-like peptide-1 (GLP-1) agit via des récepteurs
couplés à la production d’AMP cyclique, à diff érents niveaux :
il potentialise la sécrétion d’insuline en réponse au glucose et
réduit la sécrétion du glucagon ; il induit la néogenèse et la
prolifération des cellules β dans les îlots de Langerhans ; enfi n,
il inhibe la vidange gastrique et la prise alimentaire. L’incon-
vénient principal est sa dégradation rapide dans la circulation
sanguine. L’idéal serait de développer une forme “retard” ou
de mettre au point un inhibiteur de la dipeptidyl peptidase IV,
l’enzyme qui dégrade le GLP-1.
Nouveaux agents agissant par des voies
de signalisation diff érentes de celles de l’insuline
Les activateurs de l’AMP kinase
La contraction musculaire stimule le captage du glucose par le
muscle, par une voie diff érente de celle de l’insuline. Elle met en
jeu une protéine kinase : l’AMP kinase. Deux adipocytokines,
libérées par le tissu adipeux, améliorent l’insulinosensibilité
musculaire en stimulant cette enzyme (fi gure 2).
>>>

Informations
Informations
Leptine Adiponectine Contraction
AMP kinase Kinase Ca ++
AMP kinase AMP kinase-P Stimulation du
transport de glucose
Inhibition de l’oxydation
des acides gras
AICAR
+
+
Figure 2. Les activateurs de l’AMP kinase.
Insulinémie Glycémie
Diabétiques
Diabétiques
Répaglinide
Répaglinide
Répaglinide
Glucose Glucose
Répaglinide
Minutes
(µU/ml) (mg/dl)
0- 60 0 60 120 180 240 360 - 60 0 60 120 180 240 360
25
50
75
100 400
300
200
100
0
Minutes
Figure 3. Rôle des glinides en période postprandiale.
Glycémie (mg/dl)
Diabétiques
Diabétiques + GLP-1
Glucose
GLP-1
- 60 0 60 120 180 240 360
400
300
200
100
0
Minutes
Figure 4. Rôle des GLP-1 dans l’hyperglycémie postprandiale.
La Lettre du Cardiologue - n° 404 - avril 2007
13
Les inhibiteurs de la lipolyse
L’acide nicotinique (Acipimox), comme les glitazones, diminue la
libération des FFA (free fatty acid) par le tissu adipeux, respon-
sable d’une diminution de la néoglucogenèse, d’une augmen-
tation de la sécrétion d’insuline et de l’utilisation du glucose. Il
améliore de ce fait l’insulinosensibilité.
Les inhibiteurs de l’infl ammation
Le salsalate (Disalcid
®
) améliore également l’insulinosensibi-
lité, en bloquant l’IKKβ (inhibiteur du kappa B kinase β qui
diminue le transport du glucose et réduit les eff ets métaboliques
de l’insuline).
Nouveaux agents améliorant la tolérance au glucose
en période postabsorptive
La phase précoce d’insulinosécrétion joue un rôle important
dans l’hyperglycémie postprandiale.
Les glinides, en restaurant la sécrétion précoce d’insuline,
améliorent l’hyperglycémie postprandiale chez le diabétique.
Ils diminuent également la production hépatique de glucose
(fi gure 3).
L’absence de réduction de la production hépatique de glucose
en période postprandiale chez le diabétique est due en partie
à la non-suppression du glucagon. L’inhibition de la sécré-
tion du glucagon par les GLP-1 joue un rôle important dans
l’hyperglycémie postprandiale (fi gure 4).
Nouveaux agents inhibant la production hépatique
de glucose
Ce sont les antagonistes non peptidiques du glucagon, les inhibi-
teurs de la glycogène phosphorylase et les inhibiteurs d’enzymes
de la néoglucogenèse.
Nouveaux agents améliorant la signalisation
insulinique
L-783-281 (extrait d’un champignon tropical) est un activa-
teur non peptidique de l’activité tyrosine kinase du récepteur
de l’insuline, actif par voie orale, et qui a démontré chez les
souris diabétiques une diminution de la glycémie de 50 % en
quatre heures.
Les souris invalidées pour le gène de la tyrosine phosphatase
(1B PTP-1B) ont une sensibilité augmentée à l’insuline et sont
résistantes à l’induction d’une obésité par un régime hyperlipi-
dique. Les inhibiteurs de la PTP-1B auront pour but de diminuer
la glycémie des souris diabétiques. ■
1
/
3
100%