Lire l'article complet

Figure 1. Bronchiolite oblitérante = 0/syndrome de bronchiolite
oblitérante stade 0.
Débit (l/s)
7
6
5
4
3
2
1
0
– 1
– 2
– 30 0,5 1 1,5 2 2,5 3 Volume (l)
= Normal
0
1
2
3
4
5
6
7
8
9
10
Débit/volume Temps (s)
Le Courrier de la Transplantation - Volume VI - n
o 4 - octobre-novembre-décembre 2006
233
Mise
au point
Évérolimus et bronchiolite oblitérante
en transplantation pulmonaire
* Chirurgie cardiovasculaire, hôpital européen Georges-Pompidou, 75015 Paris.
** Service de pharmacologie, hôpital européen Georges-Pompidou, 75015 Paris.
R. Guillemain*, E.M. Billaud*●
La transplantation pulmonaire s’est développée au
cours des dernières décennies. Les premières réussi-
tes dans ce domaine ont été rendues possibles grâce à
la puissance de nouveaux traitements immunosuppresseurs
et aux progrès de la chirurgie thoracique, notamment la
réduction pulmonaire, introduite en France en 1992. Les
succès à court terme, particulièrement au niveau de la pré-
vention et du traitement du rejet aigu, restent cependant
pénalisés par la survenue d’une complication spécique de
la transplantation pulmonaire, la bronchiolite oblitérante
(BO). Elle est en transplantation pulmonaire l’équivalent
de la dysfonction chronique du greffon rénal ou de la mala-
die coronaire du greffon cardiaque, et représente l’expres-
sion du rejet chronique sur les voies respiratoires aérien-
nes. Il s’agit donc de la principale manifestation du rejet
chronique en transplantation pulmonaire, et il n’existe pas
actuellement de traitement pour cette pathologie.
La BO est donc le facteur majeur de réduction du pronostic
de survie (1). Une fois le processus déclenché, on ne peut
qu’assister à la détérioration inéluctable des fonctions
respiratoires, entraînant soit le décès, soit la nécessité d’une
retransplantation dont le taux de survie est alors trois fois plus
faible que lors d’une première transplantation pulmonaire.
La BO peut survenir précocement après la transplantation,
dès le deuxième mois, et son délai médian de survenue est
de 1 à 2 ans. Elle touche jusqu’à 50 à 60 % des patients à
5 ans et contribue à plus de 30 % des décès survenant 3 ans
après la transplantation pulmonaire.transplantation pulmonaire..
Les manifestations cliniques sont dominées par :
La lésion anatomique de BO, qui est une définition
anatomopathologique, consistant en une prolifération bro-
blastique au niveau des bronchioles terminales, évoluant
vers une oblitération des petites voies aériennes. Seule une
conrmation histologique de nature invasive permet d’établir
ce diagnostic, qui n’est pas accessible aux tests de biopsie
transbronchique et qui nécessite une voie chirurgicale. Cet
examen, s’il apporte la certitude diagnostique de BO, ne peut
être répété aisément.
En revanche, la traduction fonctionnelle de la BO sur
les voies aériennes s’appelle “syndrome de bronchiolite
oblitérante” (SBO) ; son diagnostic relève des explorations
fonctionnelles respiratoires (EFR), épreuves non invasives
qui peuvent être facilement renouvelées. Ce diagnostic s’ac-
compagne de la réduction progressive des débits respiratoires
et de signes radiologiques constants au niveau du scanner
effectué en expiration forcée (1).
✓
✓
La dénition et la classication du SBO reposent aujourd’hui
sur l’étude des débits expiratoires distaux DEM 25-75 (débit
expiratoire maximal médian dans la zone 25 à 75 % de la
capacité vitale) et du VEMS (volume expiré maximal par
seconde) [2, 3].
Trois grades ont été initialement dénis par l’ISHLT (International
Society of Heart Lung Transplantation) avec différents niveaux
de gravité établis par rapport à la valeur de référence individuelle
de chaque patient, c’est-à-dire son meilleur score (stade 0). Le
grade 0 correspond à l’absence de SBO et les niveaux 1, 2 et 3 à la
diminution plus ou moins importante du VEMS (respectivement
inférieurs ou égaux à 80 %, 65 % et 50 % de la valeur de
référence). Mais le VEMS explore surtout les voies aériennes
proximales, amenant à des diagnostics tardifs. Il y a 5 ans, la
classication a pris en considération un stade supplémentaire 0-p
(p = possible ou probable) correspondant à une baisse de 20 %
du DEM 25-75 pour un VEMS constant.
En prenant en compte l’imagerie et la courbe débit/volume,
l’illustration de ces différents stades apparaît clairement dans les
exemples ci-joints. La figure 1 correspond à l’absence de BO
et de SBO pour laquelle la courbe débit/volume présente une
allure convexe. Aux premiers stades d’apparition (figure 2),
on décèle une hyperplasie du chorion, se traduisant par un
syndrome obstructif dont l’expression radiologique confère
un aspect caractéristique en verre dépoli au scanner (image
type de vidage hétérogène d’obstruction) et par une concavité
de la courbe volumétrique liée à son incurvation, signant la
baisse des débits expirés. Le SBO se traduit par une difculté
fonctionnelle à vider correctement le poumon en expiration.
Les stades 2 et 3 (figure 3) correspondent à l’apparition d’un
bourgeon charnu intrabronchique, tandis que la courbe débit/
volume accentue sa déformation et que le VEMS est également

Figure 2. Syndrome de bronchiolite oblitérante stade 0-p ou 1.
5
4
3
2
1
0
– 1
– 2
– 3
Hyperplasie du chorion
Verre dépoli
Figure 3. Syndrome de bronchiolite oblitérante stades 2 et 3.
5
4
3
2
1
0
– 1
– 2
– 3
Bourgeon charnu
intrabronchique
Figure 4. Syndrome de bronchiolite oblitérante stade 4.
4
3
2
1
0
– 1
– 2
– 3
– 4
Occlusion bronchique
Raréfaction vasculaire
de la dilatation des bronches
Attention : âge extrapolé = 53
150
Référence
1er janvier 2000
2 4 6 8 10 12 2 4 6 8 10 12 2 4 6 8 10 12
2001 2002 Date (an)
Mois
130
110
90
70
50
30
10
Figure 5. Explorations fonctionnelles
respiratoires. Effondrement des débits
expirés.
Le Courrier de la Transplantation - Volume VI - n
o 4 - octobre-novembre-décembre 2006
234
Mise
au point
atteint. Au stade 4, l’imagerie devient celle d’une occlusion
bronchique, exprimant une raréfaction vasculaire d’aspect
“en arbre mort”, accompagnée d’un effondrement des débits
expirés dont la courbe rejoint l’enveloppe de regroupement
du volume courant caractérisant la dyspnée (figure 4). L’EFR
traduit l’effondrement des débits expirés (figure 5).
En résumé, l’évolution du syndrome de BO est irréversible : l’enjeu
en termes de besoin médical est donc aujourd’hui majeur.
Une notion fondamentale à prendre en compte dans la
prévention de la BO est son caractère multifactoriel. Ainsi,
il est possible d’agir sur les nombreux facteurs de risque (1)
de survenue de la BO, notamment :
Le nombre d’épisodes de rejet aigu, qui a été réduit avec
l’introduction du tacrolimus et l’optimisation du suivi théra-
peutique pharmacologique des immunosuppresseurs.
Les infections à cytomégalovirus (CMV), dont la prévention
a pu être améliorée par des traitements antiviraux disponibles par
voie intraveineuse (ganciclovir), et sous la forme de prodrogue
pour favoriser la biodisponibilité orale (valganciclovir).
✓
✓

45
40
35
30
25
20
15
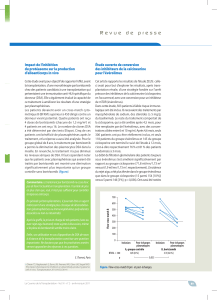
0(n = 112) (n = 101)
p = 0,034
27,7 %
15,8 %
Azathioprine 1-3 mg/kg/j Évérolimus 3 mg/j
Incidence d’une diminution > 15 %
du VEMS (%)
Figure 6. Efcacité de l’évérolimus à 12 mois sur l’incidence de
la diminution > 15 % du volume expiratoire moyen par seconde
(VEMS) versus azathioprine.
35
30
25
20
15
10
5
0
p < 0,001
p < 0,001
p < 0,022
32,1 %
25,9 %
7,9 % 10,9 %
17,9 %
6,9 %
Azathioprine 1-3 mg/kg/j Évérolimus 3 mg/j
Rejet aigu
traité Rejet aigu suspecté
cliniquement
et prouvé par biopsie
Rejet aigu prouvé
par biopsie
grade > 2A
Incidence du rejet aigu (%)
Figure 7. Efcacité de l’évérolimus sur le rejet aigu versus azathio-
prine en transplantation pulmonaire à 12 mois.
Le Courrier de la Transplantation - Volume VI - n
o 4 - octobre-novembre-décembre 2006
235
Mise
au point
Le temps d’ischémie froide.
L’âge du donneur.
Et, de manière plus spécique :
L’existence d’un reux gastro-œsophagien, facteur déter-
minant, diminué par des thérapeutiques médicamenteuses
(isoméprazole et dompéridone) ou chirurgicales (fundoplicature
sous cœlioscopie).
En termes de thérapeutiques, la modication du traitement
immunosuppresseur peut également jouer un rôle, mais, à ce
jour, aucun médicament n’a démontré un effet de réduction de
l’altération de la fonction respiratoire. Les résultats à 6 mois
comme à 3 ans de l’étude mycophénolate mofétil (MMF)
versus azathioprine en transplantation pulmonaire, analysant
315 patients, n’ont montré aucune différence signicative,
tant sur l’incidence du rejet aigu (56,6 % pour MMF versus
60,3 % à 3 ans) que sur celle de la BO (73 % pour MMF
versus 75 % à 3 ans ; p = 0,7) ou la survie des patients (75 %
pour MMF versus 69 % à 3 ans ; p = 0,18) [4, 5].
Aujourd’hui, l’apparition de nouvelles classes thérapeutiques
comme les inhibiteurs du signal de prolifération (ISP) permet
d’espérer améliorer la prise en charge des patients transplantés.
Ainsi, l’utilisation de l’évérolimus en transplantation pulmonaire
peut paraître attractive du fait de ses propriétés d’inhibition in
vitro du signal de prolifération des broblastes humains induit
par les facteurs de croissance (6, 7). Cependant, deux questions
se posent : l’évérolimus est-il efcace dans la prévention du rejet
aigu ainsi que dans celle de la BO en pratique clinique ?
L’étude B159, menée sur 213 patients de façon randomisée
et en double aveugle, a permis d’évaluer l’apport potentiel
en transplantation pulmonaire de l’évérolimus, aujourd’hui
commercialisé en transplantation rénale et cardiaque. Toutefois,
il faut souligner la faisabilité en transplantation pulmonaire
d’une étude randomisée de grande envergure en double aveugle.
Cette étude multicentrique a été réalisée dans 33 centres
(16 américains et 17 européens ou australiens) et comportait
deux bras de traitement : un bras évérolimus (101 patients)
et un bras azathioprine (112 patients) [8]. La période de
sélection a été de 3 à 6 semaines. Les patients pouvaient être
recrutés entre 3 à 36 mois post-transplantation et le critère
d’inclusion principal reposait sur un VEMS supérieur à 80 %
de la valeur de référence de l’ISHLT. La randomisation a été
effectuée lors de la première administration du traitement, à
savoir ciclosporine (à dose standard) + évérolimus (3 mg/j
sans suivi thérapeutique pharmacologique [STP]) + corticoïdes
pour le premier bras versus ciclosporine (à dose standard) +
azathioprine (1 à 3 mg/kg/j) + corticoïdes pour le second.
Le critère principal de jugement de l’efcacité était un critère
composite établi sur la combinaison d’une baisse du VEMS
supérieure à 15 %, de la perte du greffon, du décès ou de
la perte de vue à 12 mois. L’incidence de ce critère a été
significativement (p = 0,045) plus élevée dans le groupe
azathioprine (33,98 %) que dans le groupe évérolimus (21,8 %).
La progression de la BO a été, quant à elle, évaluée par la
diminution du VEMS par rapport au statut initial d’entrée
✓
✓
✓
dans l’étude (mesuré pendant la période précédant l’inclusion).
Chaque patient était donc son propre témoin. À 12 mois, ce
critère était en faveur de l’évérolimus. Ainsi, une diminution
du VEMS supérieure à 15 % a été statistiquement (p = 0,034)
plus importante dans le groupe azathioprine (27,7 %) que dans
le groupe évérolimus (15,8 %) [figure 6].
De plus, l’évérolimus apparaît aussi plus efficace que
l’azathioprine dans la prévention du rejet aigu, que ce soit
sur l’incidence du rejet aigu traité (7,9 % versus 32,1 % ;
p < 0,001), celle du rejet aigu suspecté cliniquement et prouvé
par biopsie (10,9 % versus 25,9 % ; p < 0,001) ou celle du
rejet prouvé par biopsie de grade supérieur à 2A (6,9 %
versus 17,9 % ; p = 0,022) [figure 7].
En revanche, comme dans les études princeps en transplantation
rénale et cardiaque, l’association d’évérolimus à des doses

Une pl@nète de
Solutions
Un site dédié aux Néphrologues
Une double expertise en IRC et Transplantation
Déléguer sa recherche documentaire et recevoir
des articles complets
C’est Pl@nète Roche Nephro
Imprimer ou commander des documents sur mesure
pour vos patients
C’est Pl@nète Roche Nephro
Trouver une iconographie pour votre EPU
C’est Pl@nète Roche Nephro
Télécharger le diaporama de votre choix
C’est Pl@nète Roche Nephro
Demandez à
votre attaché
scientifique
Roche votre
bulletin d’inscription.
Pour en savoir plus
planete.nephro@roche.com
NOUVEAU
www.roche.fr
Terre Neuve
-Etabli le 11/06/06.
13631_AP 210X270_E2 12/10/06 15:25 Page 1
Le Courrier de la Transplantation - Volume VI - n
o 4 - octobre-novembre-décembre 2006
236
Mise
au point
standard de ciclosporine a montré qu’elle potentialisait la
néphrotoxicité de cette dernière. Ainsi, la fonction rénale a
été moins bonne dans le bras évérolimus. À 12 mois, sur les
63 patients traités par évérolimus, la créatininémie a été en
moyenne de 176 ± 78 versus 158 ± 50 µmol/l pour les patients
sous azathioprine (p = 0,108). Les résultats étaient signicatifs
sur la différence calculée par rapport à l’état basal : 43 ± 62 µmol/
l versus 14 ± 37 µmol/l (p < 0,001). Comme en transplantation
rénale, des études utilisant l’évérolimus avec des doses réduites
de ciclosporine seront nécessaires pour valider le fait que l’on
peut améliorer les résultats sans pénaliser la fonction rénale.
En termes de sécurité, le bilan infectieux à 12 mois, toutes
infections confondues, était équivalent (82 % versus 80,2 %
pour l’azathioprine). Cependant, on observe une répartition
différente, avec, dans le bras évérolimus, plus d’infections
bactériennes (35,1 % versus 17,1 % ; p = 0,004) et plus
d’infections fongiques (27,9 % versus 14,4 % ; p = 0,021)
dont 3 à 4 % ont été traitées avec de l’amphotéricine B par
voie systémique. L’incidence des infections virales a été
similaire dans les deux groupes (29,7 % versus 28,8 %). Il
faut cependant pondérer ce dernier résultat par la mise en
place quasi systématique d’une prophylaxie par le ganciclovir
en transplantation pulmonaire.
Par ailleurs, la revue des effets indésirables de la base de données
de l’ensemble des études cliniques réalisées en transplantation
rénale (B201/B251), cardiaque (B253) et pulmonaire (B159) a
permis de recenser les anomalies pulmonaires non infectieuses
de type pneumopathie interstitielle incluant des formes de
pneumonie, brose pulmonaire, granulomatose pulmonaire,
BOOP et pneumonie cytogénique organisée. Au total, 6 cas
ont été rapportés avec l’évérolimus 3 mg, versus un cas sous
MMF. Aucun cas n’a été rapporté avec 1,5 mg d’évérolimus.
En conclusion, cette incidence correspond à 1 % à des patients,
ce qui est habituellement observé.
À 24 mois, l’incidence de la diminution du VEMS > 15 %
a été de 41,1 % pour l’azathioprine versus 34,7 % pour
l’évérolimus, sans différence signicative (p = 0,333). Les
résultats signicatifs sur l’incidence des rejets aigus traités
ont été conservés et restent supérieurs avec l’évérolimus
(14,9 % versus 41,1 % ; p < 0,001), y compris sur les rejets
aigus suspectés cliniquement et prouvés par biopsie (19,8 %
versus 33,9 % ; p = 0,018).
Ces résultats s’expliquent par le fait que la répartition des
patients encore sous traitement à 24 mois a été différente
de celle des résultats à 12 mois. Dans le groupe évérolimus,
sur 101 patients inclus, 61,4 % ont arrêté leur traitement :
41,6 % pour événement indésirable et 8,9 % pour efcacité
insufsante. Dans le groupe azathioprine, sur 112 inclusions,
46,4 % des patients ont arrêté leur traitement : 19,6 % pour
effets indésirables et 17,9 % pour effet thérapeutique insufsant.
Cette répartition inégale limite donc l’analyse à 24 mois en
provoquant un important déséquilibre entre les deux groupes
et une diminution certaine de la puissance de l’essai.
De plus, le choix d’une dose xe d’évérolimus à 3 mg/j, sans suivi
thérapeutique pharmacologique de ses concentrations sanguines,
en particulier chez les patients porteurs d’une mucoviscidose et
en association à une dose standard de ciclosporine, représente une
pratique médicale très différente de l’approche optimisée au plan
individuel préconisée aujourd’hui dans l’AMM de ce nouveau
immunosuppresseur. On peut cependant constater dans cette étude
en transplantation pulmonaire que la fourchette de taux résiduels
d’évérolimus efcace et bien tolérée varie entre 3 et 12 ng/ml en
association avec de la ciclosporine et des corticoïdes (9).
concLusIon
Cette étude B159 montre une efcacité en faveur de l’évérolimus à un
et deux ans en termes de prévention du rejet aigu et à un an en termes
de rejet chronique. Toutefois, l’évérolimus, lorsqu’il est associé à
des doses standard de ciclosporine, s’accompagne d’une plus forte
incidence des infections bactériennes et fongiques ainsi que d’une
potentialisation de la néphrotoxicité de la ciclosporine. Cependant,
c’est la première fois qu’un immunosuppresseur démontre qu’il
est possible d’obtenir un ralentissement de la perte de la fonction
respiratoire à un an, et donc un effet potentiel sur la BO.
L’utilisation d’évérolimus en transplantation pulmonaire peut
être envisagée sérieusement et, pour optimiser cette approche,
un nouvel essai clinique de type académique (australo-européen)
est actuellement mis en place dans quelques centres français. Il a
pour objectif d’évaluer l’efcacité et la tolérance de deux types
d’association : ciclosporine à dose réduite plus évérolimus versus
ciclosporine à dose standard plus acide mycophénolique. ■
RéféRences bibliogRaphiques
1. Boehler A, Estenne M. Post-transplant bronchiolitis obliterans. Eur
Respir J 2003;22(6):1007-18.
2. Cooper JD, Billingham M, Egan T et al. A working formulation for
the standardization of nomenclature and for clinical staging of chronic
dysfunction in lung allografts. International Society for Heart and Lung
Transplantation. J Heart Lung Transplant 1993;12(5):713-6.
3. Estenne M, Maurer JR, Boehler A et al. Bronchiolitis obliterans syndrome
2001: an update of the diagnostic criteria. J Heart Lung Transplant 2002;
21(3):297-310.
4. Palmer SM, Baz MA, Sanders L et al. Results of a randomized, prospective,
multicenter trial of mycophenolate mofetil versus azathioprine in the prevention
of acute lung allograft rejection. Transplantation 2001;27;71(12):1772-6.
5. McNeil K, Glanville AR, Wahlers T. Comparison of mycophenolate mofetil
and azathioprine for prevention of bronchiolitis obliterans syndrome in de novo
lung transplant recipients. Transplantation 2006;15;81(7):998-1003.
6. Azzola A, Havryk A, Chhajed P et al. Everolimus and mycophenolate
mofetil are potent inhibitors of broblast proliferation after lung transplan-
tation. Transplantation 2004;27;77(2):275-80.
7. Poirier CD. Promise of Neoral C2, basiliximab, and everolimus in lung
transplantation. Transplant Proc 2004;36(2 suppl.):509S-513S.
8. Snell GI, Valentine VG, Vitulo P et al. Everolimus versus azathioprine
in maintenance lung transplant recipients: an international, randomized,
double-blind clinical trial. Am J Transplant 2006;6(1):169-77.
9. Kovarik JM, Snell GI, Valentine V et al. Everolimus in pulmonary trans-
plantation: pharmacokinetics and exposure-response relationships. J Heart
Lung Transplant 2006;25(4):440-6.
1
/
4
100%