L’ Quelles sont les indications actuelles de la chirurgie dans le cancer

La Lettre de l'Hépato-gastroentérologue • Vol. XX - n° 3 - mai-juin 2017 | 137
EVIDENCE-BASED MEDICINE
Oncologie
Quelles sont les indications actuelles
de la chirurgie dans le cancer
de l’œsophage ?
Pierre Cattan*
* Service de chirurgie générale, diges-
tive et endocrinienne, hôpital Saint-
Louis, Paris.
L’
indication de résection chirurgicale d’un
cancer de l’œsophage dépend de la
résécabilité tumorale et de l’opérabilité
du patient. Elle ne sera portée que chez 15 à 20 %
des patients, pour une survie dépassant rarement
40 % à 5 ans (1), au terme d’une approche souvent
multimodale.
Les patients porteurs de métastases viscérales
ou d’adénopathies sus-claviculaires ou lombo-
aortiques, ainsi que ceux porteurs d’un cancer
associé non curable, ne seront jamais opérés en
vue d’une résection, quelle que soit l’évolution
de la maladie après traitement systémique et/
ou locorégional. Il en est de même des patients
dont la tumeur est classée ycT4b (envahissement
de l’aorte, de l’arbre trachéobronchique, du
nerf récurrent gauche ou d’un corps vertébral),
au terme d’un traitement néo adjuvant. Dans
toutes les autres situations, y compris en
présence d’adénopathies du tronc cœliaque ou
de la région cervicale si elles sont résécables, une
intervention de résection doit être discutée en
fonction de l’opérabilité du patient. Les contre-
indications opératoires absolues et définitives
sont une cirrhose décompensée ou avec varices
œsophagiennes, une cardiopathie évolutive,
une insuf fisance rénale chronique (débit de
filtration glomérulaire < 60 ml/mn/1,73 m
2
) et
une insuffisance respiratoire (VEMS [volume
expiratoire maximal par seconde] < 1 L). Certaines
contre-indications opératoires peuvent être
levées, tel un état de dénutrition sévère ou une
insuffisance coronarienne susceptible d’être traitée
par un geste de revascularisation. L’âge avancé
n’est pas une contre-indication, mais l’avis d’un
oncogériatre est utile pour juger du bien-fondé de
l’intervention. En l’absence de contre-indication
opératoire, un pronostic carcinologique sombre
associé à un risque opératoire élevé peut conduire
à une remise en question de l’indication opératoire.
Situations particulières
Cancers superficiels (T1)
La résection endoscopique par mucosectomie ou
dissection sous-muqueuse est une option curative
pour certains cancers superficiels. Cependant, en
raison du risque métastatique ganglionnaire, la
chirurgie est indiquée (de première intention ou
après résection endoscopique) en cas de tumeur
peu différenciée, d’emboles lymphatiques ou
vasculaires ou d’envahissement pariétal > sm1
(partie superficielle de la sous-muqueuse : 500 μm)
pour les adénocarcinomes (risque d’envahissement
ganglionnaire : 44 % pour les sm2 ou sm3)
et > m2 (envahissement de la muqueuse) pour
les épidermoïdes (risque d’envahissement
ganglionnaire : 8 à 18% pour les m3 (envahissement
de la musculaire-muqueuse). Il est à noter que la
stratégie visant à adjoindre une radiochimiothérapie
adjuvante à la résection endoscopique de tumeur
T1 à haut risque ganglionnaire est une pratique
courante au Japon (2) et qu’elle tend à être
considérée comme une alternative possible à la
chirurgie en Europe (3).
Une sélection optimale des patients pour la chirurgie du cancer de
l’œsophage, en termes de risque opératoire et de bénéfice attendu sur
le plan carcinologique, participe à l’amélioration de ses résultats. C’est
à ce prix que la résection chirurgicale gardera une place centrale dans le
traitement curatif de ce cancer. Une décision d’abstention chirurgicale
est le plus souvent prise face à une contre-indication carcinologique ou
opératoire formelle, mais aussi de manière plus nuancée en fonction du
risque opératoire et du pronostic carcinologique, ce d’autant qu’existent
des alternatives thérapeutiques potentiellement curatives.
Ce qu’il faut retenir
niveau
depreuve
1

138 | La Lettre de l'Hépato-gastroentérologue • Vol. XX - n° 3 - mai-juin 2017
Contre-indication
opératoire
– Cirrhose hépatique
– Varices œsophagiennes
– Insuffisance rénale chronique
– Insuffisance respiratoire
– Cardiopathie évolutive
Traitement potentiellement curatif
– RCT exclusive
– Résection endoscopique + RCT pour T1
à haut risque ganglionnaire
Exérèse chirurgicale
Situations particulières
– Œsophagectomie de sauvetage
Diagnostic
Contre-indication
carcinologique
Pas de chirurgie palliative (R1-R2)
– M1 (N+ lombo-aortiques
et sus-claviculaires)
– N+ ou T4b non résécables après
traitement néo-adjuvant
– Cancer associé non curable
Traitement symptomatique
50 % 25 %
– Réponse clinique complète
– Absence de réponse à la RCT
M1 : métastases viscérales à distance
N+ : adénopathies métastatiques
T1 : cancer superficiel ; RCT : radio-chimiothérapie
R1-R2 : radicalité de la résection :
marges de résection < 1 mm ou absente.
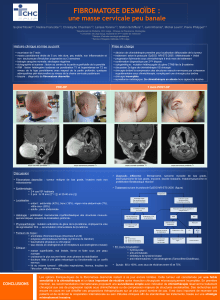
Figure. Algorithme thérapeutique.
EVIDENCE-BASED MEDICINE Oncologie
1. Shapiro J, van Lanschot JJ, Hulshof MC et al. Neo adjuvant chemoradiotherapy plus surgery
versus surgery alone for oesophageal or junctional cancer (CROSS): long-term results of
a randomised controlled trial. Lancet Oncol 2015;16(9):1090-8.
2. Yamashina T, Ishihara R, Nagai K et al. Long-term outcome and metastatic risk after
endoscopic resection of superficial esophageal squamous cell carcinoma. Am J Gastroen-
terol 2013;108(4):544-51.
3. Pimentel-Nunes P, Dinis-Ribeiro M, Ponchon T et al. Endoscopic submucosal dissection: Euro-
pean Society of Gastrointestinal Endoscopy (ESGE) Guideline. Endoscopy 2015;47(9):829-54.
4. Vincent J, Mariette C, Pezet D. et al. Early surgery for failure after chemoradiation in
operable thoracic oesophageal cancer. Analysis of the nonrandomized patients in FFCD
9102 phase III trial: Chemoradiation followed by surgery versus chemoradiation alone. Eur
J Cancer 2015;51(13):1683-93.
5. Markar S, Gronnier C, Duhamel A et al. Salvage surgery after chemoradiotherapy in
the management of oesophageal cancer: Is it a viable therapeutic option? J Clin Oncol
2015;33:3866-73.
Références bibliographiques
Réponse complète clinique (RCC)
après traitement néoadjuvant
Parmi les patients en RCC après radio-chimio thérapie
(RCT) [disparition endoluminale de la tumeur avec
biopsies négatives, absence de progression des lésions
visibles en imageries et Standard Uptake Value < 4
en TEP-TDM], il n’existe pas d’outil permettant de
discerner les patients en réponse pathologique
complète susceptibles de ne tirer aucun bénéfice d’une
résection chirurgicale. En réponse à cette situation,
l’essai PRODIGE 32 – ESOSTRATE (FFCD 1401) évalue
les résultats de 2 stratégies : la chirurgie systé matique
et la surveillance versus la chirurgie de recours après
RCC à la RCT. Dans l’attente des conclusions de cet
essai prévues en 2023, ces 2 stratégies sont possibles et
discutées en réunion de concertation pluridisciplinaire,
en prenant en compte le risque opératoire.
Absence de réponse après RCT
L’analyse du devenir des 192 patients non
répondeurs à la RCT de l’essai FFCD 9102 a établi
que l’œsophagectomie était associée à une
médiane de survie supérieure à celle des patients
non répondeurs et non opérés (17 versus 5,5 mois),
et identique à celle des patients répondeurs à la
RCT (4). L’indication de résection chez les patients
non répondeurs est donc licite, si la tumeur est
résécable et le patient opérable.
Œsophagectomie
de sauvetage
après RCT exclusive
Une étude européenne a comparé le devenir de
308 patients ayant eu une œsophagectomie de
sauvetage pour persistance ou récidive tumorale
après RCT exclusive à celui de 540 patients opérés
après RCT néoadjuvante (5).
Il n’était pas mis en évidence de différence en
termes de mortalité ou de survie à long terme
entre les 2 groupes. Le pronostic carcinologique
était cependant moins bon lorsque l’indication
d’œsophagectomie de sauvetage était une
persistance plutôt qu’une récidive tumorale. ■
Question
non résolue
» L’intérêt d’une résection
chirurgicale en cas
de réponse clinique
complète après traitement
néo-adjuvant reste
débattu. Cette question
fait actuellement l’objet
d’une étude contrôlée.

La Lettre de l'Hépato-gastroentérologue • Vol. XX - n° 3 - mai-juin 2017 | 139
Scanner thoraco-abdomino-pelvien
injecté
Sténose ou hémorragie
non contrôlable
N+ et/ou ≥ T3
N+ et/ou ≥ T2
N0 et < T3
Échoendoscopie
Chimiothérapie
péri-opératoire
Résection
chirurgicale
N0 et < T2
Figure. Arbre décisionnel pour l’adénocarcinome gastrique opérable.
EVIDENCE-BASED MEDICINE
Oncologie
À qui prescrire une chimiothérapie
néo-adjuvante dans l’adénocarcinome
gastrique ?
Thomas Aparicio*
Une chimiothérapie péri-opératoire à base de sels de platine permet
d’améliorer la survie des patients atteints d’un adénocarcinome gastrique
opérable.
Ce traitement n’est pas indiqué en cas de tumeur superficielle.
Le bénéfice du traitement péri-opératoire est essentiellement apporté
par le traitement préopératoire.
Ce qu’il faut retenir
Niveau
depreuve
1
L
e cancer gastrique reste un cancer fréquent
en France, avec une incidence de 6 585 cas en
2015, dont 48 % après 75 ans. Le pronostic des
adénocarcinomes gastriques opérés reste mauvais,
avec un taux élevé de récidive. Depuis maintenant
une dizaine d’années, le concept de chimiothérapie
péri-opératoire s’est imposé. La chimiothérapie péri-
opératoire est administrée en préopératoire et en
postopératoire. La chimiothérapie préopératoire
a pour but de réduire la taille tumorale, ce qui va
augmenter le taux de résection R0, mais également
de traiter les micrométastases pour diminuer le
risque de récidive. En effet, la chimiothérapie est
plus facilement administrée en préopératoire qu’en
postopératoire. Deux grandes études randomisées
de phase III ont comparé la chimiothérapie péri-
opératoire à la chirurgie seule (1, 2). Dans la
première étude, le schéma ECF associant épirubicine,
5-fluorouracil (5-FU) et cisplatine (3 cures espacées
de 3 semaines avant et après la chirurgie) a permis
d’obtenir 36 % de survie à 5 ans versus 23 % en
l’absence de chimiothérapie (HR : 0,75 ; IC95 : 0,60-
0,93 ; p = 0,009). Dans la seconde, avec le schéma
associant 5-FU et cisplatine (2 ou 3 cures espacées
de 4 semaines avant et après la chirurgie), on observe
38 % de survie à 5 ans versus 24 % en l’absence
de chimiothérapie (HR : 0,69 ; IC95 : 0,50-0,95 ;
p = 0,02). Dans ces 2 études, 86 % et 87 % des
patients ont pu recevoir le traitement protocolaire
préopératoire, alors que seulement 55 % et 50 %
d’entre eux ont pu bénéficier de la chimiothérapie
postopératoire. Le bénéfice semblait s’appliquer
à toutes les tranches d’âge et quel que soit l’état
général des patients, aux 2 sexes, et à toutes les
localisations dans l’étude britannique. Aucune
étude de sous-groupes concernant le stade, le type
histologique ou le nombre de cures reçues n’est
disponible. La majorité des patients inclus dans ces
2 études avait un adénocarcinome de stade avancé
(T3-T4 : 57 %, N+ : 66 à 71 %).
Le Thésaurus national de cancérologie diges-
tive (TNCD) [www.tncd.org] recommande une
chimiothérapie péri-opératoire pour tous les
malades de stade supérieur à IA avec un niveau élevé
de recommandation (grade A) [figure].
* Service de gastroentérologie et oncologie digestive, hôpital Saint-Louis
(AP-HP) ; université Paris 7, Sorbonne Paris Cité, Paris.

140 | La Lettre de l'Hépato-gastroentérologue • Vol. XX - n° 3 - mai-juin 2017
EVIDENCE-BASED MEDICINE Oncologie
Cependant, les schémas de chimiothérapie proposés
dans les études FFCD-FNCLCC et MAGIC sont des
schémas responsables d’une toxicité importante.
Il a été montré par plusieurs études en situation
métastatique que les chimiothérapies à base d’oxa-
liplatine étaient mieux tolérées que celles à base
de cisplatine, notamment chez les patients de
plus de 65 ans. Une étude rétrospective française
de l’AGEO (Association des gastro-entérologues
oncologues) a montré de bons résultats pour le taux
de résection R0, la survie sans récidive et la survie
globale avec une chimiothérapie péri-opératoire par
FOLFOX bimensuel (3). Les patients recevaient un
nombre médian de 6 cures de chimiothérapie au
total, dont 4 en préopératoire. La chimiothérapie
péri-opératoire par FOLFOX est maintenant une
option reconnue par le TNCD.
Il faut noter que l’âge médian des patients inclus
dans les études (62 ans dans l’étude MAGIC, 63 ans
dans l’étude FFCD-FNCLCC et 66 ans dans l’étude
AGEO) est inférieur à l’âge au diagnostic du cancer
de l’estomac, qui est proche de 70 ans. Une éva-
luation gériatrique peut être nécessaire pour aider
à prendre la décision d’une chimiothérapie pré-
opératoire. En effet, une chimiothérapie sous-dosée
par crainte des effets indésirables risque de ne pas
être efficace et une chimiothérapie normalement
dosée peut être responsable de toxicités ou d’alté-
ration de l’état nutritionnel pouvant retarder le
geste chirurgical.
Certaines caractéristiques tumorales ont été récem-
ment rapportées comme pouvant influer sur l’effi-
cacité de la chimiothérapie péri-opératoire. Ainsi,
l’instabilité microsatellitaire présente dans environ
20 % des adénocarcinomes gastriques et probable-
ment plus fréquemment chez les patients de plus de
75 ans est associée à un meilleur pronostic spontané
et à une plus faible efficacité de la chimiothérapie,
selon des données rétrospectives (4). D’autre part,
les patients atteints par le sous-type histologique
des tumeurs à cellules indépendantes paraissent
également ne pas tirer bénéfice d’une chimiothé-
rapie néo-adjuvante, selon les résultats d’une grande
étude rétrospective française (5). En outre, il n’est pas
encore établi, pour les tumeurs surexprimant HER-2,
que l’inhibition de ce récepteur améliore les résultats
de la chimiothérapie péri-opératoire. Les résultats
d’études prospectives sont attendus prochainement.
Enfin, les patients dont la tumeur est responsable
d’hémorragies significatives doivent être opérés
d’emblée. Pour les patients présentant une intolé-
rance alimentaire importante et dénutris, la renu-
trition sera le premier temps thérapeutique. Une
discussion multidisciplinaire approfondie devra avoir
lieu pour décider, selon le cas, soit d’une chimio-
thérapie néo-adjuvante avec assistance nutrition-
nelle, soit d’une chirurgie d’emblée.
En conclusion, la chimiothérapie péri-opératoire
est une avancée significative dans le traitement des
adénocarcinomes gastriques localisés. Tous les dos-
siers des patients doivent être présentés en réunion
de concertation pluridisciplinaire après le diagnostic
d’un adénocarcinome gastrique pour discuter la
meilleure stratégie thérapeutique au cas par cas. Des
interrogations sont apparues concernant le bénéfice
apporté par la chimiothérapie péri-opératoire dans
certains sous-groupes de patients et doivent faire
l’objet d’études prospectives spécifiques. ■
Questions
non résolues
» La chimiothérapie
péri-opératoire
est-elle bénéfique
pour les patients
atteints d’une tumeur à
cellules indépendantes
ou avec instabilité
des microsatellites ?
» La chimiothérapie
néo-adjuvante est-elle
indiquée pour tous les
patients âgés ?
1. Cunningham D, Allum WH, Stenning SP et al. Periope-
rative chemotherapy versus surgery alone for resectable
gastroesophageal cancer. N Engl J Med 2006;355(1):11-20.
2. Ychou M, Boige V, Pignon JP et al. Perioperative che
-
motherapy compared with surgery alone for resectable
gastroesophageal adenocarcinoma: an FNCLCC and FFCD
multicenter phase III trial. J Clin Oncol 2011;29(13):1715-21.
3. Mary F, Zaanan A, Boige V et al. Perioperative
chemotherapy with FOLFOX in resectable gastro-
esophageal adenocarcinoma in real life practice:
An AGEO multicenter retrospective study. Dig Liver
Dis 2016;48(12):1498-502.
4. Kim SY, Choi YY, An JY et al. The benefit of microsatellite
instability is attenuated by chemotherapy in stage II and
stage III gastric cancer: Results from a large cohort with
subgroup analyses. Int J Cancer 2015;137(4):819-25.
5. Messager M, Lefevre JH, Pichot-Delahaye V et al.
The impact of perioperative chemotherapy on sur-
vival in patients with gastric signet ring cell adenocar-
cinoma: a multicenter comparative study. Ann Surg
2011;254(5):684-93.
Références bibliographiques

La Lettre de l'Hépato-gastroentérologue • Vol. XX - n° 3 - mai-juin 2017 | 141
EVIDENCE-BASED MEDICINE
Oncologie
Quand peut-on envisager le traitement
local des métastases hépatiques
dans le cancer colorectal ?
Michel Rivoire*
* Département de chirurgie, centre
Léon-Bérard, Lyon.
D
urant les 15 dernières années, les stra-
tégies de traitement local des patients
atteints d’un cancer colorectal métasta-
tique (CCRm) ont beaucoup évolué et permis une
amélioration des résultats cliniques. La discussion
des dossiers en réunion de concertation pluridis-
ciplinaire (RCP), dans des centres spécialisés, est
une nécessité pour l’évaluation de la résécabilité
(métastases hépatiques [MH] résécables, poten-
tiellement résécables ou définitivement non résé-
cables) et la définition de la stratégie thérapeutique
(niveau de preuve 4, grade de recommandation B).
Elle est fondée sur des critères techniques (chirurgi
-
caux) et carcinologiques (pronostiques). La défini-
tion moderne de la résécabilité technique est basée
sur la possibilité d’une résection complète des MH
(R0) laissant en place plus de 30 % de foie sain
fonctionnel (ou un rapport poids du foie restant/
poids du corps supérieur à 0,5). Le taux de récidive
d’environ 50 % à 3 ans rend nécessaire l’utilisation
de critères carcinologiques pour évaluer les chances
de survie sans récidive et de guérison (4, B). Les
principaux facteurs de risque validés dans des
études rétrospectives sont le nombre et la taille des
MH, la présence de métastases extrahépatiques,
le stade de la tumeur primitive et l’intervalle libre
sans maladie, ainsi que le dosage des marqueurs
tumoraux (ACE, CA 19-9). Le score de Fong (Clinical
Risk Score) est le plus utilisé (1).
La résection hépatique est le standard de traitement
des MH isolées. Elle assure les meilleurs taux de
survie, qu’elle soit réalisée en 1 temps, en 2 temps
ou de manière itérative (4, B). Chez les patients pré-
sentant des MH résécables et des critères carcinolo-
giques favorables (en particulier MH métachrones),
la résection d’emblée ou la chimiothérapie péri-opé-
ratoire sont les 2 options (1, C). En effet, dans l’étude
EPOC, la survie globale à 5 ans du groupe chimio-
thérapie péri-opératoire était de 51 % contre 48
dans le groupe chirurgie d’emblée (RR = 0,88 ; IC95 :
0,68-1,14 ; p = 0,34) [2]. Chez les patients présentant
des MH résécables et des critères carcinologiques
défavorables, une chimiothérapie péri-opératoire
par FOLFOX est recommandée (1, B), sans adjonc-
tion d’une thérapie ciblée (2, E). La chimiothérapie
péri-opératoire est préconisée chez les patients
ayant des critères carcinologiques défavorables
et une résécabilité borderline ainsi que chez les
patients porteurs d’un cancer colorectal avec MH
synchrones (4, B). La chimio thérapie adjuvante n’est
pas recommandée chez les patients ayant des cri-
tères pronostiques favorables (sauf s’ils n’ont jamais
reçu de chimiothérapie par oxali platine) [2, C], alors
que les patients présentant des critères défavorables
peuvent bénéficier d’un tel traitement (3, B).
Chez les patients porteurs de MH potentiel-
lement résécables, une chimiothérapie première
permettant d’obtenir une forte réduction de taille
tumorale (chimiothérapie de conversion) est recom-
mandée (2, A). Son efficacité doit être évaluée après
4 cures. Les options dépendent des caractéristiques
moléculaires de la tumeur. Pour une tumeur RAS
sauvage, les 3 options sont une bichimiothérapie
associée à un anti-EGFR, une trichimiothérapie
associée à du bévacizumab ou, plus rarement, une
La place des traitements locaux (résection et ablation par voie chirurgicale
ou percutanée) des métastases hépatiques (MH) du cancer colorectal n’a
cessé de s’accroître au cours des 15 dernières années. La définition de la
résection a changé. Alors que dans les années 1990 elle était réservée aux
patients porteurs de moins de 4 MH, l’approche actuelle se concentre
sur la quantité de foie sain conservable et la possibilité d’un nouveau
traitement local en cas de récidive. L’utilisation de chimiothérapies
péri-opératoires et de chimiothérapies de conversion est maintenant
mieux codifiée. Dans ce cadre, les techniques d’ablation avec ou sans
résection sont considérées comme une alternative efficace de prise en
charge pour les patients porteurs de MH non résécables préalablement
contrôlées par une chimiothérapie.
Ce qu’il faut retenir
Niveaux
de preuve
1-4
 6
6
1
/
6
100%