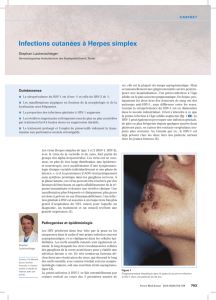
HSV-1 HSV-2

Virus herpes simplex
Physiopathologie, Epidémiologie, Pouvoir pathogène
SFM 26/11/2014
Flore Rozenberg

Virus Herpes Simplex
Latence – Réactivation
Neuro-tropisme/virulence/invasion

Réplication : cycle lytique
α β γ
précoce précoce très tardive
glycoprotéines
NOYAU
CYTOPLASME
transcription
réplication
ADN
assemblage
bourgeonnement
fusion
décapsidation
d’après B.Roizman
In vitro
In vivo

Latence : établissement
Koyuncu, 2013

Latence : maintien
Koyuncu, 2013
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
1
/
24
100%